Дата: Подпись преподавателя:
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 5
Тема: Обмен простых белков
Задания для подготовки к занятию:
1. Напишите формулами реакции трансаминирования между следующими парами аминокислот и a-кетокислот:
А) Глу + Пируват ®
Б) Глу + Оксалоацетат ®
2. Напишите названия продуктов, образующихся в реакциях:
А)
Б)
3. Напишите полное название ферментов по обратной реакции:
А)
Б)
4. Назовите вид дезаминирования аминокислот:
А. Ала | 1. Прямое окислительное |
Б. Гис | 2. Прямое неокислительное |
В. Тре | 3. Непрямое |
Г. Глу | |
Д. Фен |
5. Напишите названия коферментов и соответствующих витаминов, необходимых для осуществления реакций непрямого дезаминирования:
А)
Б)
6. Чем определяется центральная роль глутаминовой кислоты в промежуточном обмене аминокислот?
7. Назовите конечные продукты азотистого обмена, которые выводятся из организма:
8. Назовите процессы – источники аммиака в организме:
9. На каких клетках прежде всего сказывается токсическое действие аммиака? Каковы механизмы токсического действия аммиака?
10. Перечислите способы обезвреживания аммиака в организме:
в мозге:
в мышцах:
в печени:
в почках:
11. Напишите суммарное уравнение синтеза мочевины. Сколько моль АТФ требуется для синтеза 1 моль мочевины. Напишите реакции, идущие с затратой энергии (АТФ), укажите ферменты.
12. Проследите путь азота аминогруппы аланина в мочевину, составив схему:
Ала ® 1 ® 2 ® 3 ® Мочевина
1.
2.
3.
13. При нарушениях орнитинового цикла в крови повышается содержание:
А. Аланина
Б. Орнитина
В. Глутамата (глутаминовой кислоты)
Г. Глутамина (амида глутаминовой кислоты)
Д. Аммиака
ЛАБОРАТОРНАЯ РАБОТА 14
Тема: Количественное определение активности аланинаминотрансферазы (АлАТ) в сыворотке крови
Цель: Изучить активность аланинаминотрансферазы (АлАТ) в сыворотке крови, ее значение для диагностики гепатита.
Принцип метода: Аминотрансферазы или трансаминазы катализируют межмолекулярный перенос аминогруппы с амнокислот на кетокислоты. Коферментом трансаминаз является фосфопиридоксаль, который служит непосредственным переносчиком аминогрупп с аминокислоты на кетокислоту. АлАТ катализирует реакцию переаминирования между аланином и a-кетоглутаровой кислотой:

α- кетоглутарат | Аланин | Глутамат | пируват |
По количеству образовавшейся пировиноградной кислоты можно судить об активности фермента. Количество пировиноградной кислоты определяется колориметрическим путем по цветной реакции с 2,4-динитрофенилгидразином, при которой развивается красно-бурое окрашивание:

Пируват | 2,4-ДНФГ | 2,4-ДНФ-гидразон пирувата |
Повышение активности АлАТ наблюдается при заболеваниях печени, а повышение активности АсАТ – при патологии сердечной мышцы.
Активность АлАТ в норме составляет 28 – 190 нмоль/с×л
Схема постановки опыта
Контрольная проба | Опытная проба | |
Реагент 1 (АлАТ, субстрат), мл | 0,25 | 0,25 |
Дистиллированная вода, мл | 0,05 | – |
Сыворотка, мл | – | 0,05 |
Перемешать и инкубировать 30 мин | ||
Реагент 2 (динитрофенилгидразин), мл | 0,25 | 0,25 |
Перемешать и оставить при комнатной температуре на 20 мин | ||
NaOH (С = 0,4 моль/л), мл | 2,5 | 2,5 |
Перемешать и через 10 минут измерить оптическую плотность пробы против контрольной пробы при длине волны 540 нм, кювета с толщиной слоя 5 мм. Активность АлАТ в опытной пробе определить по калибровочному графику в нмоль/с×л.
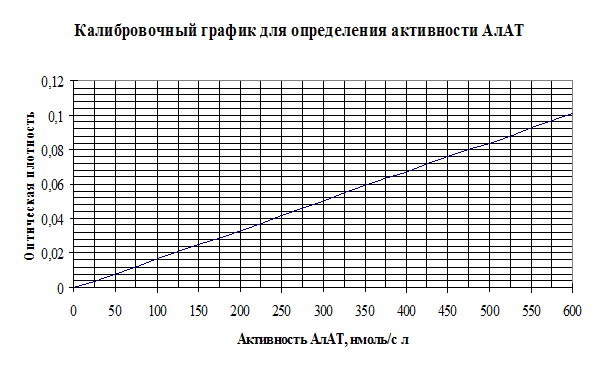
Результат анализа:
Вывод:
Дата: Подпись преподавателя:
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ 4
Семинар Патологии белкового обмена
Вопросы для подготовки к семинару:
1. Нарушения азотистого баланса
2. Нарушения переваривания белков в желудке и кишечнике
3. Нарушения обмена аммиака. Гипераммониемия
4. Нарушения синтеза мочевины
5. Нарушения обмена фенилаланина и тирозина
6. Гиповитаминозы витаминов – участников обмена белка
7. Патологии печени и их влияние на обмен белков
8. Нарушения катаболизма пуриновых нуклеотидов. Подагра
9. Проблемы синтеза коллагена
10. Наследственные заболевания белкового обмена
ЛАБОРАТОРНОЕ ЗАНЯТИЕ 6
Тема: Обмен сложных белков
Задания для подготовки к занятию:
1. Выберите положения, правильно характеризующие функции АТФ в организме:
А. Продукт окислительного фосфорилирования
Б. Источник энергии при связывании аа-тРНК с рибосомой
В. Субстрат аденилатциклазы
Г. Регулятор метаболических процессов
Д. Донор фосфата в реакциях, катализируемых протеинкиназами
Е. Источник энергии для транспорта веществ путем облегченной диффузии
2. Нарисуйте пуриновое кольцо и покажите происхождение в нем отдельных атомов.
3. При катаболизме пуриновые основания превращаются в мочевую кислоту, используя цифровые обозначения, расположите перечисленные метаболиты в порядке их превращения в мочевую кислоту:
1. АМФ; 2. мочевая кислота; 3. ксантин; 4. инозин; 5. аденозин; 6. гипоксантин.
5. Напишите схему синтеза гема.
7. Напишите схему катаболизма гема до образования конечных продуктов, выделяемых из организма.
1. Заполните таблицу дифференциальной диагностики различных типов желтух
Название желтухи | Причины возникновения | Биохимические показатели обмена билирубина | |||||
кровь | моча | кал | |||||
общий билирубин | непрямой билирубин | прямой билирубин | прямой билирубин | уробилин | стеркобилин | ||
ЛАБОРАТОРНАЯ РАБОТА 15
Тема: Определение содержания билирубина в сыворотке крови
Цель: Научиться определять содержание билирубина в сыворотке крови, изучить значение этого показателя для дифференциальной диагностики патологий (желтух).
Принцип метода:
Прямой (связанный, конъюгированный с глюкуроновой кислотой) билирубин непосредственно реагирует с диазотированной сульфаниловой кислотой, а общий билирубин – в присутствии кофеинового реагента с образованием окрашенного азосоединения. Интенсивность окраски реакционной среды пропорциональна концентрации билирубина и измеряется фотометрически при длине волны 535 (500-560) нм в кювете с толщиной поглощающего слоя 5 мм.
Схема постановки опыта:
Подготовьте пробы следующего состава | Опытная проба | Контрольная проба | Калибровочная проба | |
Общий билирубин | Прямой билирубин | |||
Сыворотка, мл | 0,2 | 0,2 | 0,2 | - |
Реагент №1, мл | 1,4 | - | - | 1,4 |
Реагент №4, мл | 0,2 | 1,6 | 1,8 | 0,2 |
Калибратор, мл | - | - | - | 0,2 |
Диазореагент, мл | 0,2 | 0,2 | - | 0,2 |
Пробы тщательно перемешайте.
Для определения прямого билирубина (точно!) через 5 минут (комнатная температура) измерьте величину оптической плотности опытной пробы против контрольной пробы при длине волны 535 нм (500-560).
Для определения общего билирубина через 20 мин (комнатная температура) измерьте величину оптической плотности опытной пробы против контрольной пробы при длине волны 535 нм (500-560).
Оптическую плотность калибратора измерьте против дистиллированной воды через 20 мин (комнатная температура) при длине волны 535 нм (500-560).
Расчёт концентрации билирубина в пробе (С) проведите по формуле:
Е пробы
C = -------------- х 85,5мкмоль/л, где
Е калибр.
Е пробы – оптическая плотность опытной пробы,
Е калибр. – оптическая плотность калибровочной пробы,
85,5 – концентрация билирубина в калибраторе, мкмоль/л.
Нормальные значения:
Общий билирубин – 8.5-20.5 мкмоль/л
Прямой билирубин – до 4,0 мкмоль/л
Результат анализа:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




