C NO3- = 10- lgC NO3-
Проверить полученный результат у преподавателя.
По окончании всех действий электрод промыть дистиллированной водой, удалить оставшиеся капли фильтровальной бумагой и закрыть мембрану электрода колпачком.
Лабораторная работа 3
Тема: Потенциометрическое титрование. Определение карбоната натрия в растворе.
Цель работы: Определить с помощью потенциометрического титрования содержание карбоната натрия в исследуемом растворе.
Посуда и принадлежности:
- рН-метр комбинированный стеклянный электрод магнитная мешалка химический стакан, 100 мл, 150 мл мерная колба, 1000 мл мерная пипетка, 10 мл бюретка для титрования, 25 мл
Реактивы:
- соляная кислота 0,1М (фиксанал) деионизированная вода
Выполнение работы:
1. Приготовление 0,1М раствора соляной кислоты
В мерной колбе 1000 мл приготовить раствор 0,1М соляной кислоты из фиксанала.
Приготовленный раствор используется в ходе работы как рабочий раствор для титрования определяемого раствора карбоната натрия.
2. Промыть рабочим раствором бюретку для титрования 2 раза и снова заполнить ее рабочим раствором. Закрепить бюретку на штативе.
3. Подготовка к работе рН-метра.
рН-метр включить в сеть. Электрод погрузить в стакан с деионизированной водой, нажать клавишу включения. В течение 3-5 секунд идет автоматическая настройка рН-метра. Выбрать единицы измерения рН или mV.
При необходимости откалибровать прибор по стандартным буферным растворам.
4. Потенциометрическое титрование исследуемого раствора.
Погрузить в исследуемый раствор магнитную мешалку и стеклянный электрод. Включить магнитную мешалку и тщательно перемешать раствор.
Снять показания рН и mV до начала титрования.
Наконечник бюретки поместить в стакан с исследуемым раствором, не погружая его непосредственно в раствор.
Начать титрование исследуемого раствора 0,1М раствором HCl с шагом 0,5 мл. После добавления каждой порции рабочего раствора снимать показания на шкале рН-метра в единицах рН и mV, переключая во время измерения клавиши рН и mV.
По результатам титрования заполнить таблицу:
VHCl, мл | pH | mV | ΔV, мл | ΔmV | ΔmV/ΔV |
0 | |||||
0,5 | 0,5 | ||||
1,0 | 0,5 | ||||
1,5 и т. д. | 0,5 |
Первое титрование считается грубым. После его проведения необходимо построить график зависимости ΔmV/ΔV - VHCl, мл с целью приблизительного нахождения точки эквивалентности. После этого провести точное титрование, причем вблизи точки эквивалентности - с шагом 0,1-0,2 мл.
Титрование проводить дважды (или трижды) для более точного определения точки эквивалентности.
NB! Перед каждым титрованием электроды необходимо промывать дистиллированной водой.
5. Построение кривых титрования
По полученным усредненным данным титрования в программе EXCEL построить кривые титрования:
а) интегральную кривую в системе координат ось х - VHCl, ось у – рН или mV
б) дифференциальную кривую в системе координат: ось х - VHCl
ось у - ΔmV/ΔV
6. Обработка полученных данных
На интегральной кривой титрования карбоната натрия имеется два скачка потенциала: первый скачок потенциала соответствует количеству в исследуемом растворе гидрокарбоната натрия NaHCO3, второй – количеству карбоната натрия Na2CO3. Поэтому рассчитывать содержание карбоната натрия следует по второму изгибу на кривой титрования или по второму пику на дифференциальной кривой титрования.
По графику определить VHCl, пошедший на титрование карбоната натрия.
Рассчитать массу карбоната натрия в растворе по формуле:
m Na2CO3 = VHCl · ТHCl/ Na2CO3 ,
где ТHCl/ Na2CO3 – титр рабочего раствора по определяемому веществу
ТHCl/ Na2CO3 = 0,001 · Мэкв Na2CO3 · СN HCl
7. Проверить результат у преподавателя
Лабораторная работа 4
Тема. Потенциометрическое титрование. Окислительно-восстановительный метод
Цель работы: Определение содержания пероксида водорода в водных растворах.
Приборы:
· титратор Excellence T50
· окислительно-восстановительный электрод DM140SG
· пластиковый стаканчик для титрования, 100 мл, 3 шт.
· плоскодонная колба для титратора, 250 мл, 3 шт.
· пипетка, 2 мл (2 шт).
· бюретка, 10 мл.
· промывалка.
· лабораторные весы.
· принтер
Реактивы:
- пероксид водорода (анализируемая проба). серная кислота, 20%раствор. перманганат калия, кристаллический. оксалат натрия, кристаллический. дистиллированная вода.
Ход работы:
1. Приготовить 250 мл ≈ 0,1н раствора KMnO4.
Для этого на аналитических весах взвесить приблизительно 0,8 г KMnO4, перенести навеску в мерную колбу на 250 мл и довести до метки дистиллированной водой. Приготовленный раствор поставить в темное место на 1- 2 недели.
2. Установить точную нормальную концентрацию KMnO4 по Na2C2O4.
2 KMnO4 + 5 Na2C2O4 + 8 H2SO4 → K2SO4 + 2 MnSO4 +10 CO2 + 5 Na2SO4 +8 H2O
Для этого:
• Поместить в плоскодонную колбу 120 мл дистиллированной воды.
• Добавить 1,25 мл 20% серной кислоты.
• Нагреть до кипения.
• В горячий раствор внести 25 – 40 мг оксалата натрия Na2C2O4.
• Раствор оттитровать приготовленным раствором KMnO4.
Для определения точной нормальной концентрации раствора KMnO4 необходимо:
• На рабочем столе дисплея выбрать ярлык Titer.
• В поле Number of standarts (количество параллельных проб) ввести цифру 3.
• Установить плоскодонную колбу с горячим раствором в титратор.
• Нажать на клавишу Start → OK
• После завершения титрования в появившемся окне ввести массу внесенного оксалата
натрия с точностью до 0,0001 г. Для подтверждения нажать ОК.
• После появления на дисплее окна с надписью U8000: Add sample x/3 необходимо
сначала установить в титратор колбу со следующей пробой, и только после этого
нажать ОК, тем самым начав новое титрование.
По данной схеме провести титрование оставшихся образцов. Получить результаты в распечатанном виде.
3. Определить процентное содержание перекиси водорода в водном растворе.
2 KMnO4 + 5 H2O2 + 6 H2SO4 → 2 MnO2 ↓ + 5 O2 + 8 H2O
2 MnO4- + 5 H2O2 + 12 H+ = 2 Mn4+ + 5 O2 + 8 H2O
Для этого:
• Налить в стаканчик для титрования 60 мл дистиллированной воды.
• С помощью пипетки добавить в него 0,5 мл раствора пероксида водорода.
• С помощью пипетки добавить туда же 1,25 мл раствора 20% серной кислоты.
• Установить стаканчик в титратор.
• На рабочем столе дисплея зайти в меню H2O2 и выбрать методику 004 Hydrogen
Peroxide Content .
• В поле Number of standarts (количество проб) ввести 3.
4. После результатам трех параллельных титрований рассчитать среднее содержание
пероксида водорода в водном растворе.
5. Результат представить преподавателю.
Работа с титратором:
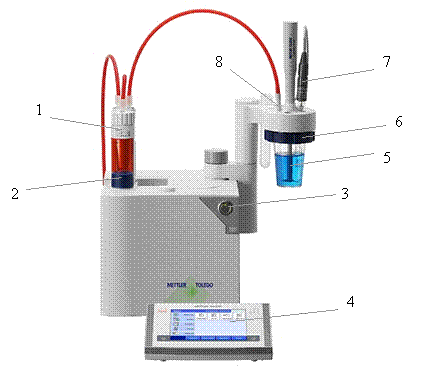 |
Рис. 1. Титратор Excellence T50
Установить бюретку с титрантом 1, для фиксации бюретки использовать синюю ручку 2. Включить титратор, нажав на кнопку 3. Включить компьютер и запустить программу LabX (ярлык программы находится на рабочем столе компьютера). Дождаться появления рабочего меню 4. Через некоторое время после загрузки программы титратора, на дисплее появится сообщение об использованном титранте. Если в сообщении указан титрант, соответствующий проводимому опыту (в данной работе это 1/5 KMnO4), то нажать кнопку OK, если же другой, то – Modify. Поле нажатия на клавишу Modify появится меню Titrant parameter. В поле Name ввести имя титранта, нажав на кнопку, находящуюся справа от поля. Далее нажать на кнопку Proposal и выбрать из списка 1/5 KMnO4. После этого нажать OK. При необходимости изменить концентрацию титранта в поле Concentration и нажать на клавишу Save. Через широкое верхнее отверстие в стенде поместить в стаканчик электрод DM140-SC, предварительно открыв резиновый колпачок на нем 7. Через маленькое отверстие ввести носик бюретки 8. Произвести промывку носика бюретки. Для этого необходимо выбрать на рабочем столе дисплея титратора Dispense. На дисплее появятся параметры Dispense. В поле Titrant - KMnO4. При необходимости уменьшить или увеличить количество мл для промывки. После этого нажать на ОК. По окончании промывания носика бюретки нажать на ОК. Для выхода из меню Dispense нажать на клавишу в виде домика, находящуюся справа или слева от экрана.NB! Если был установлен новый титрант, то перед началом титрования необходимо заполнить бюретку. Для этого необходимо выбрать на рабочем столе дисплея титратора Rinse. На дисплее появятся параметры Rinse. В поле Titrant - KMnO4. При необходимости уменьшить количество циклов. После этого нажать на ОК. По окончании заполнения и промывания бюретки нажать на ОК. Для выхода из меню Rinse нажать на клавишу в виде домика, находящуюся справа или слева от экрана.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
