3. Обработка полученных данных.
По графику определить объем V1NaOH , пошедший на нейтрализацию серной кислоты (первый излом), и объем V2NaOH (второй излом). Разность объемов (V2NaOH - V1NaOH) соответствует объему гидроксида натрия, пошедшему на титрование сульфата меди.
a) Рассчитать массу серной кислоты в исследуемом растворе:
m H2SO4 = V1NaOH · TNaOH/H2SO4
TNaOH/H2SO4 = 0,001· Мэкв H2SO4· СN NaOH ,
где TNaOH/H2SO4 – титр рабочего раствора по определяемому веществу
b) Рассчитать массу сульфата меди в исследуемом растворе:
m CuSO4 = (V2NaOH - V1NaOH) · TNaOH/CuSO4
TNaOH/CuSO4 = 0,001· Мэкв CuSO4· СN NaOH,
где TNaOH/CuSO4 – титр рабочего раствора по определяемому веществу
Полученный результат проверить у преподавателя.
Лабораторная работа 7
Тема: Кондуктометрическое титрование. Определение хлороводородной и уксусной кислот
Цель работы: методом кондуктометрического титрования определить массу HCl и CH3COOH в анализируемом растворе. Провести статистическую оценку полученных результатов.
Теоретическая часть
Кондуктометрия – метод физико-химического анализа, основанный на измерении электропроводности растворов. Она обладает рядом преимуществ перед химическими методами анализа, так как позволяет определять содержание индивидуального вещества в растворе простым измерением электропроводности раствора.
Кондуктометрическое титрование, в отличие от обычного, не требует применения индикаторов и может быть проведено в окрашенных, а также в очень разбавленных растворах. В процессе титрования за ходом реакции следят, измеряя электропроводность титруемого раствора после каждого нового прибавления титранта. Конец титрования совпадает с перегибом на кривой электропроводность – объем добавленного титранта. Изменение электропроводности при кондуктометрическом титровании связано с заменой в растворе по мере протекания реакции одних ионов на другие с иной проводимостью. Кондуктометрическое титрование отличается от обычного также тем, что дает не одну только точку эквивалентности, а полную кривую всего процесса титрования. На ее основе можно составить как представление о ходе реакции, так и о некоторых свойствах получающихся веществ. Например, резкий минимум или явный перегиб на кривой кондуктометрического титрования говорит об устойчивости или малой растворимости продуктов реакции. Размытость области перехода от одного участка кривой к другому указывает (в зависимости от природы реакции) на гидролиз образовавшейся соли, повышенную растворимость осадка или на недостаточную стойкость нового соединения. При соблюдении известных условий кондуктометрически можно определить содержание двух различных соединений, присутствующих в одном и том же растворе.
В данной работе определение основано на последовательном взаимодействии с раствором сильного основания NaOH кислот, отличающихся друг от друга степенью ионизации. В первую очередь с гидроксидом натрия взаимодействует сильная кислота, что вызывает резкое понижение электрической проводимости раствора вследствие связывания высокоподвижных водородных ионов. При титровании слабой кислоты проводимость обычно возрастает, так как вместо слабого электролита образуется хорошо диссоциирующая соль. И наконец, после точки эквивалентности проводимость резко возрастает благодаря появлению в растворе гидроксильных ионов, обладающих высокой подвижностью. Объем щелочи (V1) на кривой титрования соответствует оттитровыванию HCl, объем V2- оттитровыванию суммы HCl и CH3COOH.
Посуда и приборы:
· Кондуктометр S30 SevenEasy
· Кондуктометрический электрод InLab 720 MT
· Пластмассовый химический стакан, 80 мл
· Колба мерная, 50 мл
· Пипетки, 10 мл
· Бюретка, 25 мл
Реактивы:
· Гидроксид натрия, NaOH, 0,1N раствор
· Хлороводородная кислота, HCl, 0,1N раствор
· Уксусная кислота, СН3СООН, 0,1N раствор
· Дистиллированная вода
Выполнение работы:
1. Подготовка к работе кондуктометра.
Включить кондуктометр в сеть, нажать клавишу включения ![]() . В течение 3-5 секунд идет автоматическая настройка кондуктометра. Выбрать измеряемый параметр µS/cm, нажимая клавишу
. В течение 3-5 секунд идет автоматическая настройка кондуктометра. Выбрать измеряемый параметр µS/cm, нажимая клавишу ![]() .
.
При необходимости откалибровать прибор по стандартным буферным растворам (см. руководство пользователя).
2. Анализ смеси соляной и уксусной кислот
Заполнить бюретку для титрования раствором 0,1N NaOH.
Приготовить анализируемую смесь, состоящую из....... мл 0,1N раствора HCl и...... мл 0,1N раствора CH3COOH в соответствии с вариантом.
Пипеткой перенести 10 мл полученного раствора в пластиковый стакан для титрования, добавить дистиллированную воду до отметки 50 мл. Погрузить электрод кондуктометра в раствор и включить магнитную мешалку. Снять показания электропроводности до начала титрования, нажав на клавишу Read/√А.
NB! Перед началом титрования отключить на кондуктометре автостабилизацию показаний, нажав и удерживая клавишу Read/√А – буква А исчезнет.
Начать титрование, приливая раствор NaOH порциями по 0,5 мл. После приливания каждой порции титранта измерять электрическую проводимость раствора. Показания записывать. Титрование прекратить после того, как будут обнаружены два излома на кривой титрования : от резкого падения показаний к плавному, а затем резкому росту значений.
По результатам титрования заполнить таблицу:
Объем раствора 0,1N NaOH, V, мл | æ, µS/сm | ||
0 | |||
0,5 | |||
1,0 |
3. Построение кривой титрования
По полученным данным построить график зависимости y = f(x) в программе EXCEL, где y - электрическая проводимость раствора, х - объем титранта. Из графика найти значения V1 и V2.
V1 и V2 – объемы титранта в первой и второй точках эквивалентности: V1 соответствует нейтрализации HCl, а (V2 –V1) – нейтрализации CH3COOH.
Титрование повторить три раза.
4. Расчет массы HCl и CH3COOH в растворе
Каждый раз на основе графика рассчитать массу HCl и CH3COOH в титруемом растворе по формулам:
mHCl = V1 ·T NaOH / HCl · (VCH3COOH+VHCl) /10 = V1·0.001·MэквHCl·CN NaOH · (VCH3COOH+VHCl) /10
mCH3COOH = (V2 - V1) ·T NaOH / CH3COOH· (VCH3COOH+VHCl) /10 = (V2 - V1) ·0.001·MэквCH3COOH·
CN NaOH · (VCH3COOH+VHCl) /10
5. Расчет действительной массы HCl и CH3COOH в исходном исследуемом растворе .
6. Статиcтическая обработка экспериментальных данных.
Для этого рассчитать:
· Среднее арифметическое значение определяемой величины:
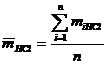
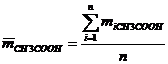
- Отклонение каждого результата от среднего (в %) :
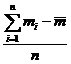 Надежность среднего результата:
Надежность среднего результата: 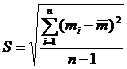
где n – число степеней свободы или число независимых данных, в нашем случае 3.
* Значения ошибок, полученных по упрощенной формуле среднего отклонения ∆ср и по формуле дисперсии среднеквадратичного отклонения S, должны совпадать
- Относительное стандартное отклонение:
σабсол. = mнайдено - mдействит
- Относительную ошибку (отношение абсолютной ошибки к измеряемой величине), в %
σотносит = σабсолют / mдействит
* Относительная ошибка может иметь как положительное, так и отрицательное значение. Ею пользуются чаще, так как она лучше характеризует точность определения.
· Точность определения : 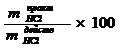 %
% ![]()
Можно ли с вероятностью 95% утверждать, что Ваш полученный результат по массе гидрохлорида водорода и уксусной кислоты в анализируемом растворе составляет: m HCl = ... ±..... г. ; m CH3COOH = ... ±..... г. ?
Варианты выполнения работы 2013 г:
10 мл 0,1M HCl и 10 мл 0,1M CH3COOH 5 мл 0,1M HCl и 10 мл 0,1M CH3COOH 10 мл 0,1M HCl и 5 мл 0,1M CH3COOHЛабораторная работа 8
Тема: Кондуктометрическое титрование. Определение массы карбоната натрия и гидроксида натрия в исследуемом растворе при их совместном присутствии
Цель работы: методом кондуктометрического титрования определить массу гидроксида натрия и карбоната натрия в анализируемом растворе. Провести статистическую оценку полученных результатов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
