Теоретическая часть
Кондуктометрия – метод физико-химического анализа, основанный на измерении электропроводности растворов. Она обладает рядом преимуществ перед химическими методами анализа, так как позволяет определять содержание индивидуального вещества в растворе простым измерением электропроводности раствора.
Кондуктометрическое титрование, в отличие от обычного, не требует применения индикаторов и может быть проведено в окрашенных, а также в очень разбавленных растворах. В процессе титрования за ходом реакции следят, измеряя электропроводность титруемого раствора после каждого нового прибавления титранта. Конец титрования совпадает с перегибом на кривой электропроводность – объем добавленного титранта. Изменение электропроводности при кондуктометрическом титровании связано с заменой в растворе по мере протекания реакции одних ионов на другие с иной проводимостью. Кондуктометрическое титрование отличается от обычного также тем, что дает не одну только точку эквивалентности, а полную кривую всего процесса титрования. На ее основе можно составить как представление о ходе реакции, так и о некоторых свойствах получающихся веществ. Например, резкий минимум или явный перегиб на кривой кондуктометрического титрования говорит об устойчивости или малой растворимости продуктов реакции. Размытость области перехода от одного участка кривой к другому указывает (в зависимости от природы реакции) на гидролиз образовавшейся соли, повышенную растворимость осадка или на недостаточную стойкость нового соединения. При соблюдении известных условий кондуктометрически можно определить содержание двух различных соединений, присутствующих в одном и том же растворе.
В данной работе определение основано на последовательном титровании сильной кислотой (HCl) сильного основания (NaOH) и соли сильного основания и слабой кислоты (Na2CO3). При взаимодействии с HCl сначала реагирует сильное основание NaOH, а затем – Na2CO3.
Na+ + OH - + H+ +Cl - = Na+ + Cl- +H2O
2Na+ + CO3 2- + 2H+ + 2Cl - = 2Na+ + 2Cl - + H2CO3
Кривая титрования смеси соды со щелочью имеет два излома. Объем титранта V1 соответствует нейтрализации NaOH, объем (V2-V1) – нейтрализации Na2CO3. При нейтрализации NaOH электрическая проводимость линейно понижается, так как уменьшается концентрация подвижных ионов ОН-. При взаимодействии кислоты с Na2CO3 электрическая проводимость раствора практически не изменяется, так как при протонировании CO2-3 до H2CO3 вместо 1 моль CO2-3 в раствор вводится 2 моль Cl-. Избыток кислоты после оттитровывания Na2CO3 вызывает резкое увеличение электрической проводимости раствора. Кривая титрования резко идет вверх.
Посуда и приборы:
· Кондуктометр S30 SevenEasy
· Кондуктометрический электрод InLab 720 MT
· Пластмассовый химический стакан, 80 мл
· Пипетка, 10 мл;
· Бюретка, 25 мл.
Реактивы:
· Хлороводородная кислота, HCl, 0,1N раствор
· Гидроксид натрия, NaOH, 0,1N раствор
· Карбонат натрия, Na2CO3, 0,1N раствор
1. Подготовка к работе кондуктометра.
Включить кондуктометр в сеть, нажать клавишу включения ![]() . В течение 3-5 секунд идет автоматическая настройка кондуктометра. Выбрать измеряемый параметр µS/cm, нажимая клавишу
. В течение 3-5 секунд идет автоматическая настройка кондуктометра. Выбрать измеряемый параметр µS/cm, нажимая клавишу ![]() .
.
При необходимости откалибровать прибор по стандартным буферным растворам (см. руководство пользователя).
2. Проведение анализа смеси гидроксида натрия и карбоната натрия
Приготовить анализируемую смесь, состоящую из....... мл 0,1N раствора NaOH и ...... мл 0,1N раствора Na2CO3 в соответствии с вариантом.
Заполнить бюретку для титрования раствором 0,1N HCl. Пипеткой отмерить 10 мл полученного раствора, поместить в пластиковый стаканчик для титрования, довести объем пробы дистиллированной водой до метки 50 мл, погрузить в него электрод. Включить магнитную мешалку, тщательно перемешать раствор.
Провести титрование исследуемого раствора, добавляя из бюретки по 0,5 мл 0,1N раствора HCl и измерять в каждой точке электрическую проводимость. Показания записывать. Снять показания электропроводности до начала титрования, нажав на клавишу Read/√А. Титрование прекратить после обнаружения двух скачков показаний электропроводности.
NB! Перед началом титрования отключить на кондуктометре автостабилизацию показаний, нажав и удерживая клавишу Read/√А – буква А исчезнет.
По результатам титрования заполнить таблицу:
Объем раствора 0,1N HCl, V, мл | æ, µS/сm | ||
0 | |||
0,5 | |||
1,0 |
3. Построение графика
По полученным данным построить график зависимости y = f(x) в программе EXCEL, где y - электрическая проводимость раствора, х - объем титранта. Из графика найти значения V1 и V2.
Титрование повторить три раза. Каждый раз на основе графика рассчитать массу гидроксида натрия и карбоната натрия в титруемом растворе по формулам:
mNaOH = V1 ·THCl / NaOH · (VNaOH+V Na2CO3) /10 = V1·0.001·MэквNaOH·CN HCl · (VNaOH+V Na2CO3) /10
mNa2CO3 = (V2 - V1) ·THCl / Na2CO3 · (VNaOH+V Na2CO3) /10 = (V2 - V1) ·0.001·MэквNa2CO3·
CN HCl·(VNaOH+V Na2CO3) /10
4. Расчет действительной массы NaOH и Na2CO3 в исходном исследуемом растворе.
4. Статистическая обработка экспериментальных данных.
Для этого рассчитать:
- Среднее арифметическое значение определяемой величины:
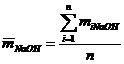
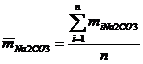
- Отклонение каждого результата от среднего (в %) :
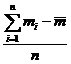 Надежность среднего результата:
Надежность среднего результата: 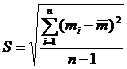
где n – число степеней свободы или число независимых данных, в нашем случае 3.
* Значения ошибок, полученных по упрощенной формуле среднего отклонения ∆ср и по формуле дисперсии среднеквадратичного отклонения S, должны совпадать
- Относительное стандартное отклонение:
σабсол. = mнайдено - mдействит
- Относительную ошибку (отношение абсолютной ошибки к измеряемой величине), в %
σотносит = σабсолют / mдействит
* Относительная ошибка может иметь как положительное, так и отрицательное значение. Ею пользуются чаще, так как она лучше характеризует точность определения.
9. Точность определения : ![]() %
%
Можно ли с вероятностью 95% утверждать, что Ваш полученный результат по массе гидроксида натрия и карбоната натрия в анализируемом растворе составляет: mNaOH = ... ±..... г. ; mNa2СO3 = ... ±..... г. ?
Варианты выполнения работы 2013 г:
1. 10 мл 0,1N NaOH и 10 мл 0,1N Na2CO3
2. 5 мл 0,1N NaOH и 10 мл 0,1N Na2CO3
3. 10 мл 0,1N NaOH и 5 мл 0,1N Na2CO3
Лабораторная работа 9
Тема. Спектрофотометрия.
Цель работы: Определение содержания меди в растворе с помощью спектрофотометра
Посуда и приборы:
· спектрофотометр Helios Gamma
· кювета (стеклянная – G), 10 мм
· мерная колба, 50 мл (6 шт.), 1000 мл (1 шт.)
· чашка Петри, 45 мл
· аналитические весы, с точностью 0,0001
· воронка, 90 мм, 45 мм
· бюретка, 25 мл
· промывалка
· пипетка, 10 мл
· компьютер с программным обеспечением для спектрофотометра Helios Gamma - VISIONlite
· принтер ОКI
· бумага
Реактивы:
· сульфат меди CuSO4∙5H2O
· серная кислота концентрированная (ρ=1,84 г/см3)
· раствор аммиака концентрированный
· дистиллированная вода.
Ход работы:
1. Приготовление исходного раствора для построения калибровочного графика
Приготовить 1 л раствора сульфата меди (из расчета 1 мг меди в 1 мл раствора). Для этого взять точную навеску 3,9270 г CuSO4∙5H2O и количественно перенести ее в мерную колбу вместимостью 1000 мл. Растворить навеску в небольшом количестве воды, подкислить раствор 5 мл концентрированной серной кислоты, разбавить водой до метки, тщательно перемешать.
Полученный раствор использовать для приготовления серии стандартных растворов.
2. Приготовление стандартных растворов меди
Из исходного раствора приготовить серию стандартных растворов. Для этого в мерные колбы (от 1 до 6) вместимостью 50 мл внести 25, 20, 15, 10, 5, 3 мл исходного раствора, используя бюретку. В каждую мерную колбу добавить по 3 мл концентрированного раствора аммиака. Растворы долить дистиллированной водой до метки. Тщательно перемешать, выдержать перед определением в течение 15-20 минут.
3. Выбор светофильтра (см. Работа со спектрофотометром, Определение максимального светопоглощения)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
