Вопросы раздела
1. Биохимические функции мышечной ткани
2. Мышечное волокно.. Структурные компоненты мышечного волокна
3. Химический состав мышечной ткани
4. Белковые вещества мышечной ткани: миофибриллярные, саркоплазматические, сарколеммы (стромы)
5. Миофибриллярные белки
· Миозин. Строение молекулы миозина. Активация миозина
· Строение молекулы актина.
· Взаимодействие миозина с другими белками и АТФ. Роль актина и миозина.
· Тропонин и тропомиозиновый комплекс
6. Саркоплазматический белок миоглобин
7. Сокращение и расслабление мышечных волокон. Биохимические механизмы этих процессов.
· Типы мышечных клеток и их энергообеспечение.
· Структура миофибриллы
· Сокращение саркомера, тонкие и толстые филаменты
· Преобразование энергии гидролиза АТФ в механическую работу актиновых филаментов
· Регуляция сокращения произвольных поперечно-полосатых мышц. Роль кальция в этом процессе
· Регуляция сокращения гладкой мышцы. Роль кальция в этом процессе
8. Мышечное окоченение
9. Ферменты мышечной ткани. Изменение активности ферментов
10. Небелковые компоненты.
· Липиды.
· Углеводы. Скорость окислительных превращений углеводов в мышцах
· Мышечный гликоген. Превращения гликогена
· Превращения нуклеотидов
· Протеолитические превращения
· Обмен свободных аминокислот
11. Азотистые экстрактивные вещества
· Карнозин (b-аланилгистидин), ансерин
· Карнитин
· Холин
· Глютатион (глютаминилцистеилглицин)
12. Креатин. Перенос энергии с креатинфосфата (КрФ) на АДФ. Биохимические изменения при мышечных дистрофиях. Креатинурия. Роль витамина Е.
Таблица 35.Биохимия мышечной ткани.
Задание | Указания к выполнению задания |
Изучите химический состав мышц. | 1. Выпишите основные группы веществ, входящих в состав мышечной ткани: а), б), в), г). 2. Дайте классификацию и общую характеристику мышечных белков: а), б), в). 3. Охарактерезуйте белки миофибрилл: а) миозин, б) актин, в) актомиозин, г) тропомиозин, д) тропонин. 4. Охарактеризуйте саркоплазматические белки, мышечные глобулины. Напишите структуру простетической части миоглобина. Какое значение имеет более высокое средство миоглобина и кислороду чем у гемоглобина. 5. Выпишите основные небелковые (экстрактивные) вещества мышечной ткани. |
Изучите биохимический механизм мышечного сокращения и расслабления. | 1. Охарактеризуйте роль ионов кальция в процессе сокращения и расслабления мышц. Каковы механизмы его аккумуляции в саркоплазматическом ретикулуме и роль в этом процессе Са2+- насоса. 2. Охарактеризуйте роль градиента одновалентных катионов в регуляции мышечного сокращения. 3. Схематически представьте этапы мышечного сокращения. 4. Расслабление мышц. Фактор расслабления. 5. Дайте понятие химических механизмов, лежащих в основе мышечного утомления. |
Изучите особенности энергетического обмена в мышцах.. | 1. Охарактеризуйте роль аэробного дихотомического окисления углеводов и окисления кетоновых тел в обеспечении метаболизма в покоящейся мышце. 2. Охарактеризуйте роль гликолиза в энергообеспечении интенсивно работающей мышцы. 3. Охарактеризуйте механизмы быстрой регенерации АТФ для работающей мышцы: а), б). 4. Напишите схему синтеза креатина, креатинфосфата, образования креатинина и выведения его из организма. |
СПИСОК ЛИТЕРАТУРЫ
Основная литература:
1. Биохимия: учебник для студентов мед. вузов /под редакцией .- 4-е издание исправленное.-М. :ГЭОТАР-Медиа, 2013.- 768 с.
2. Биохимия. Краткий курс с упражнениями и задачами: учебное пособие/под редакцией , .-М.:ГЭОТАР-МЕД, 2013.-624с.
3. , . Биологическая химия: Учебник.-М.:Медицина.-2004.-704с.
Дополнительная литература:
1. Биохимические основы патологических процессов: учебное пособие/ под редакцией .-М.: Медицина, 2009.- 304с.
2. Наглядная медицинская биохимия: Учебное пособие: / Дж. Г. Солвей; пер. с английского под ред. .- М.: ГЭОТАР-МЕД, 2011.-136с.
3. Клиническая биохимия: учебное пособие/ под редакцией .- 3-е издание.- М.: ГЭОТАР-Медиа, 2012.-203с.
4. Введение в биомембранологию / Под ред. .- М.: Изд–во МГУ, 2011.-213с.
5.Витамины: Учебное пособие / Под ред. .- Оренбург: -сервис».- 2014.-54с.
6., Мрочек . Учеб. пособие. – Минск: Книжный Дом, 2009. - 608с.
7.Камышников -биохимическая лабораторная диагностика: Справочник: В 2 т. – Минск: Интерпресссервис, 2013.
8.Клиническая биохимия: учебное пособие / Под ред. .- М.:ГЭОТАР-Медиа, 2009.- 264 с.
9. -Г. Наглядная биохимия.- М.: Мир, 2014. - 469 с.
10. ж. Клиническая биохимия.- М.-Спб: Изд-во «БИНОМ», 2011.-213с.
Список интернет-ресурсов
1. http://biokhimija. ru (лекции и видеоматериал)
2. http://vmede. org
3. http://www. biochemistry. ru/
4. http://www. med-edu. ru/basic-science/biohim/ (видео-лекции)
Приложение А
БИОХИМИЧЕСКИЕ МЕХАНИЗМЫ ТОКСИЧНОСТИ.
Токсикант - вещество любой химической природы, способное нарушить гомеостаз биологической системы и оказать на нее вредное влияние при взаимодействии, вызывая повреждение или гибель. Формирование токсического эффекта включает 4 стадии (рисунок 3):
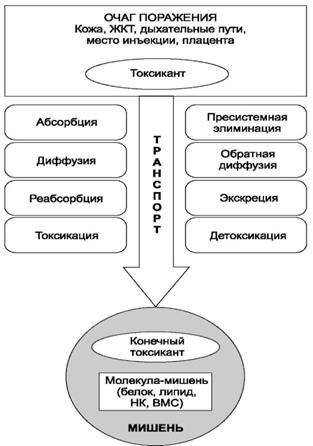
Рисунок 3. Стадии формирования токсического эффекта. НК-нуклеиновые кислоты, ВМС-высокомолекулярные биомолекулы любой природы.
Этап 1.Доставка токсиканта к мишеням. Na+, К+-АТФаза, потенциалзависимые кальциевые каналы, связывание с промежуточным переносчиком, эндоцитоз и рециркуляция мембраны облегчают транспорт токсикантов в определенные клетки - клетки-мишени.
Накопление токсиканта в лизосомах происходит благодаря pH-ловушке. Митохондриальное накопление происходит вследствие электрофореза. Некоторые вещества, например органические и неорганические катионы, полициклические ароматические углеводороды, накапливаются в меланинсодержащих клетках за счет связывания с меланином. Прочное связывание с белками плазмы пролонгирует эффекты и задерживает элиминацию токсикантов. Существуют также специализированные барьеры для токсикантов в клетках мозга, сперматогенных клетках, в плаценте.
Экскреция - удаление ксенобиотиков из крови и выделение во внешнюю среду. Это - физический процесс, в то время как биотрансформация - химический механизм удаления токсиканта. Путь и скорость экскреции в значительной степени зависят от физико-химических свойств токсиканта. Для высоколипофильных соединений не существует эффективных механизмов элиминации. Для элиминации таких соединений существуют три неэффективных механизма: экскреция с грудным молоком, выделение с желчью и в просвет кишечника из крови. Летучие соединения, такие как газы и летучие жидкости, диффундируют из легочных капилляров в альвеолы и удаляются при выдохе.
Токсиканты, попавшие в почечные канальцы, могут проникать обратно через клетки стенок канальцев в околоканальцевые капилляры. Реабсорбция путем диффузии зависит от липофильности и обратно пропорциональна степени ионизации.
Токсиканты, попавшие в желудочно-кишечный тракт с желчью, желудочным и кишечным соком, слюной, секретом поджелудочной железы, могут реабсорбироваться путем диффузии через слизистую оболочку. Реабсорбция соединений, выделенных в желчь, возможна, если они достаточно липофильны или превращены в более жирорастворимые формы в просвете кишечника.
Биотрансформация токсикантов в более ядовитые продукты называется токсикацией, или метаболической активацией. Значительно чаще токсикация изменяет эндо - и ксенобиотики так, что они приобретают способность взаимодействовать с функциональными группами молекул различных эндогенных соединений и превращать их в электрофилы; свободные радикалы (химические агенты с неспаренными электронами и высокой активностью, такие как супероксид-анион радикал О2-, гидроксил-радикал НО); нуклеофилы; редокс-активные частицы.
Этап 2 - взаимодействие конечного токсиканта с молекулой-мишенью
Нековалентное связывание - образование водородных и ионных связей типичны для токсикантов, взаимодействующих с мембранными и внутриклеточными рецепторами, ионными каналами и некоторыми ферментами.
Образование ковалентного аддукта характерно для электрофильных токсикантов, реагирующих с нуклеофильными атомами в биологических макромолекулах (белках и нуклеиновых кислотах). Свободные радикалы типа HO, NO2• и C13C• могут ковалентно связываться с макромолекулами или отщеплять атомы водорода от эндогенных соединений, превращая их в радикалы. В результате этих превращений часто образуются карбонильные соединения, формирующие поперечные сшивки с ДНК или белками. Химические агенты способны участвовать в реакциях окисления-восстановления, образуя токсичные продукты. Например, окисление токсикантами Fe(II) до Fe(III) в гемоглобине вызывает метгемоглобинемию.
Некоторые токсиканты активируют молекулы-мишени. Однако чаще химические агенты ингибируют функции молекул-мишеней, блокируя рецепторы, ионные каналы или ферменты.
Токсиканты могут нарушать матричную функцию ДНК. Ковалентное связывание химических агентов с ДНК (образование аддуктов) вызывает ошибки при репликации. Кроме образования аддуктов, токсиканты изменяют первичную структуру эндогенных молекул поперечным сшиванием или фрагментацией.
Этап 3 - клеточная дисфункция и последствия токсичности
Если молекула-мишень участвует в клеточной регуляции (передаче сигналов), прежде всего происходит дисрегуляция экспрессии генов и/или дисрегуляция выполняемой клеткой функции. Однако если молекула-мишень вовлечена в процессы клеточного жизнеобеспечения, ее повреждение может привести к гибели клетки.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 |



