МАТЕРИАЛЫ ДЛЯ ПОДГОТОВКИ К ПРАКТИЧЕСКИМ ЗАНЯТИЯМ ПО БИОХИМИИ ДЛЯ МЕДИКО_ПРОФИЛАКТИЧЕСКОГО ФАКУЛЬТЕТА
ПРЕДИСЛОВИЕ
Студентам рекомендуется вести запись в отдельной тетради для выполнения заданий при самостоятельной подготовке к предстоящему практическому занятию. В ходе подготовки к занятию выполните в тетради задания из таблицы. Задания необходимо выполнять, пользуясь учебниками, конспектами лекций, видеоматериалами (список приводится в разделе Список литературы).
В ходе изучения материала соответствующей темы необходимо:
1. Внимательно ознакомиться с формулировками домашних заданий.
2. Изучить необходимый материал, касающийся темы предстоящего практического занятия по учебнику и конспектам лекций, а в случае необходимости получить более широкие и глубокие знания – по дополнительным источникам.
3. Воспроизвести в тетради для самоподготовки требуемые формулы, схемы биохимических процессов, графики и др.
4. Понять взаимосвязь изученных процессов, а также их биологическое и физиологическое значение.
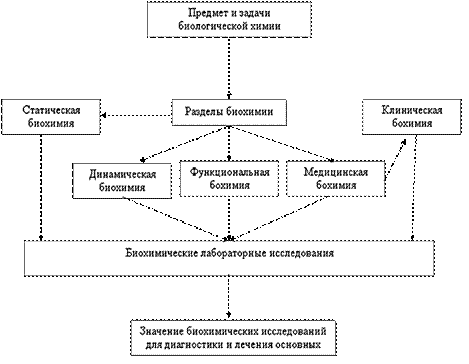
Рисунок 1. Разделы биологической химии
СОДЕРЖАНИЕ
Предисловие…………………………………………………………………………….1
Раздел 1. Белки.…..………………………………………………………………….
1.1.Структура и свойства белков. Методы выделения и очистки белков………………………………………………………………………… 3
Раздел 2. Ферменты……………………………………………………………………8
2.1.Ферменты: общие свойства и механизм действия. Энзимопатии………………………………………………………………………………………………8……...
2.2.Регуляция активности ферментов. Ферменты в медицинской практике…………………………………………………………………………………………10
Раздел 3. Биологические мембраны. Биохимия питания. Общие пути катаболизма. Биоэнергетика………………………...12
3.1. Биологические мембраны……………………………………………………………………12
3.2.Введение в обмен веществ и энергии. Роль витаминов………………………………………14
3.3. Биологическое окисление. Цикл трикарбоновых кислот-общий путь метаболизма. Строение дыхательной цeпи……………………………………………………………17
3.4. Тканевое дыхание. Окислительное фосфорилирование и транспортные системы митохондрий……………………………………………………………………………18
Раздел 4. Взаимосвязь и регуляция обмена веществ. Гормоны……………….……21
4.1.Биохимия гормонов. Молекулярные механизмы передачи гормонального сигнала…………………………………………………………………………………………
4.2.Гормоны белковой природы и производные аминокислот………………………………………………………………………………………23
4.3. Стероидные гормоны………………………………………………..………………25
Раздел 5.Обмен белков и аминокислот…………………………………………………27
5.1. Переваривание белков. Пути использование аминокислот в клетке……………27
5.2. Общие пути катаболизма аминокислот. Специфические пути обмена аминокислот. Обезвреживание и выведение аммиака…………………………………………29
Раздел 6. Обмен нуклеотидов. Матричные синтезы ДНК, РНК, белка ………………………31
6.1. Обмен нуклепротеидов: пищеварение и всасывание. Синтез и распад пуриновых и пиридиновых мононуклеотидов……………………………………………………32
6.2. Молекулярные механизмы биосинтеза нуклеиновых кислот……………………34
6.3.Биосинтез белка. Фолдинг белка. Ингибиторы матричных биосинтезов…………34
Раздел 7.Структура и обмен углеводов………………………………………………35
7.1. Обмен углеводов: поступление, переваривание и всасывание. Синтез и распад гликогена………………………………………………………………………………………35
7.2. Аэробный и анаэробный катаболизм глюкозы. Глюконеогенез. Обмен галактозы и фруктозы. Пентозофосфатный путь………………………………………………………38
Раздел 8.Структура и обмен липидов………………………………………………41
8.1. Липиды: переваривание и всасывание……………………………………
8.2. Катаболизм эндогенных липидов. Окисление глицеридов и жирных кислот…………………………………………………………………………………………42
8.3. Анаболизм липидов. Биосинтез жирных кислот. Обмен холестерола. Синтез кетоновых тел…………………………………………………………44
8.4.Взаимосвязь обменных процессов. Патохимия сахарного диабета.…………………………………………………………………………………………46
Раздел 9. Биохимия органов и тканей………..47
9.1.Регуляция водно-солевого обмена. Биохимия почек. Общий анализ мочи…………………………………........................................................................................49
9.2. Биохимия крови. Белки плазмы крови. Гемостаз…………………………………………….53
9.3. Печень- центральный орган в метаболизме белков, жиров и углеводов. Микросомальное окислние………………………………………53
9.4.Биохимия печени. Синтез и распад хромопротеидов в печени………55
9.5. Биохимия соединительной ткани и ткани кости…………………........................56.
9.6. Биохимия нервной ткани…………………................................................................59
9.7. Биохимия мышечной ткани…………………........................................................63.
Список литературы………………………………………………64
Приложение «Биохимия токсических состояний»……………………………………65
.
РАЗДЕЛ 1. Белки.
1.1. Структура и свойства белков. Методы выделения и очистки белков
Белки (протеины) – высокомолекулярные азотсодержащие органические соединения, играют важную роль в построении живой ткани и в осуществлении процессов жизнедеятельности. Особенности структуры и наличие ряда уникальных свойств обеспечивают функционирование белков как одного из основных материальных носителей жизни. Представление о структуре, физико-химических свойствах и биологических функциях белков являются теоретической основой изучения всех последующих разделов биологической химии.
Вопросы раздела.
1. Белки. Определение. Биологическая роль. Классификация по структуре, по форме молекул, по физико-химическим свойствам.
2. Аминокислоты как структурные компоненты белковых молекул. Особенности структуры аминокислот. Классификации аминокислот (по структуре радикалов, по биологической значимости). Физико-химические свойства. Цветные реакции на α-аминокислоты, практическое применение.
3. Уровни организации белковой молекулы. Первичная структура белков. Пептидная связь, ее характеристика. Принцип формирования пептидной связи. Биуретовая реакция – универсальная реакция на пептидную связь, практическая значимость. Гидролиз белка (кислотный, щелочной, ферментативный)
4. Вторичная, третичная, четвертичная структуры белков. Связи, стабилизирующие высшие уровни организации белковой молекулы. Супервторичная структура белка:примеры. Доменная структура. Биологическое значение уровней организации белковой молекулы.
5. Физико-химические свойства белков в связи со структурными особенностями. Факторы стабилизации белковых растворов (структурная организация, наличие заряда, наличие гидратной оболочки). Способы осаждения белков (обратимые – высаливание, изоэлектрическое осаждение; необратимые - денатурация). Практическое применение.
6. Методы очистки белков от низкомолекулярных примесей (диализ, ультрафильтрация). Принципы, практическое применение.
7. Хроматографические методы разделения белков (гель-хроматография, ионообменная хроматография, аффинная хроматография). Принципы методов. Практическое применение.
8. Принцип метода количественного определения белка в сыворотке крови, величина нормы, диагностическое значение. Возрастные особенности нормальных величин белков сыворотки крови.
9. Электрофорез белков сыворотки крови. Принцип метода, диагностическое значение. Особенности протеинограммы в детском возрасте.
Таблица 1.Структура и свойства белков.
Задание | Указания к выполнению задания | ||||||||||||||||||||||||||||||||||||
Вспомните структуру и свойства аминокислот, аминокислотный состав белков. | 1.Напишите общую формулу протеиногенных α-аминокислот. Как классифицируются альфа-аминокислоты по строению бокового радикала? В виде каких частиц находятся α-аминокислоты в водных растворах при нейтральном значении рН? Напишите формулы трипептидов: а) пролил-глицил-аланин; б) лизил-фенилаланил-серин. Выделите пептидные связи. Вспомните функциональное многообразие белков – белки ферменты, белки-рецепторы, транспортные белки, антитела. 3.Перечислите группы простых белков, охарактеризуйте их биологическую роль. 4. Перечислите группы сложных белков (хромопротеиды, липопротеины, фосфопротеины), охарактеризуйте их биологическую роль, охарактеризуйте функции небелковой части (лиганда).
| ||||||||||||||||||||||||||||||||||||
1.Изучите уровни организации белковой молекулы. | 1.Дайте определение первичной структуры белка. Какая основная связь стабилизирует первичную структуру? Дайте определение конформации и нативной конформации полипептидной цепи. Дайте определение понятию «конформационная лабильность белков», ее значение. Дайте определение вторичной структуры. Какие формы вторичной структуры встречаются в природных белках? За счет каких связей стабилизируются конформации α-спирали? Аминокислотные радикалы каких α-аминокислот способствуют образованию α-спирали? Для какой формы вторичной структуры полипептидной цепи характерны межцепочечные водородные связи? Дайте определение понятия «третичная структура» полипептидной цепи. Какие связи обеспечивают стабильность третичной структуры полипептидной цепи? Между какими группами может возникнуть гидрофобное взаимодействие? Между аминокислотными остатками каких α-аминокислот возникает дисульфидная связь? Как располагаются полярные радикалы аминокислотных остатков при формировании третичной структуры полипептидной цепи в водной среде? Каковы основные факторы, определяющие трехмерную структуру белка? Дайте определение глобулярных и фибриллярных белков. Какие белки называют гомологичными? Каков характер взаимосвязи между уровнями организации белковой молекулы и ее биологической активностью? Дайте понятие:активный центр белка, комплементарность связывания с лигандом. Дайте определение доменной структуры. Какова её роль в функционировании белков. Приведите примеры. Дайте определение четвертичной структуре белка. Какие связи стабилизируют четвертичную структуру белка? Что такое протомеры белковой молекулы? Дайте понятие активного и аллостерического центра белка. | ||||||||||||||||||||||||||||||||||||
2.Изучите методы исследования первичной структуры белка. | 1. Какие методы гидролиза белка Вы знаете? Обратите внимание на то, что при установлении аминокислотной последовательности проводится кислотный, а не основный гидролиз белка, так как в щелочной среде происходит разрушение некоторых аминокислот. 2. В чем суть хроматографического анализа? Приведите классификацию хроматографических методов. 3. Приведите примерную последовательность операций при установлении первичной структуры белка. 4. Продумайте, какое практическое значение для медицины имеют исследование аминокислотного состава и первичной структуры белков. 5.Перечислите методы, позволяющие изучить вторичную, третичную и четвертичную структуру белка. | ||||||||||||||||||||||||||||||||||||
4. Методы определения белка | 1.Сформулируйте принцип количественного определения белка биуретовым методом. Напишите реакцию. 2.Выпишите границы содержания белка в сыворотке крови в физиологичеких условиях и приведите примеры заболеваний, сопровождающихся гипо - и гиперпротеинемией. |
Таблица 2 .Физико-химические свойства белков.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 |



