Активация рецептора может привести к изменению экспрессии гена и/или химической модификации определенных белков (обычно путем фосфорилирования). Дисрегуляция генной экспрессии происходит при воздействии на структуры, принимающие участие в транскрипции, передаче сигналов, синтезе, хранении или выделении экстрацеллюлярных сигнальных веществ.
Транскрипция, представляющая собой передачу генетической информации от ДНК к мРНК, управляется взаимодействием факторов транскрипции (TFs) и промоторных участков гена. Биогенный или чужеродный лиганд может оказывать токсический эффект в двух случаях - при воздействии в больших дозах и/или в определенные периоды онтогенеза. Другие вещества, взаимодействующие с TFs, могут нарушать дифференцировку клеток за счет усиления экспрессии различных генов.
Экстрацеллюлярные сигнальные молекулы (факторы роста, цитокины, гормоны и нейротрансмиттеры) могут в конечном счете активировать TFs, воздействуя на мембранные рецепторы и/или внутриклеточную систему передачи сигнала. Химические агенты могут нарушать (прекращать или извращать) передачу сигнала путем повреждения структур, участвующих в фосфорилировании (например, G-белков), и в конечном счете влиять на клеточный цикл. Kсенобиотики, облегчающие фосфорилирование элементов цепи передачи сигнала, часто провоцируют усиление клеточного деления и формирование опухоли.
Существуют 3 механизма инициирования клеточной смерти - истощение запасов AТФ, устойчивое повышение концентрации ионов кальция и избыточная продукция AФK.
ATФ играет центральную роль в жизнеобеспечении клетки, используется и как субстрат для биосинтеза, и как главный источник энергии. Многие токсиканты нарушают окислительное фосфорилирование (таблица 35). Вещества класса A вмешиваются в процесс транспорта ионов водорода по цепи передачи электронов. Вещества класса Б блокируют передачу электронов к атомам кислорода. Kласс В - ингибиторы транспорта кислорода к последнему в цепи переносчику электронов - цитохромоксидазе. Класс Г - ингибиторы AТФ-синтетазы, ключевого фермента окислительного фосфорилирования. Синтез ATФ может ингибироваться в случае прямого ингибирования AТФ-синтетазы, нарушения доставки неорганического фосфата AДФ, прекращения потока протонов. Класс Д - вещества, разрушающие митохондриальную ДНK.
Плазменная мембрана непроницаема для ионов кальция. Токсиканты увеличивают уровень цитоплазматического кальция путем усиления потока кальция внутрь клетки и/или ослабления потока из клетки. Повышенное содержание кальция оказывает токсическое действие на клетку - проявляющееся истощением энергетических запасов (ингибирование AТФазы), дисфункцией микрофиламентов и микронитей (цитоскелет), активацией гидролитических ферментов и генерацией AФK. AФK также могут истощать запасы AТФ. NO+ - катион нитрония (производное NO') инактивирует глицеральдегид-3-фосфатдегидрогеназу, ухудшает гликолиз, необратимо ингибирует часть компонентов цепи переноса электронов. Kроме того, ONOO - может стимулировать одиночные разрывы цепей ДНК и др. Приток ионов кальция в митохондрию снижает абсолютное значение мембранного потенциала митохондрий, вызывает генерацию AФK, разобщение метаболических процессов, регресс синтеза AТФ.
Чаще всего процесс гибели клетки под действием токсикантов связан с деградацией митохондрий. Другой путь - выход в цитоплазму цитохрома с (cyt c), гемсодержащего белка, который обычно находится на поверхности внутренней мембраны в митохондриальном межмембранном пространстве. Суt с - последний компонент ЦПЭ, его отсутствие полностью блокирует синтез AТФ. Происходит увеличение содержания О2 - и начинается процесс некроза. Одновременно свободный cyt с является запускающим фактором апоптоза.
Mногие ксенобиотики могут вызывать и апоптоз, и некроз. Aпоптоз обычно индуцируется при воздействии низких концентраций токсикантов, при высоких концентрациях развивается некроз.
Этап 4 - восстановление или повреждение
После химического повреждения ДНK и перекисного окисления жиров клетка гидролитически удаляет поврежденную часть.
Окисленные тиольные группы белков восстанавливаются энзиматически при каталитическом участии тиоредоксина и глутаредоксина.
Восстановление окисленного гемоглобина осуществляется путем передачи электронов с цитохрома b5, последний регенерируется при участии НAДН-зависимой цитохром b5-редуктазы. Mолекулы шаперонов (например, белки теплового шока) активно синтезируются в ответ на денатурацию белков. Они восстанавливают структуру поврежденных белков. Последние также уничтожаются протеолизом. AТФ/убихинон-зависимые протеолитические системы контролируют уровень регуляторных белков (например, р53, IkB, циклинов), которые элиминируют поврежденные внутриклеточные белки.
Окисленные жиры восстанавливаются в ходе сложного процесса, включающего ферменты класса редуктаз, глутатионпероксидазу и глутатионредуктазу. Для регенерации редуктаз необходим НAДФН.
В тканях, способных к регенерации, дефекты устраняются некрозом или апоптозом и пролиферацией. При восстановлении поврежденных тканей происходят регенерация клеток и компонентов внеклеточного матрикса, а также реинтеграция новых клеток в ткани и органы.
Химические канцерогены нарушают процессы репарации ДНК, апоптоза и терминации клеточной пролиферации. Химические агенты, действующие на ДНК, вызывают образование аддуктов, оксиление, сшивки цепей. Наиболее неблагоприятная ситуация - экспрессия поврежденными генами белков-регуляторов клеточного деления. Такие клетки способны к сверхнормальному росту и вытесняют здоровые структуры. Результатом является образование опухоли.
Таблица 35. Химические агенты, нарушающие процесс синтеза AТФ
Влияние на процесс синтеза АТФ | Химические агенты |
А. Ингибиторы процессов транспорта протонов на ЦПЭ | Арсениты, дихлорвинилцистеин, п-бензохинон, 4-пентаеновая ксилота, фторацетат, малонат, этанол, пентахлорбутадиенилцистеин, пероксид водорода |
Б. Ингибиторы транспорта электронов по ЦПЭ | Амитад, цианиды, сероводород, азиды, формиаты, NO+, фосфин, паракват, миксотиазол, динитроацилиновые и дифенилэфирные гербициды, CCl4, доксорубицин |
В. Ингибиторы транспорта кислорода по ЦПЭ | Депрессанты, ковульсанты, алкалоиды спорыньи, кокаин, угарный газ, метгемоглобинобразователи |
Г. Ингибиторы фосфорилирования АДФ | ДДТ, свободные жирные кислоты, амиодарон, валиномицин, грамицидин, кальцимици, салицилаты, тиодиазольные гербициды |
Д. Химические агенты, повреждающие митохондириальную ДНК и нарушающие процесс транскрипции | Противовирусные препараты, этанол (при хроническом отравлении) |
П р и м е ч а н и е. ЦПЭ - цепь переноса электронов.
Рецепторы токсинов.
Теоретически все известные к настоящему времени химические вещества потенциально могут нанести вред организму. Существуют различные классификации рецепторов(таблица 36).
Таблица 36. Локализация рецепторов и механизм действия
Лиганды | Локализация рецепторов | Регуляция числа рецепторов | Механизм функционирования |
Белково-пептидные гормоны, биогенные амины, ацетилхолин, бензодиазепины, имипрамин, опиаты, стероидные гормоны, прстагландины | Плазматическая мембрана | «Регуляция снизу» выявлена во всех случаях (интернализация) | Индукция образования или ингибирование образования цАМФ или цГМФ. Изменение проницаемости для ионов К+, Cl-, Na+ или Са2+. Изменение обмена фосфолипидов. |
Липопротеины низкой плотности, гликопротеины, фибрин, кобаламин | Плазматическая мембрана | Зависимость связывающей способности от концентрации двухвалентных ионов | Интернализация лиганда в клетку |
Стероидные гормоны всех классов | Цитозоль | Ядерная транслокация. Изменение транскрипции генома | |
Тиреоидные гормоны | Ядро | Изменение транскрипции генома |
Рецептор токсичности - это химически активная группировка, в норме участвующая в метаболизме клетки, к которой способна присоединиться молекула ксенобиотика. Например, химическими рецепторами для соединений мышьяка (III) и ртути (II) служат тиоловые (сульфгидрильные) группы (-SН).
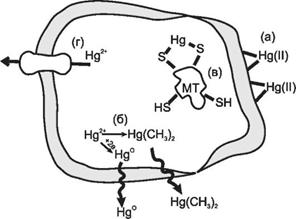
Рисунок 4. Механизмы взаимодействия соединений металлов с клеткой. a - связывание с мембраной; б - восстановление и/или метилирование с образованием летучих соединений; в - комплексообразование с металлотионеином (МТ); г - выведение ионов через ионные каналы.
Специфические и неспецифические рецепторы - мишени токсичности - могут быть локализованы в области клеточной мембраны (активные центры G-белков, ионные каналы, мембранные переносчики, ферменты, белки, липиды), во внутриклеточном пространстве (цитоплазматические, митохондриальные, ядерные рецепторы) или вне клетки (любые химические структуры, вступающие во взаимодействие с токсикантом).
Специфические метаболические (биохимические, токсикокинетические) противоядия способны изменять механизмы метаболических процессов с участием токсичных веществ. Например, при отравлении метгемоглобинобразователями, в том числе цианидами, применяют метиленовый синий - тетраметилтионина хлорид, который в крови способен окислять железо (II) гемоглобина, т. е. превращать его в метгемоглобин. Попавшие в кровь цианиды образуют более прочные связи с метгемоглобином, покидая менее прочные центры связывания - геминовые структуры тканей. Происходит восстановление функции цитохромоксидаз тканей. Комплекс МеtHbCN - постепенно отщепляет цианид в печени и метаболизируется до безопасных продуктов. Связывание цианида можно усилить введением специфического химического антидота - натрия тиосульфата:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 |



