Во всех случаях при достижении достаточно высокого анодного потенциала на поляризационных кривых наблюдаются участки предельных диффузионных токов. Величины предельных токов и значения потенциалов, при которых наблюдается переход в область диффузионного контроля, определяются как природой металла, так и составом электролита. Величины предельных токов возрастают при увеличении скорости вращения дискового электрода (рис. 1). Подобного рода зависимости имеют место как в растворах электрополирования, так и в системах, где имеет место химическое полирование при отсутствии внешнего тока.
|
|
Рис. 1. Зависимость предельной анодной плотности тока для: а – циркония в водно-спиртовом растворе состава 1 М NaCl + 6 М ИПС; б – вольфрама в электролитах, содержащих 1 М NaCl и различное количество МЭА (моль/л):
1 – 1; 2 – 6; 3 – 8 от квадратного корня из скорости вращения электрода скорости вращения электрода. Т=298К.
Хроноамперометрические измерения при потенциостатическом анодном растворении никеля и циркония в водно-изопропанольных хлоридсодержащих растворах также свидетельствуют об ограничении скорости исследуемой реакции диффузионными процессами; это следует из линейного характера зависимостей jа – ф-1/2. Значения эффективной энергии активации анодного процесса, определенные температурно-кинетическим методом, имеют величины, характерные для замедленности стадии массопереноса (табл. 1).
Таблица 1.
Значение эффективной энергии активации анодного растворения металлов и сплавов в области предельных токов.
Металл | Ni | W | Zr | Hf | Ti | Ag | CрМ925 | ВК8 |
Аэф, кДж/моль | 16 | 14 | 13 | 14 | 17 | 16 | 14 | 12 |
Состав раствора оказывает значительное влияние на показатели анодного растворения металлов. Введение в состав водного электролита органических растворителей способствует повышению вязкости растворов (табл. 2) и уменьшению растворимости продуктов анодного окисления металла, поэтому в большинстве случаев приводит к уменьшению предельного анодного тока.
Таблица 2.
Кинематическая вязкость и электропроводность растворов
Н2О – 3 М органический растворитель – 1 М NaCl. Т=298 К.
Органический растворитель | – | Изопропиловый спирт | Этиленгликоль | Глицерин |
н∙106, м2/с | 0,956 | 2,198 | 1,443 | 1,953 |
κ, См/м | 7,24 | 4,58 | 5,59 | 5,87 |
При анодной поляризации вольфрама в растворах, содержащих моноэтаноламин (МЭА), наблюдается обратная картина – скорость растворения возрастает при увеличении содержания органического компонента до определенного предела (рис. 1.б). Это связано с тем, что для активации вольфрама необходима щелочная среда, а аминоспирты являются слабыми основаниями. В то же время, объемная концентрация гидроксид-ионов даже в растворе, содержащем 8 М МЭА, не превышает 0,015 моль/л, что недостаточно для обеспечения высокой скорости растворения вольфрама. Следовательно, МЭА принимает непосредственное участие в процессе анодного растворения вольфрама. Экстремальная зависимость предельного тока от концентрации МЭА обусловлена значительным повышением вязкости раствора.
При электрополировании серебра в растворах KCNS растворение протекает при наличии на его поверхности пассивирующей пленки, скорость растворения которой лимитируется подводом роданид-ионов. Уменьшение предельной плотности тока при введении в состав раствора глицерина обусловлено наложением процессов диффузии и гетерогенной химической реакции растворения солевого слоя. Экспериментальные зависимости 1/j - 1/![]() имеют линейный характер как в водном, так и в водно-органическом электролитах, однако не экстраполируются в ноль, что должно наблюдаться при чисто диффузионном контроле процесса. Следовательно, анодный процесс на серебряном электроде осложнен гетерогенной химической реакцией растворения солевого слоя AgSCN: AgSCN + SCN-→[Ag(SCN)2]-, для чего необходим избыток роданид-ионов. Рассчитанные значения реакционных токов составляют соответственно 45 и 17 А/см2 для водного и водно-глицеринового электролитов, что обусловлено, по-видимому, уменьшением растворимости AgSCN в водно-глицериновом электролите.
имеют линейный характер как в водном, так и в водно-органическом электролитах, однако не экстраполируются в ноль, что должно наблюдаться при чисто диффузионном контроле процесса. Следовательно, анодный процесс на серебряном электроде осложнен гетерогенной химической реакцией растворения солевого слоя AgSCN: AgSCN + SCN-→[Ag(SCN)2]-, для чего необходим избыток роданид-ионов. Рассчитанные значения реакционных токов составляют соответственно 45 и 17 А/см2 для водного и водно-глицеринового электролитов, что обусловлено, по-видимому, уменьшением растворимости AgSCN в водно-глицериновом электролите.
Роль органического растворителя не всегда ограничивается только изменением вязкости электролита и растворимости продуктов анодного окисления. В ряде случаев возможно его непосредственное участие в анодном процессе в качестве комплексообразователя (по механизму «поверхностного комплексобразования», предложенному ).
Нами с использованием метода ядерной магнитной релаксации доказано непосредственное участие молекул алифатического спирта в реакции анодного окисления никеля. Уменьшение величины коэффициента релаксационной эффективности с ростом концентрации органического компонента в растворе доказывает, что в первой координационной сфере катиона никеля (II) происходит процесс пересольватации.
Из величины константы равновесия были определены коэффициенты распределения сольватных форм никеля (II) для систем с различной концентрацией спирта. По значениям доли акваформы никеля (II) в водно-спиртовых системах были рассчитаны величины сольватационной составляющей энергии Гиббса (![]() ), характеризующей энергетику процесса переноса ионов Ni (II) из воды в водно-спиртовой растворитель:
), характеризующей энергетику процесса переноса ионов Ni (II) из воды в водно-спиртовой растворитель: ![]() . Как видно из рис. 2, имеет место корреляция между зависимостями плотности тока и
. Как видно из рис. 2, имеет место корреляция между зависимостями плотности тока и ![]() от содержания спирта, что подтверждает положение о непосредственном участии молекул спирта в процессе анодного растворения никеля.
от содержания спирта, что подтверждает положение о непосредственном участии молекул спирта в процессе анодного растворения никеля.
| Рис. 2. Зависимость скорости анодного растворения никеля (1) и величины сольватацион-ной составляющей энергии Гиббса переноса иона никеля (II) из воды в раствор: вода-спирт-хлорид натрия - хлорид никеля (2) от концентрации пропилового спирта. |
На примере анодного растворения меди установлена корреляция между донорным числом органического растворителя и шероховатостью поверхности после анодной обработки в водно-органических растворах. В качестве добавок были выбраны растворители с высокой основностью (гексиламин, триэтиламин), в водных растворах которых образуются аминные комплексы меди; диметилформамид, дающий смешанные гетеросольватные комплексы с ионами D - металлов, а также диоксан – растворитель с низкой основностью.
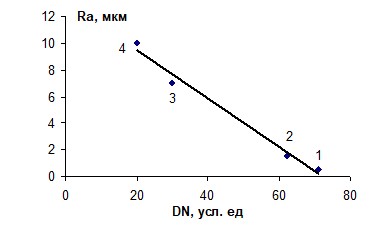
С усилением координирующей способности растворителя и соответственно ростом прочности связи Сu2+– растворитель полирующий эффект в смешанных водно-органических растворителях возрастает (рис. 3).
| Рис. 3. Зависимость качества обработанной поверхности меди (Ra, мкм) от донорного числа Гутмана (DN) для растворителей, используемых в качестве добавок: 1 – гексиламин, 2 – триэтиламин, ja = 0,8 А/см2, 294 К. |
Причина наблюдаемого эффекта электрополирования тесно связана с механизмом активирования анодного процесса путем нарушения оксидной пленки и образования смешанных гетеросольватных комплексов ионов меди с аминами.
Данные, полученные методом фотоэлектрополяризации, показали, что помимо массопереноса в растворе важную роль в эффекте выравнивания микропрофиля поверхности играют поверхностные оксидные или оксидно-солевые слои.
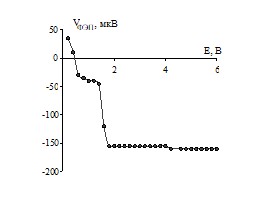
На вольфрамовом электроде величина отрицательной фото-ЭДС в водно-МЭА растворах на порядок меньше, чем в водном растворе хлорида натрия (рис. 4). Поэтому, в отличие от водного раствора NaCl, полная пассивация не наступает, а растворение протекает через слой поверхностного оксида.
|
|
Рис. 4. Зависимость ЭДС фотоэлектрополяризации от потенциала для вольфрамового электрода: а – в растворе 1 М NaCl; б – в водно-органических растворах: 1 – 1 М NaCl + 1 М МЭА; 2 – 1 М NaCl + 6 М МЭА.
Наличие такого резистивного слоя, наряду с формированием вязкого приэлектродного слоя, насыщенного продуктами растворения, является необходимым условием, обеспечивающим эффект электрополирования, что подтверждается данными табл. 3.
Таблица 3.
Качество поверхности вольфрамового электрода (высота микронеровностей RZ) после обработки в растворах 1 М NaCl с различным содержанием МЭА при потенциале 4 В.
СМЭА, моль/л | 0,1 | 0,5 | 1,0 | 2,0 | 4,0 | 6,0 | 8,0 |
RZ, мкм | 2,72 | 0,43 | 0,38 | 0,37 | 0,29 | 0,18 | 0,34 |
Аналогичные результаты получены и при исследовании анодного растворения никеля, циркония и гафния.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



 а
а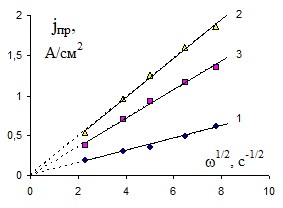 б
б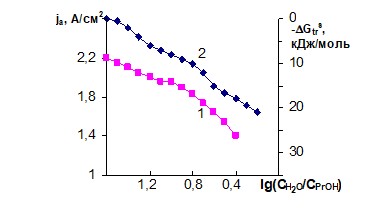
 а
а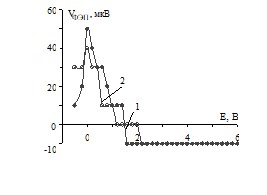 б
б