Таблица 6.
Зависимость шероховатости поверхности сплава ВК8 от потенциала.
Состав и концентрация электролита | Высота микронеровностей Rz, мкм | |||
1,3 | 2,3 | 3,3 | 4,0 | |
1М NaCl |
|
|
|
|
1М NaCl + 6М МЭА |
|
|
|
|
(В числителе указаны значения Rz при растворении в потенциостатическом режиме, а в знаменателе – при наложении прямоугольного напряжения,
f=200 Гц).
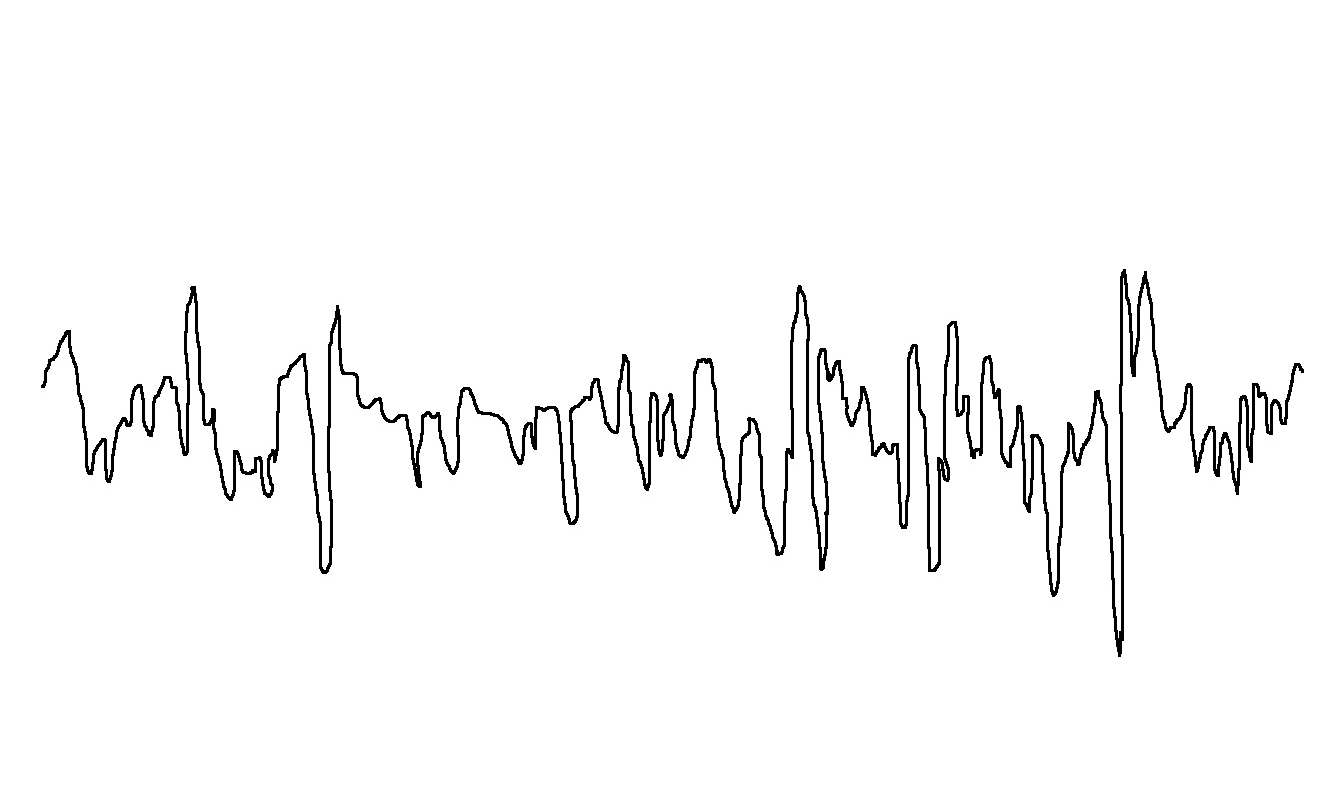
Положительный результат от применения нестационарного режима обработки был получен и при электрополировании серебра и сплава СрМ925. Было установлено, что оптимальный эффект сглаживания микропрофиля достигается при длительности импульса 0,5–1 с и скважности 8–10. Максимальное сглаживание микропрофиля имеет место при обработке серебра в импульсном режиме в растворе, содержащем глицерин (рис. 10, табл. 5).
|
|
|
|
Рис. 10. Профилограммы поверхности серебра после анодной обработки в растворах 4М KSCN (а, б) и 4М KSCN + 0,4М С3Н8О3 (в, г): а, в – постоянный ток, j=0,07 А/см2; б, г – импульсный ток, jи=0,7 А/см2, tи=1с, скважность 10. Продолжительность обработки 1 мин, Т=298 К. Вертикальное увеличение Ч5000, горизонтальное увеличение Ч100.
Ведение в роданидный электролит многоатомного спирта в оптимальной концентрации (0,4 моль/л) способствует также повышению отражательной способности обработанной поверхности на 15-20%.
Глава 5. Поведение металлов при химической обработке
В разделе 5.1 приведены результаты исследований поведения титана и меди в процессе химического полирования. Химическое полирование титана может быть использовано как в процессе предварительной подготовки деталей под гальванические покрытия, так и в качестве самостоятельной операции финишной обработки изделий из титановых сплавов. Традиционно применяемые в промышленности растворы для химического полирования титана содержат фтористоводородную и азотную кислоты. Такие растворы отличаются высокой агрессивностью по отношению к оборудованию, в ходе обработки образуется большое количество оксидов азота. Нами было предложено использовать в качестве активатора кислый фторид аммония, а в качестве окислителя - солянокислый гидроксиламин (Патент РФ № 000).
При изучении влияние концентраций компонентов раствора на стационарный потенциал титанового электрода установлено, что, изменяя соотношение концентраций окислителя и активатора, возможно достижение компромиссного потенциала поверхности, соответствующего протеканию коррозионного процесса в режиме полирования.
Наряду с составом раствора на показатели полирования большое влияние оказывает и температура. При низких температурах коррозионный ток недостаточен для получения эффекта сглаживания поверхности. Увеличение температуры от 250С до 800С приводит к увеличению скорости растворения почти в 3 раза.
По величинам расчетного коррозионного тока температурно-кинетическим методом была рассчитана эффективная энергия активации. Ее значения (в интервале температур 25-900С) находятся в пределах 16-22 кДж/моль, что указывает на протекание процесса со смешанным диффузионно-кинетическим контролем. Увеличение концентрации окислителя приводит к уменьшению энергии активации.
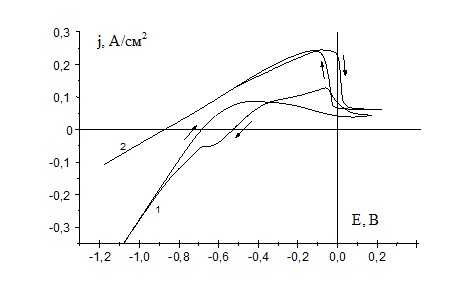
Электрохимическое поведение титана в растворе фторида аммония и в растворе химического полирования, представлено на рис. 11. По сравнению с чисто фторидным раствором, в растворе полирования катодная стадия процесса ускоряется, а анодная – тормозится.
| Рис. 11. Циклические потенцио-динамические (50 мВ/с) поляризационные кривые титанового электрода в растворах: 2 - 1,4 М NH4F⋅HF. Т=293 К. |
В отличие от чисто фторидного раствора, величина анодного тока в большей степени зависит от гидродинамических условий, что свидетельствует о существенной роли диффузионных ограничений. При увеличении скорости вращения дискового электрода возрастает как высота анодного тока максимума, так и значения токов на катодной ветви кривых. Следовательно, на скорость процесса влияет как подвод NH2OH⋅HCl к поверхности электрода, так и отвод продуктов растворения титана от поверхности в объем раствора, причем, судя по отношениям токов на вращающемся и неподвижном электродах, стадия отвода продуктов влияет сильнее.
Изменение содержания окислителя во фторидном растворе влияет и на анодный и на катодный процессы. При использовании неподвижного электрода увеличение концентрации окислителя приводит к уменьшению анодных токов начала пассивации титана, а на вращающемся электроде, наоборот, к повышению токов.
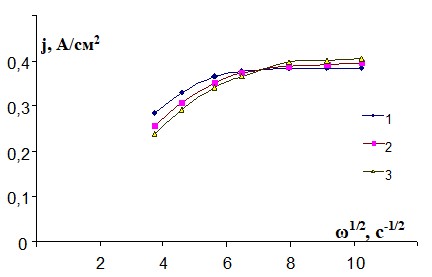
При увеличении концентрации NH2OH⋅HCl роль диффузии в растворе возрастает, о чем свидетельствуют результаты, представленные на рис. 12. Следует отметить, что в случае чисто диффузионного контроля зависимость jд - ![]() должна быть прямолинейной и выходить из начала координат, а зависимости, полученные нами – криволинейны. Это характерно для процессов, протекающих со смешанным диффузионно-кинетическим контролем. В таком случае становится возможным определение порядка реакции по уравнению:
должна быть прямолинейной и выходить из начала координат, а зависимости, полученные нами – криволинейны. Это характерно для процессов, протекающих со смешанным диффузионно-кинетическим контролем. В таком случае становится возможным определение порядка реакции по уравнению:![]() ,
,
где p – порядок реакции; jk – кинетический ток, jd – диффузионный ток.
| Рис. 12. Зависимость плотности тока в максимуме поляризационной кривой от скорости вращения титанового дискового электрода в растворах, содержащих 1 М NH4F⋅HF и различное количество NH2OH⋅HCl, моль/л: |
Определенное из зависимости lg j – lg (1-j/jd) значение кинетического тока составило 0,44 А/см2, а порядок реакции оказался близким к нулю. Такое же значение порядка реакции по окислителю было получено из угла наклона зависимости lgjmax – lgCNH2OH⋅HCl. По-видимому, гидроксиламин не принимает непосредственного участия в анодной стадии процесса, а некоторое увеличение анодного тока с ростом его концентрации обусловлено уменьшением поляризации сопряженного катодного процесса.
Изучение механизма растворения титана в процессе полирования проводили также при потенциостатических исследованиях. Одновременно со значениями тока и количества прошедшего через систему электричества измеряли убыль массы образца, из которой рассчитывали коррозионный ток, соответствующий растворению титана (в расчете на Ti (IV)). Вид кривых, построенных исходя из количества пропущенного электричества и из убыли массы, аналогичен, но значения плотностей тока заметно отличаются, за исключением области пассивации. Причина этого заключается в стадийном механизме окисления титана. В раствор переходят ионы титана в низших степенях окисления, а доокисление до TI(IV) происходит в объеме электролита кислородом воздуха (в случае чисто фторидного раствора) или с участием окислителя. В растворе, содержащем окислитель, растворение титана начинается при более положительном потенциале вследствие усиления роли оксидной пленки, и значения измеренных и рассчитанных токов заметно ниже.
О стадийном механизме окисления титана во фторидсодержащих средах и переходе в раствор в виде ионов Ti(III) свидетельствуют и результаты волюмометрических измерений. Объем водорода, выделяющегося при растворении титана, соответствует реакции окисления до Ti(III). Переход титана во фторидсодержащий раствор в виде Ti(III) отмечен и в работах и . Эффективная степень окисления (nэф) титана, рассчитанная принимая для анодной реакции ВТ=100%, меняется от 2 до 4, возрастая при увеличении потенциала анода. При потенциале, соответствующем максимуму анодного тока nэф=3.
Несмотря на высокую концентрацию активирующих фторид-ионов, на поверхности титана присутствует оксидный слой, о чем свидетельствуют результаты, полученные методом ФЭП. Свойства этого слоя изменяются в зависимости от состава раствора и электродного потенциала. Во фторидном растворе без NH2OH⋅HCl в области активного растворения фото-ЭДС близка к нулю, то есть роль оксидной пленки невелика и начинает заметно сказываться лишь в области пассивации (табл. 7). Введение в раствор окислителя способствует ускорению окислительных процессов и препятствует накоплению ионов Ti3+ в оксидном слое, что обеспечивает увеличение амплитуды фотоответа. Таблица 7.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



 а
а б
б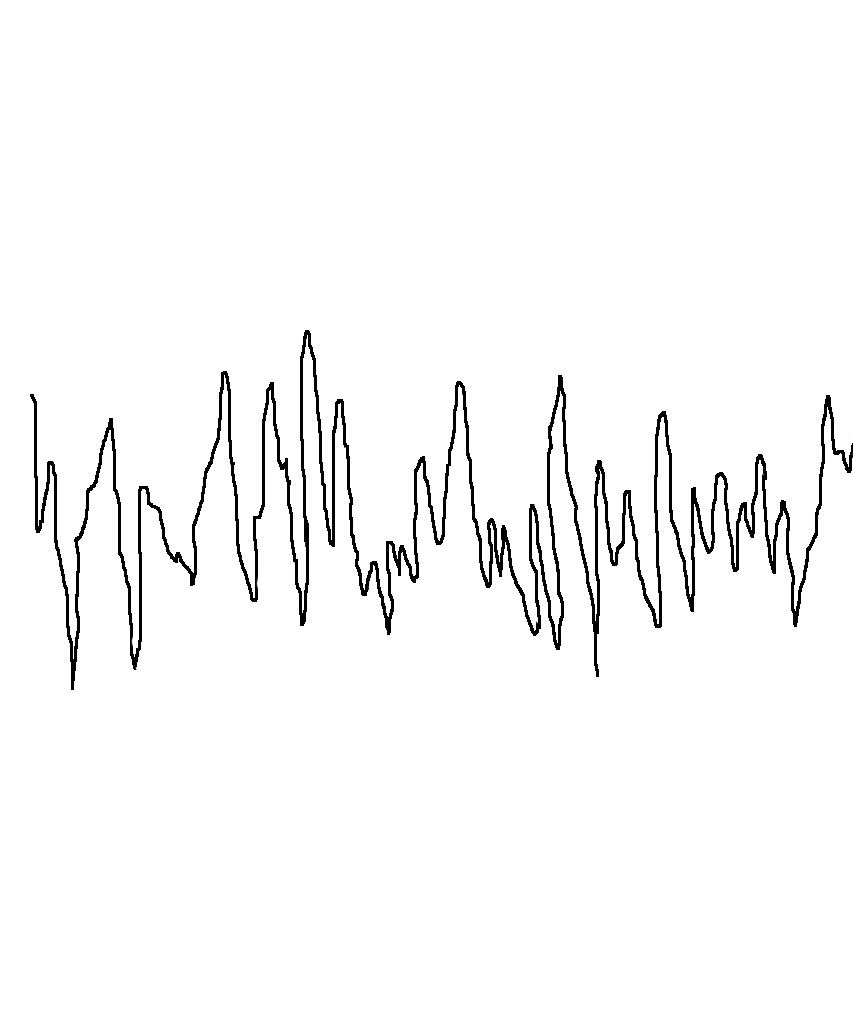 в
в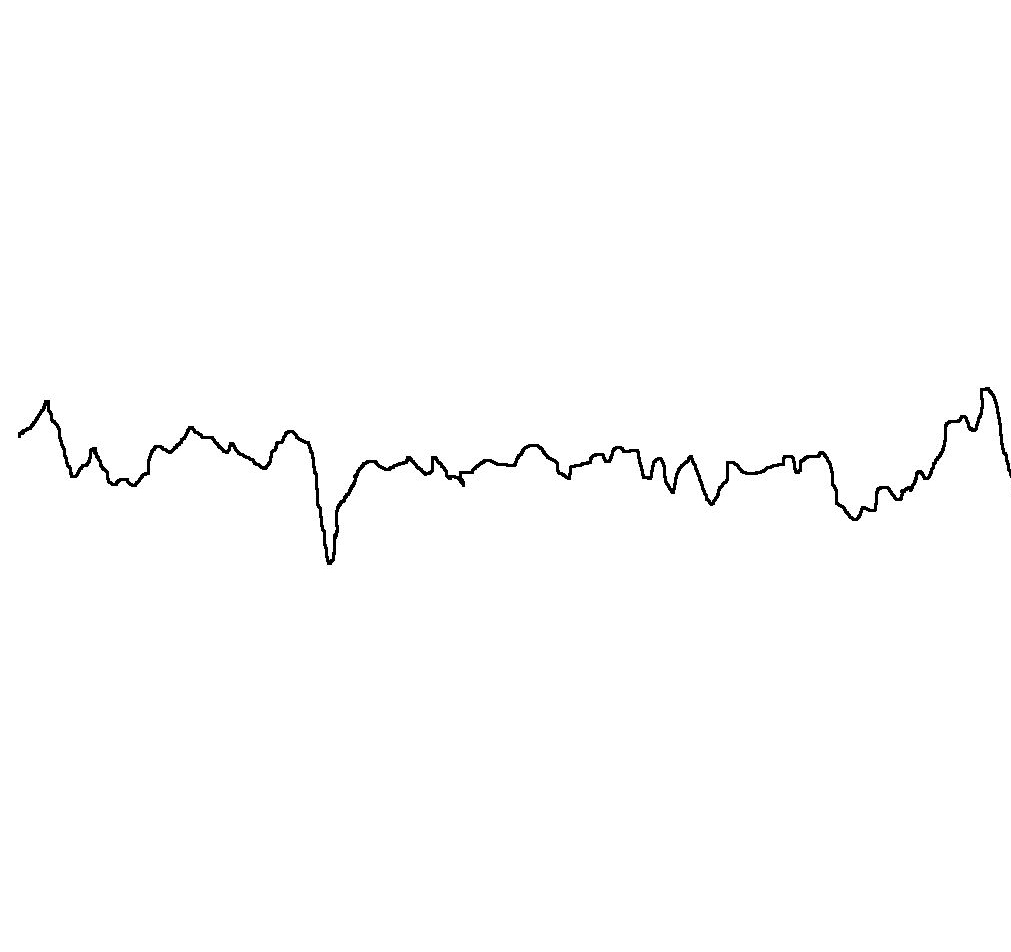 г
г