Зависимость фото-ЭДС титанового электрода от потенциала после обработки во фторидсодержащих растворах.
Состав раствора | Vфэп, мкВ после обработки при потенциале, В | ||||
-1,6 | -1,3 | -1,0 | -0,7 | -0,4 | |
1 М NH4F⋅HF | -10 | -50 | -130 | -80 | -110 |
2,8 М NH2OH⋅HCl, | -260 | -300 | -170 | -540 | -600 |
Импедансные измерения показали, что введение NH2OH⋅HCl во фторидный раствор приводит к резкому уменьшению емкости (на частоте 1000 Гц она снижается с 38,24 мкФ/cм2 до 17,73 мкФ/cм2). Электрическое сопротивление пленки, сформированной во фторидсодержащем растворе без окислителя, в 2 раза ниже, чем после обработки в растворе, содержащем гидроксиламин (5,01 и 10,21 Ом⋅см2 соответственно). Следовательно, увеличение содержания окислителя в растворе полирования приводит к изменению структуры и состава поверхностных пленок, что способствует уменьшению шероховатости.
Показатели процесса химического полирования титана во многом определяются соотношением концентраций активирующего компонента раствора и окислителя. При низкой концентрации NH2OH⋅HCl и при высокой концентрации NH4F⋅HF происходит растравливание поверхности. Увеличение содержания окислителя способствует повышению эффекта полирования. Повышение температуры раствора положительно влияет на качество поверхности.
Процесс глянцевания предпочтительнее проводить при температуре 104-1060С в растворе, содержащем NH2OH⋅HCl 200-250 г/л и NH4F⋅HF 60-100 г/л в течение 1-1,5 мин. В этих условиях отражательная способность достигает 60-80% при исходном значении 7-8 %, а степень сглаживания 70-85% (исходное Ra=0,7 мкм). При химическом полировании деталей, не требующих высокой степени блеска и имеющих точные размеры, обработку целесообразно проводить при меньшей температуре (80-900С) в растворе, содержащем NH2OH⋅HCl 200-250 г/л и NH4F⋅HF 60-80 г/л в течение 1 - 1,5 мин. При таких условиях сглаживание поверхности составляет от 48 до 75% (конечное Ra=0,2–0,3 мкм), отражательная способность 30-57%.
Используемые в настоящее время растворы химического полирования меди и ее сплавов на основе азотной кислоты характеризуются высокой агрессивностью, а процесс обработки в таких растворах сопровождается выделением большого количества оксидов азота. Нами был разработан ряд новых растворов для химического полирования меди и ее сплавов на основе фосфорной кислоты, в которых вместо азотной кислоты использованы ее соли.
Поляризационные измерения показали, что введение окислителя в раствор фосфорной кислоты способствует деполяризации катодного процесса, тогда как значение анодного тока не изменяется или даже уменьшается. Скорости как катодной, так и анодной реакций заметно зависят от гидродинамических условий и возрастают при увеличении скорости вращения дискового электрода.
Компромиссный потенциал коррозионного процесса при введении окислителя смещается в сторону положительных значений, что обусловлено усилением пассивационных явлений. При увеличении скорости вращения электрода он смещается в отрицательную сторону. Такого рода зависимости характерны для процессов коррозии, осложненных диффузией продуктов растворения от поверхности электрода в объем раствора.
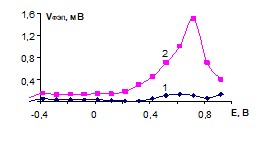
На анодной ветви обратного ходе наблюдается область предельного тока. Высота этой площадки линейно зависит от квадратного корня из скорости вращения дискового электрода. Следовательно, процесс химического полирования протекает при наличии на поверхности меди слоя продуктов анодного окисления, растворение которых протекает с диффузионным контролем. О существенной роли оксидных слоев в процессе ХП меди свидетельствуют значения фото – ЭДС, полученные при анодной поляризации меди в растворе фосфорной кислоты и при добавлении окислителя – в окислительной среде фото–ЭДС заметно выше (рис. 13).
| Рис. 13. Зависимость ЭДС фотоэлектрополяризации медного электрода от потенциала после обработки в растворах: 1 – 15 М H3PO4; 2 – 15 М H3PO4 + 3 M NH4NO3. |
Положительный знак фотоответа свидетельствует о формировании на поверхности полупроводниковой пленки с дырочной проводимостью. В таком поверхностном слое ионы меди способны перемещаться по катионным вакансиям, а электроны – по электронным дыркам (катионам более высокой степени окисления).
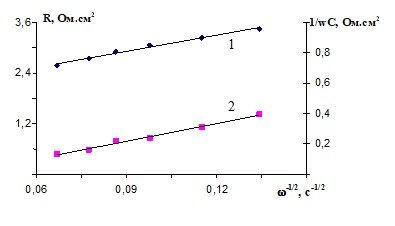
Для изучения свойств поверхностных слоев непосредственно в процессе обработки нами был использован метод электродного импеданса. При наложении потенциала, соответствующего области предельных токов растворения меди в фосфорной кислоте, имеет место линейная зависимость активной и реактивной составляющей импеданса от щ-1/2 (рис. 14), обусловленная уменьшением толщины диффузионного слоя с ростом скорости вращения электрода в соответствии с уравнением: δ = 1,61D1/3ν1/6ω-1/2. Такого рода зависимости характерны для случая замедленной стадии отвода продуктов растворения от электрода в объем раствора (полирование за счет формирования солевой пленки). Поэтому увеличение скорости вращения электрода, способствующее уменьшению толщины резистивного слоя, приводит к снижению активного высокочастотного сопротивления.
В растворе, содержащем нитрат аммония, при вращении электрода активная и реактивная составляющие импеданса при высоких скоростях вращения перестают зависеть от числа оборотов дискового электрода. По-видимому, в этом случае имеет место изменение природы лимитирующей стадии: ограничения по отводу ионов меди снимаются, и преобладающее влияние приобретает подвод акцепторов, необходимых для растворения оксидного слоя.
|
|
Рис. 14. Зависимости активной (1) и реактивной (2) составляющих импеданса медного дискового электрода от скорости вращения в растворах: а – 15 М Н3РО4. Еа=0,72 В; б – 15 М H3PO4 + 3 M NH4NO3. f=5000 Гц, Т=298 К.
Величины составляющих импеданса при обработке меди в окислительной среде заметно выше, чем значения, полученные в растворе фосфорной кислоты. Это свидетельствует об усилении влияния оксидного слоя при обработке меди в растворе химического полирования.
Таким образом, несмотря на существенное различие в электрохимических свойствах титана и меди, причины, определяющие возможность достижения эффекта химического полирования, остаются прежними – замедленность стадии массопереноса в растворе и формирование на поверхности металла полупроводникового оксидного слоя.
Дополнительные возможности управления процессом дает совместное введение в состав раствора полирования двух окислителей, восстановление одного из которых сопровождается выделением газа и возникновением конвективных потоков, а продукты восстановления второго остаются в жидкой фазе. При этом скорость растворения металла несколько снижается, но увеличивается интенсивность сглаживания микрорельефа.
Используя комбинации кислородсодержащих окислителей и реагентов, восстановление которых протекает без участия ионов гидроксония, а изменения сводятся к перезаряду иона, можно целенаправленно влиять на величину рН приэлектродного слоя и формирование оксидных слоев на поверхности металла. Реакции перезаряда ионов протекают с низким электрохимическим перенапряжением, вследствие чего возрастает роль диффузионных ограничений.
Исходя из вышеизложенных положений, нами были разработаны малоагрессивные растворы для обработки меди и сплавов на ее основе, содержащие одновременно два окислителя. Преимущества от введения второго окислителя видны из данных, представленных в табл. 8.
Таблица 8.
Показатели обработки поверхности меди и латуни ЛС59 в растворах различного состава.
№ п. п. | Показатель | Металл | Состав раствора, г/л | |
H3PO4 -1400 KNO3 - 450 | H3PO4 -1400 NH4NO3 – 280 Ox2 - 10 | |||
1 | Шероховатость поверхности Ra, мкм | Медь | 0,362 | 0,228 |
Латунь | 0,375 | 0,304 | ||
2 | Отражательная способность поверхности, % | Медь | 59 | 81 |
Латунь | 78 | 94 | ||
3 | Удельный объем выделяющегося газа, см3/г | Медь | 230 | 46 |
Латунь | 235 | 49 | ||
4 | Температура раствора, оС | 90 - 100 | 20 - 40 |
Предлагаемые растворы характеризуются невысокой скоростью съема металла (3 – 5 мкм/мин.), что облегчает управление процессом. Пониженная температура и скорость растворения металла дают возможность вести обработку деталей насыпью в установках барабанного типа. Их применение позволяет в 4 – 5 раз сократить количество вредных выбросов оксидов азота.
В разделе 5.2 рассмотрены вопросы подготовки поверхности титана перед электрохимическим серебрением. Для обеспечения прочного сцепления покрытия с титаном применяют сложные многостадийные схемы, включающие нанесение промежуточных подслоев никеля и меди. Однако при эксплуатации деталей в жестких климатических условиях при нарушении сплошности серебряного покрытия возникают гальванические пары (Ag-Cu, Ag-Ni), что приводит к коррозии и сокращению срока эксплуатации деталей. По этой причине целесообразно осаждать серебро непосредственно на титан. Для обеспечения надежного сцепления покрытия с основой, его сплошности и равномерности необходима высокая степень активности поверхности и ее сохранение в момент погружения деталей в электролит. Такие свойства поверхности титана обеспечивает гидридная обработка.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



 а
а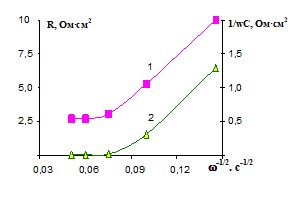 б
б