Цель работы: Закрепление навыков по приготовлению, стандартизации растворов.
Реактивы и оборудование:
Реактивы: трилон Б (т. в), дистиллированная вода
Оборудование: аналитические весы, бюкс, мерная колба на 250мл, электроплитка.
Теоретическая часть.Стандартные растворы готовят различными способами.
1. Из химически чистого вещества. Берут навеску точно на аналитических весах и растворяют ее в мерной колбе. Концентрацию рассчитывают математическим путем.
2. Из нехимически чистого вещества. Берут навеску на технохимических весах и растворяют в воде, объем которой измеряют цилиндром или мензуркой. Концентрацию такого стандартного раствора определяют титрованием исходного раствора.
3.Из фиксанала. Фиксанал — это стеклянная, герметически запаянная ампула с точным количеством раствора или сухого вещества. Чаще всего из одного фиксанала можно приготовить 1л 0,1 н. или 1 л 0,01 н. раствора, если растворять в мерной колбе вместимостью 1 л. Беря различное количество фиксаналов и мерные колбы разной вместимости, можно готовить растворы различной концентрации.
Чаще всего стандартные растворы готовят вторым способом. Для работы удобнее всего использовать 0,1 и. стандартные растворы.
II. Методика выполнения работы:
Навеску Трилона Б![]()
![]() г. Взвешивают на аналитических весах растворяют в мерной колбе при нагревании. Объем колбы доводят до метки.
г. Взвешивают на аналитических весах растворяют в мерной колбе при нагревании. Объем колбы доводят до метки.
ПРОТОКОЛ АНАЛИЗА
Масса трилона Б-________, г;
Объем трилона Б общий-_______, мл;
Эквивалент трилона Б-_______, г/моль.
III. Расчетная часть:
По формуле 6.1 определяем нормальность трилона Б
Nтр. Б= | (6.1) |
где
mmp. Б-масса трилона Б, г;
Vmp. Б-обьем трилона Б общий, мл;
Эmp. Б-эквивалент трилона Б, г/моль;
mmp. Б=________, г; Vmp. Б=_______, мл; Эmp. Б=_______, г/моль.
Nтр. Б=![]()
![]() =______, г∙э/л
=______, г∙э/л
Ответ
IV. Заключение:
Подпись преподавателя:_____________
Вопросы и задачи для самоконтроля
1. Каким способом приготовлен раствор
Задача1. Определить массу соли и объем дистиллированной воды, необходимых для получения 230г 12% поваренной раствора.
Задача 2.Какую массу соли и объем воды необходимо взять для приготовления:
50 г 0,5 %-ного раствора;
60 г 1 %-ного раствора;
70 г 2 %-ного раствора.
ЛАБОРАТОРНАЯ РАБОТА 7-ОПРЕДЕЛЕНИЕ ПРОЦЕНТНОГО СОДЕРЖАНИЯ КАЛЬЦИЯ В КАЛЬЦИТЕ
Цель работы: определение процентного содержания кальция в кальците Оценка качества выполненных работ и правильности полученного результата.
Материалы и оборудование:
Материалы и реактивы: кальцит (мел) твер., соляная кислота 2н, буферная смесь, индикатор эриохром черный, стандартный раствор раствора трилона Б
Оборудование: аналит. весы, химический стакан на 50мл, колба для титрования, бюретка, пипетка, мерная колба на 100 мл.
Теоретическая часть.
Строительная воздушная известь – вяжущее вещество, получаемое умеренным обжигом не до спекания (900…1100єС) карбонатных горных пород (известняков, мела, доломитов и т. п.), состоящих преимущественно из углекислого кальция СаСО3 и небольшого количества углекислого магния МgСО3, а также примесей кварца и глины, которые ухудшают качество строительной извести. Содержание глины в карбонатных породах не должно превышать 6 %. В результате обжига получают комовую негашеную известь, называемую «кипелкой», и состоящую в основном из оксида кальция СаО рисунок 7.1.
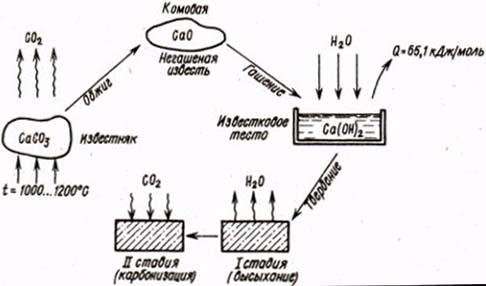
Рисунок 7.1- Получение, гашение и твердение воздушной извести
В зависимости от содержания оксида магния МgО воздушную известь разделяют на кальциевую (содержание МgО≤ 5 %), магнезиальную (МgО - от 5 до 20 %) и доломитовую (МgО от 20 до 40 %).
Методика выполнения работы: Приготовление исследуемого раствора.Исследуемый кальцит тонко растирают в ступке и взвешивают на аналит. весах в химическом стакане, предварительно взвешивают примерно 0,2гр. А в этот стакан добавляют 15мл. 2н. соляной кислоты и нагревают смесь на электроплитке до растворения кальцита. Раствор охлаждают и переносят в мерную колбу. Не доводя объем колбы до метки, раствор кипятят 5 мин. для удаления углекислого газа. После охлаждения раствора объем колбы доводят до метки. Реакция при растворении:
CaCO3+2HCl=CaCl2+H2O+CO2
Титрование.
Порцию исследуемого раствора 20мл. пипеткой переносят в колбу для титрования, добавляют 15мл. буферной смеси и немного индикатора (раствор хорошо размешать до растворения индикатора) окраска должна быть вишнево-красноватой. Титруют стандартным раствором трилона Б до появления синезеленой окраски.
ПРОТОКОЛ АНАЛИЗА
Масса исследуемого вещества -_______, г;
Объем исследуемого общий -______, мл;
Объем исследуемый на титр. -_____, мл;
Объем трилона Б на титрование-ср.![]()
![]() мл.
мл.
III. Расчетная часть:
По формуле 7.1 определяем нормальность исследуемого вещества
По формуле 7.2 определяем массу Ca
По формуле 7.3 определяем процентное содержание Ca
Nиссл. = | (7.1) |
где Nmp. Б-нормальность трилона Б, г∙э/л; Vmp. Бср.-обьем трилона Б среднее, мл; Vuccл. mump-обьем исследуемого раствора пошедшего на титрование, мл. Nmp. Б=________, г∙э/л; Vmp. Бср.=______, мл; Vuccл. mump=_____, мл Nиссл. = | |
MCa= | (7.2) |
Nuccл-нормальность исследуемого раствора, г∙э/л; Vuccл. общ-обьем исследуемого раствора общий, мл; ЭCa-эквивалент Ca, г/моль. Nuccл=______, г∙э/л; Vuccл. общ=_____, мл; ЭCa=_____, г/моль. MCa= | |
% Ca= | (7.3) |
где mCa-масса Са, г;
muccл-масса исследуемого расствора, г.
mCa-______, г; muccл-______, г.
% Ca= ![]()
![]() =_____, %
=_____, %
Ответ
IV. Заключение:
Подпись преподавателя:_____________
Вопросы для самоконтроля
Виды воздушной строительной извести. Основные показатели качества воздушной строительной извести. Области применения воздушной извести. Что называют строительной известью?ЛАБОРАТОРНАЯ РАБОТА 8-ОПРЕДЕЛЕНИЕ КАЧЕСТВА ИЗВЕСТИ
Цель работы:определение содержания в извести активных СаО+МgО, скорости гашения извести. Оценка качества выполненных работ и правильности полученного результата.
Материалы и оборудование:
Материалы: комовая известь негашеная, соляная кислота 1н HCl, раствор фенолфталеина, вода, метилоранж,1н NaOH.
Оборудование: сито 0,2мм., стакан, термометр, коническая колба, часовое стекло, песочная баня.
Теоретическая часть.
При взаимодействии негашеной извести с водой происходит гидратация оксида кальция по реакции:
СаО + Н2О = Са(ОН)2 + Q,
где q – количество тепла, выделяющегося при реакции.
Этот процесс называют гашением извести. Он сопровождается выделением значительного количества тепла. При этом температура гасящейся извести повышается до определенного максимума. С окончанием реакции прекращается выделение тепла, и температура смеси падает. Момент начала снижения температуры смеси является признаком прекращения реакции гашения извести.
Сущность метода заключается в определении максимально высокой температуры гашения извести и времени, за которое произошло повышение температуры.
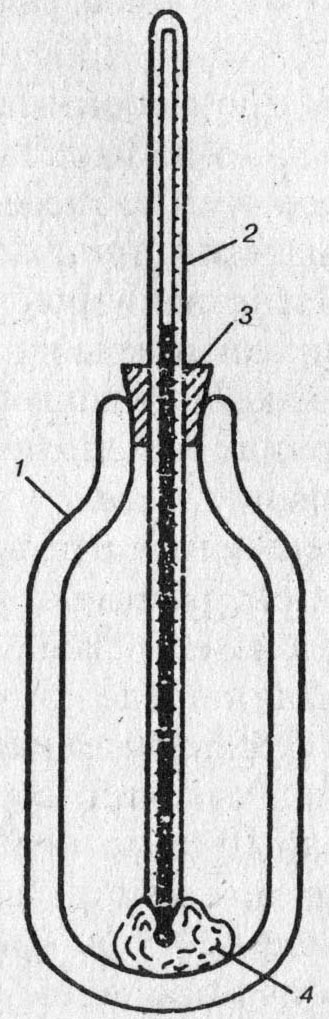
Для испытаний используют сосуд Дьюара указанный на рисунке 8.1, который состоит из термосной колбы (1), термометра со шкалой на 150є (2) и пробки (3).
Рисунок 8.1- Прибор для определения скорости гашения извести |
Определение скорости гашения извести
В зависимости от скорости гашения известь делят на быстрогасящуюся (скорость гашения до 10мин.), среднегасящуюся (скорость гашения от 10 до 30мин.) и медленногасящуюся (скорость гашения свыше 30мин.)
Для определения скорости гашения извести пробу измельчают до прохода ее через сито 0,2 мм. Навеску 10 грамм измельченной извести помещают в сосуд Дьюара, в который предварительно наливают 20мл. воды, имеющей температуру 20 оС. Закрывают пробкой, в которую установлен термометр, и взбалтывают. Затем сосуд оставляют в покое и через каждые 30сек. отмечают температуру гасящейся извести. Наблюдения ведут до достижения максимальной температуры и начала ее падения.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |