Затем реакционную смесь нагревают почти до кипения и держат при этой температуре при постоянном перемешивании 20-30 мин.
После этого смесь оставляют дня на два. По истечении этого времени осадок примет темно-синий цвет. С него осторожно слить раствор и промыть чистой водой и отфильтровать.
Получение зеленых красок: яр-медянки и зелени Гинье.
Для получения яр-медянки к 100 мл 1M раствора СuSO4 прилейте 100 мл раствора 1М. Напишите уравнение происходящей реакции.
Выпавший осадок промойте несколько раз водой, затем растворите его в уксусной кислоте, избегая избытка последней. Если останутся какие-либо нерастворимые примеси, то жидкость профильтруйте. Полученный раствор упарьте, не доводя жидкость до кипения, затем охладите и дайте постоять для уплотнения осадка. После этого отделите кристаллическую яр-медянку от маточного раствора. Кристаллы высушите.
Для получения зелени Гинье смешивают в одну весовую часть двухромового калия с тремя весовыми частями кристаллической борной кислоты. Смесь загружают в тигель, около 30 минут нагревают до плавления. Извлекают из тигля оставшуюся массу, измельчают в ступке, переносят в фарфоровую чашку, заливают водой и кипятят около 1-2 часа. При выщелачивании полученного сплава происходит реакция. Напишите уравнение реакции. Раствор, содержащий борную кислоту, сливают с осадка и выпаривают во второй чашке до начала выделения кристаллов. Осадок зеленого цвета, полученный после удаления борной кислоты, промывается горячей водой, затем 1М раствором серной кислоты и, наконец, 1М раствором едкого натра, после чего его отфильтровывают и сушат при температуре около 100°С.
4. Задания и оформление работы
Описать методы получения минеральных красок. Написать уравнения соответствующих уравнений. Провести расчеты по выходу полученных красок. Оформить результаты анализа.
Блиц-тест
1. Основным компонентом всех лакокрасочных материалов, обуславливающих образование пленки, является:
А. пленкообразователи В. краски С. пигмент
D. отвердители Е. сиккативы
2. Растворы пленкообразующих веществ в органических растворителях:
А. лаки В. краски С. обычный пигмент
D. клей Е. наполнители
3. Минимальное количество пленкообразующего необходимое для превращения 100т пигмента - это:
А. красящая способность В. маслоемкость
С. Диспергируемость D. светостойкость Е. укрываемость
4. Как называются высокодисперсные окрашенные порошки нерастворимые в воде и пленкообразующих веществах?
А. неорганические пигменты В. органические пигменты
С. синтетические вещества D. минеральные краски
Е. отвердители
5. Как называются однородные суспензии пигментов в пленкообразующих веществах?
А. лаки В. краски С. обычный пигмент
D. клей Е. наполнители
Контрольные вопросы
Опишите способ получения берлинской лазури. Напишите уравнения реакции. Опишите способ получения цинковых белил. Напишите уравнения реакции. Как получают зелень Гинье? Напишите уравнения реакции. Опишите способ получения берлинской лазури. Напишите уравнения реакции. В чем отличие минеральных красок от органических? Что является сырьем для получения минеральных красок? Перечислите области применения минеральных красок. Как классифицируются минеральные краски?
Литература
, Технология лаков и красок. М., Химия, 1990, 384с. Химия и технология лакокрасочных материалов. Л, Химия, 1989, 448с. , , Пигментирование лакокрасочных материалов. Л.: Химия, 1986, 160с. , , Пигменты и пигментированные лакокрасочные материалы. Л.: Химия, 1987, 198с.
Работа 8. ПОЛУЧЕНИЕ МЫЛА
1. Цель работы
1. Получение мыла из пищевого сырья
2. Определение содержания жирных кислот в образце мыла
2. Теоретическая часть
В группу моющих средств входят моющие, водосмягчающие, отбеливающие средства. Моющими средствами называют сложные органические соединения, применяемые в чистом виде или с добавками для стирки изделий из текстильных волокон и мытья различных предметов домашнего обихода. Эти средства облегчают также отбеливание и крашение тканей, изготовление эмульсий и суспензий при получении пищевых товаров, красочных составов, очистку и измельчение руд и других природных материалов, повышают антифрикционную способность смазочных материалов и т. д.
Основной (активной) частью моющих средств являются моющие вещества. Они представляют собой органические соединения, обладающие поверхностной активностью, способностью образовывать пену и полуколлоидный раствор в воде. Благодаря поверхностной активности они понижают поверхностное натяжение воды, увеличивая тем самым ее смачивающую способность. В молекуле моющих веществ имеется длинная углеводородная цепь R и короткую часть в виде реакционной солеобразующей (карбоксильной) группы. Соотношение длины неполярной и полярной частей в молекуле обусловливает различную растворимость моющего вещества в воде. С увеличением длины углеводородной цепи понижается растворимость, но повышается твердость моющего вещества.
Мыла – это натриевые или калиевые соли высших жирных кислот, гидролизующихся в водном растворе с образованием кислоты и щелочи.

Общая формула твердого мыла:
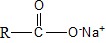
Сырьем для получения обычного мыла, используемого в быту при стирке и мытье, служат жиры животного или растительного происхождения. Они содержат до 40% насыщенных жирных кислот. Жиры (триацилглицерины, триацилглицериды) – сложные эфиры трехатомного спирта глицерина и высших жирных кислот. Их общая формула:
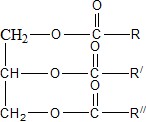
В состав животных жиров входят смеси предельных высших карбоновых кислот (маргариновая С16Н33COOH, пальмитиновая С15Н31COOH, стеариновая С17Н35COOH), а в состав растительных жиров — непредельные (олеиновая С17Н33СООН, линолевая С17Н31СООН, линоленовая С17Н29СООН).
Натриевое мыло твердое, калиевое — жидкое. Сорт мыла зависит от содержания в нем жирных кислот, которое выражается в процентах.
Наша промышленность выпускает 72%-, 70%- и 60% - ное мыло. В высококачественное хозяйственное и туалетное мыло добавляют красители и отдушки.
Cоли, образованные сильными основаниями щелочных металлов и слабыми карбоновыми кислотами, подвергаются гидролизу:
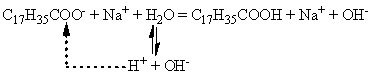
Образовавшаяся щелочь эмульгирует, частично разлагает жиры и освобождает таким образом прилипшую к ткани грязь. Карбоновые кислоты с водой образуют пену, которая захватывает частицы грязи. Калиевые соли по сравнению с натриевыми лучше растворимы в воде и поэтому обладают более сильным моющим свойством.
Гидрофобная часть мыла проникает в гидрофобное загрязняющее вещество, в результате поверхность каждой частицы загрязнения оказывается окруженной оболочкой гидрофильных групп. Они взаимодействуют с полярными молекулами воды. Благодаря этому ионы моющего средства вместе с загрязнением отрываются от поверхности ткани и переходят в водную среду. Так происходит очистка загрязненной поверхности моющим веществом.
Производство мыла состоит из двух стадий: химической и механической. На первой стадии (варка мыла) получают водный раствор натриевых (реже калиевых) солей, жирных кислот или их заменителей.
В общем виде получение мыла можно представить следующими реакциями:
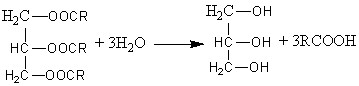
где R = С11Н23; С15Н31; С17Н31 и др.
RСООН + NaОН → RСООNa + Н2О
Так как в настоящее время основным сырьем для получения мыла являются растительные жиры, их предварительно гидрируют водородом в присутствии катализатора (например, никеля) и получают твердые жиры, называемые саломасом. Получение мыла проводят в несколько стадий:
1. Гидролиз, расщепление жиров водяным паром в автоклавах при температуре 523—573 К и давлении 25 • 105 и 30 • 105 Па.
2. Очистка полученных жирных кислот.
3. Омыление кислот гидроксидом натрия или калия (или кальцинированной содой).

3. Экспериментальная часть
Химические реактивы, посуда, приборы
- жир гидроксид натрия этанол или пропанол хлорид натрия (насыщ. Р-р с = 1,16 – 1,18 103 кг/м3 туалетное мыло соляная кислота фарфоровый стакан на 100-150 мл (2шт) колбы на 100-250 мл стеклянные палочки
Порядок проведения работы
Получение мыла
Проводят гидролиз жиров спиртовым раствором гидроксида натрия. Для этого взвешивают 6 г жира, помещают в фарфоровый стакан и нагревают до расплавления. Готовят раствор гидроксида натрия путем растворения 2,5 г NaOH в 6 мл. H2O и 15 мл этанола или пропанола -1. Спиртовой раствор NaOH приливают при перемешивании к расплавленному жиру. Полученный раствор кипятят в течении 10-15 мин., добавляют к нему 10 – 15 мл насыщенного раствора хлорида натрия и охлаждают в бане с водой. Образовавшийся на поверхности слой мыла извлекают из стакана, тщательно высушивают фильтровальной бумагой и взвешивают. Рассчитывают выход мыла на взятый жир.
Определение содержания жирных кислот
Взвешивают 5 г туалетного мыла или хозяйственного мыла, нарезают его тонкими полосками, помещают в стакан емкостью 100 мл, приливают 50 мл дистиллированной воды и нагревают на закрытой электроплитке до полного растворения мыла. К полученному раствору добавляют 10 мл соляной кислоты (1:1) и продолжают нагревание до образования на поверхности раствора маслянистого слоя (опыт проходит лучше, если в раствор поместить стеклянную палочку). Стакан охлаждают, вынимают стеклянные палочки и через образовавшееся отверстие сливают жидкость. Оставшиеся в стакане жирные кислоты переносят на фильтровальную бумагу и высушивают. Остатки их снимают со стенок стакана скальпелем. Полученные жирные кислоты взвешивают.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 |




