|
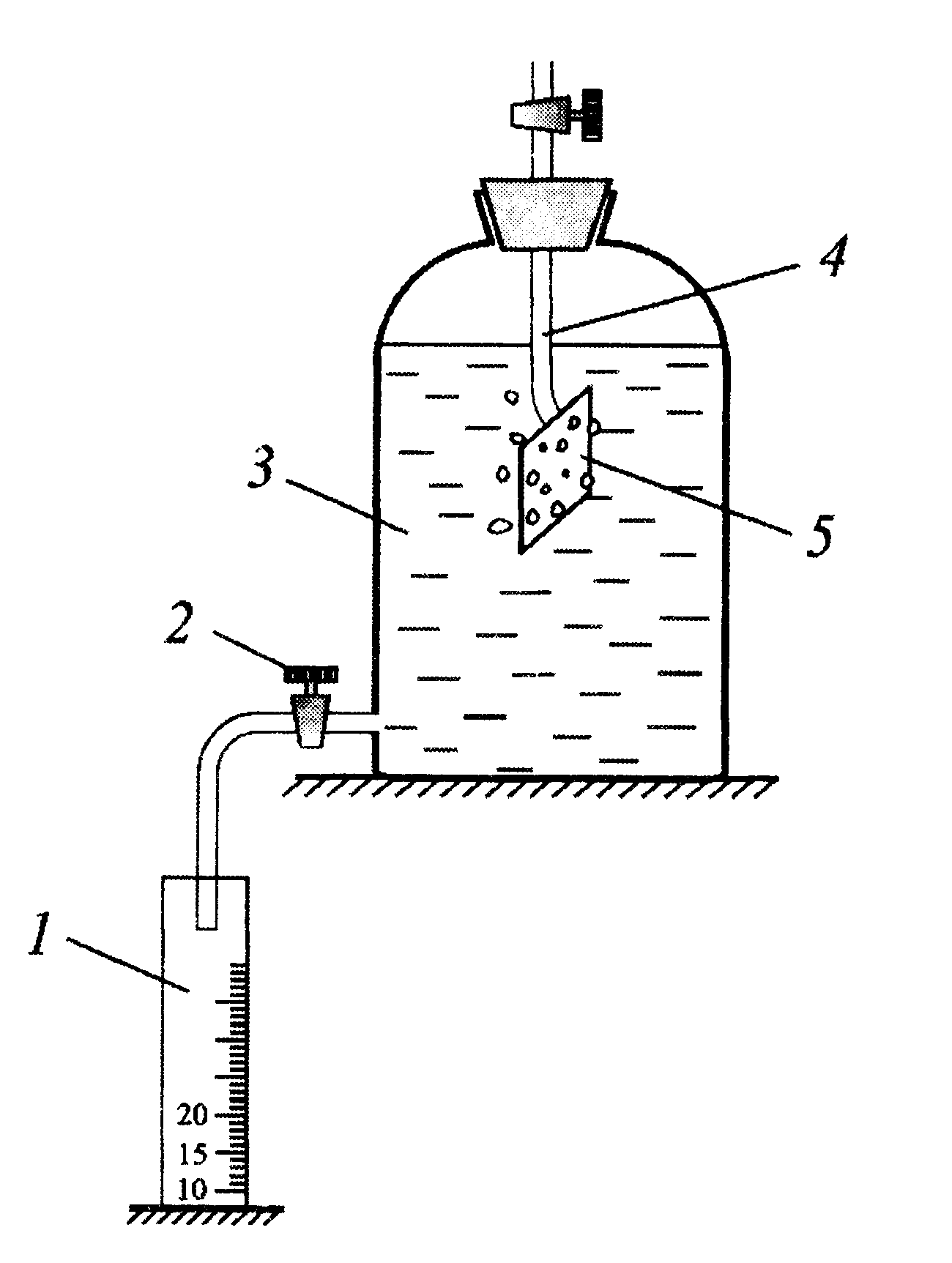
Рис. 5.1. Схема лабораторной установки: 1 – мерная бюретка, 2 – кран, 3 – емкость, 4 – испытуемый образец, 5 – стеклянная подвеска |
Она представляет собой стеклянную емкость объемом 1-2литра 3, заполненную на две трети 5%-ным раствором серной кислоты. Емкость, герметично закрывающуюся резиновой пробкой, имеет внизу краник 2, через который в ходе эксперимента вытесненная кислота сливается в мерную бюретку 1. Испытуемый образец 4 помещают в емкость 3 при помощи стеклянной подвески 5.
Порядок проведения эксперимента
Перед проведением эксперимента образцы предварительно нужно подготовить, для чего с помощью мелкой наждачной бумаги их поверхность тщательно зачищают. После этого штангенциркулем определяют их геометрические размеры: высоту, ширину и толщину. Далее определяют площадь образца (в см2) и результаты расчета записывают в таблицу 5.1.
Поверхность образца тщательно обезжиривают раствором соды или ацетоном, взвешивают на аналитических весах, надевают на стеклянный крючок подвески 5 и помещают в емкость 3, плотно закрыв резиновую пробку, после чего открывают кран 2. Фиксируют уровень вылившейся из емкости кислоты и отмечают время начала эксперимента. Кран 2 остается открытым до конца эксперимента, который длится 60-100 мин. Через каждые 20 мин определяют количество вытесненной кислоты и данные записывают в таблицу 5.1.
По окончании эксперимента кран 2 необходимо закрыть, извлечь из емкости испытуемый образец, тщательно промыть водой, просушить и взвесить, вновь записав данные в таблицу.
Таблица 5.1
Экспериментальные данные по определению скорости коррозии
Материал образца | Площадь, S, см2 | Масса образца, г | Дmгр=mн – mк, г | Объем вытесненной кислоты v (мл) за время* | ||
Начальная mн | Конечная mк | 20 мин | 40 мин | 60 мин | 80 мин | 100 мин |
* - объем вытесненной кислоты соответсвует показаниям бюретки.
4. Обработка результатов эксперимента
Для определения убыли металла исходят из того, что при растворении одного грамм-моля железа (55,85г.) при нормальных условиях (760 мм рт. ст. и 273К) выделяется 22,4л водорода. Следовательно,
![]()
![]() (5.1)
(5.1)
здесь vi – объем выделившегося водорода за соответствующий интервал времени (таблица 5.2).
Скорость коррозии щкор образца определяют по уравнению:
![]()
![]() (5.2)
(5.2)
здесь Дt – время эксперимента, ч; S – площадь образца, см2.
Глубинный показатель коррозии, характеризующий уменьшение толщины металла в единицу времени, определется по формуле:
![]()
![]() (5.3)
(5.3)
Здесь с – плотность материала образца, кг/м3.
Таблица 5.2
Результаты обработки экспериментальных данных
Интервал времени, Дt, мин | Объем выделившегося водорода Дvi, г* | Масса растворенного металла, Дmi, г | Скорость коррозии (щкорр)i, г/(см2ч) | Глубинный показатель коррозии, Пi, мм/год |
0-20 | ||||
20-40 | ||||
40-60 | ||||
60-80 | ||||
80-100 |
*- объем вылелившегося водорода соответсвует объему вытесненной кислоты
В практике эталонным обычно считается гравиметрический метод испытания.
Средняя скорость коррозии, определенная гравиметрическим методом, рассчитывается по формуле:
![]()
![]() (5.4)
(5.4)
здесь ![]()
![]() - убыль материала образца, определенная гравиметрическим методом, г (см. табл 5.1); t – полное время эксперимента, выраженное в часах.
- убыль материала образца, определенная гравиметрическим методом, г (см. табл 5.1); t – полное время эксперимента, выраженное в часах.
Средняя скорость коррозии, определенная объемным методом, рассчитывается как
![]()
![]() (5.5)
(5.5)
где n – количество слагаемых (щкорр)i.
Масса растворенного металла (г), рассчитанная объемным методом, определяется по формуле:
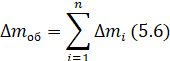
где Дmi – данные из таблицы 5.2.
Тогда глубинный показатель коррозии по гравиметрическому методу составит
![]()
![]() (5.7)
(5.7)
Средняя величина глубинного показателя по объемному методу определяется как
![]()
![]() (5.8)
(5.8)
здесь Пi – данные таблицы 11.2.
Погрешность объемного метода определяют по уравнению
![]()
или
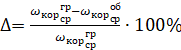
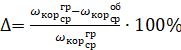 (5.9)
(5.9)
Все результаты расчетов вносят в таблицу 5.3.
Таблица 5.3
Сводная таблица результатов, полученных двумя методами
Материал образца | Масса растворенного металла Дmi, г | Средняя скорость коррозии (щкорр)ср, г(см2.ч) | Глубинный показатель коррозии Пi, мм/год | ||
гравимет рический | объемный | Гравимет рический | объемный | Гравимет рический | объемный |
5. Задание к работе
Для наглядности результаты расчета экспериментальных данных следует представить графиком зависмости (щкорр)=f(t).
В выводах по работе необходимо отразить :
1. коррозионную стойкость испытуемых образцов по 10-бальной шкале, представленную в таблице 5.4.
2. характер коррозионного процесса и его развитие во времени.
Таблица 5.4
Десятибальная шкала коррозионной стойкости металлов
Металлы | Глубинный показатель, мм/год | Балл |
Совершенно стойкие | Менее 0,001 | 0 |
Весьма стойкие | 0,001-0,005 0,005-0,01 | 1 2 |
Стойкие | 0,01-0,05 0,05-0,1 | 3 4 |
Пониженностойкие | 0,1-0,5 0,5-1,0 | 5 6 |
Малостойкие | 1,0-5,0 5,0-10,0 | 7 8 |
Нестойкие | Свыше 10,0 | 9 |
Блиц-тест
1.Электрохимическую коррозию металла вызывает
A. контакт металла с кислородом B. контакт металла с оксидами серы
C. контакт с другими металлами D. контакт металла с электролитами
Е. электричество
2. Химическую коррозию металла вызывают
A. кислород B. все перечисленные вещества C. хлор
D. оксиды серы E. контакт с другими металлами
3. К электрохимическим методам защиты металлов от коррозии относится
A. никелирование B. Шлифование E. деструкция
C. воронение D. катодная защита
4. В качестве легирующих добавок при получении нержавеющих сталей используют
A. Zn и Mn B. Ag и Au C. Ni и Cu
D. Cr и Ni E. K и Na
5. Глубинный показатель коррозии определется по формуле:
A. ![]()
![]() B.
B. ![]()
![]() C.
C. ![]()
![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 |