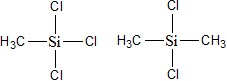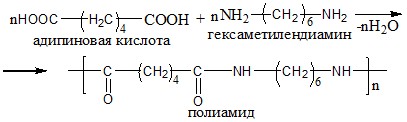
II. Реакции полимеризации, заключающиеся в соединении молекул низкомолекулярного вещества (мономера) с образованием макромолекул полимера, причем каких-либо веществ при этих реакциях не образуется.
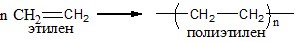
К пластмассам относят обширную группу синтетических материалов, главной составной частью которых служат смолы, способные при повышенной температуре и давлении переходить в пластическое состояние, формоваться под воздействием внешних сил и затем устойчиво сохранять приданную форму при эксплуатации. Составными частями смесей, используемых для формирования пластмасс, являются:
1. Смола – важнейшая составная часть, скрепляющая все компоненты в монолитное целое и придающая композиции пластичность, способность формоваться а также электроизоляционные, антикоррозионные и другие важнейшие свойства.
2. Пластификаторы – вещества, повышающие пластичность смол и облег-чающие формирование из них изделий.
3. Наполнители – инертные вещества, придающие пластмассам те или иные механические свойства и уменьшающие содержание связующего вещества.
4. Растворители – вещества, снижающие вязкость связующего вещества и испаряющиеся при формовке изделий.
5. Стабилизаторы – вещества, обеспечивающие химическую стабильность пластмассы, т. е. препятствующие протеканию реакций окисления, разложения и т. д.
Синтетические смолы на основании их свойств и условий переработки делятся на две группы:
I. Термопластичные смолы, которые при нагревании переходят в эластичное, затем в вязко-текучее состояние, после охлаждения они снова затвердевают. Нагревание и охлаждение этих смол не вызывают изменений в их структуре, т. к. нагревание и охлаждение не сопровождаются какими-либо реакциями.
II. Термореактивные смолы при нагревании вследствие протекающих химических реакций подвергаются сильным изменениям. В частности, они перестают размягчаться при повторном нагревании.
Синтетические смолы получаются несколькими методами, основанными на реакциях полимеризации, поликонденсации, сополимеризации, привитой полимеризации и блок-полимеризации.
Наиболее распространенные поликонденсационные смолы
Смолы | Исходные мономеры |
Феноло-формальдегидные | Фенол С6Н5ОН и формальдегид СН2О |
Мочевино-формальдегидные | Мочевина СО(NH2)2 и формальдегид СН2О |
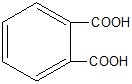
Алкидные (полиэфирные) | Многоосновные кислоты, например фталевая кислота
и многоатомные спирты, например глицерин СН2ОН – СНОН – СН2ОН |
Полиамидные | Многоосновные кислоты, например адипиновая кислота НООС – (СН2)4 – СООН и амины, например гексаметилендиамин
|
Кремнийорганические | Моно - и диметилсиликонхлориды
|
Скорость и направление реакций поликонденсации, а также состав и характер получаемых соединений зависят от соотношения реагирующих веществ и их свойств, количества функциональных групп, поверхности соприкосновения реагирующих веществ, температуры, интенсивности отвода образующихся побочных продуктов и характера применяемого катализатора.
Фенолформальдегидные смолы получаются при поликонденсации в растворе, т. к. мономеры (фенол и формальдегид) находятся в водной среде. Катализатор растворим в реакционной среде (гомогенный катализ). Протекает в более мягких температурных условиях, не требует применения вакуума и инертного газа. Данная реакционная система гомогенная только вначале, а затем образуется гетерогенная система (две несмешивающиеся жидкости: более тяжелый олигомерный слой и водная фаза – надсмольная вода). В состав водной фазы входят, кроме воды, не вступившие в реакцию фенол, формальдегид и растворимые продукты конденсации. После разделения слоев поликонденсация продолжается. Поэтому синтез проводят при энергичном перемешивании, и, чем он продолжительнее, тем полнее связываются фенол и формальдегид, тем больше выход смолы и ее средняя молекулярная масса. Реакция фенола и формальдегида – это низкотемпературная (ниже температуры 373 К) неравновесная (необратимая) поликонденсация, при которой выделяющаяся в ходе процесса вода оказывает небольшое влияние на равновесие и скорость процесса. Поэтому синтез проводят без вывода из сферы реакции низкомолекулярного продукта.
В зависимости от соотношения фенола и формальдегида получаются так называемые новолачные и резольные смолы.
Новолачные смолы образуются при небольшом избытке фенола (на 7 моль фенола берется 6 моль формальдегида). В качестве катализатора применяется соляная, а иногда и щавелевая кислота. Образующиеся олигомеры преимущественно линейного строения. Такие термопластичные олигомеры, сохраняющие при длительном хранении и нагревании до температуры 473 К плавкость и растворимость, называются новолачными смолами или новолаками.
При поликонденсации первоначально образуются фенолоспирты, которые затем реагируют с фенолом, превращаясь в диоксидифенилметаны. Эти соединения далее взаимодействуют с СН2О и фенолоспиртами. Дальнейший рост линейной цепи происходит в результате последовательного присоединения и конденсации. Общее уравнение поликонденсации в кислой среде:
(n + 1)С6Н5ОН + nСН2О → Н – [– С6Н3 (ОН) – СН2 –]n –С6Н5ОН + nН2О,
где n = 4 – 8
При поликонденсации фенола с молярным избытком формальдегида в щелочной среде получаются термореактивные олигомеры. Такие олигомеры, которые при нагревании или на холоде в присутствии кислот и оснований переходят в неплавкое и нерастворимое состояние (резит), называются резольными смолами или резолами. Они представляют собой смесь линейных и разветвленных полимергомологов, для которых характерно наличие реакционноспособных метилольных групп. Содержание этих соединений и степень разветвленности цепей возрастает с увеличением избытка СН2О в реакционной смеси. Процесс образования резолов протекает так же, как и новолаков, через стадию образования фенолоспиртов. Но в щелочной среде дальнейшая конденсация фенолоспиртов между собой или с фенолом протекает медленнее, чем в кислой среде. Поэтому в молекулах олигомеров сохраняется много метилольных групп, способных к дальнейшим превращениям. Общее уравнение поликонденсации в щелочной среде:
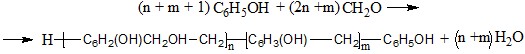
где n – среднее число звеньев, содержащих метиольные группы, n = 2 – 5; m - среднее число звеньев, не содержащих метиольные группу, (n + m + 1) = от 4 до 10.
3. Экспериментальная часть
Химические реактивы, посуда, приборы
- Фенол Формалин (40% - ный раствор формальдегида в воде) Соляная кислота (с = 1,19 · 103 г/см3) Этиловый спирт или ацетон Аммиак 25% - ный раствор или 40% - ный раствор гидроксида натрия Уротропин (гексаметилентетрамин) Круглодонная колба Фарфоровая чашка Водяная баня Ступка с пестиком Металлическая плита (размеры 1,5 х 10 х 10 см) Стеклянная палочка Секундомер
Порядок проведения эксперимента
Получение новолачной смолы
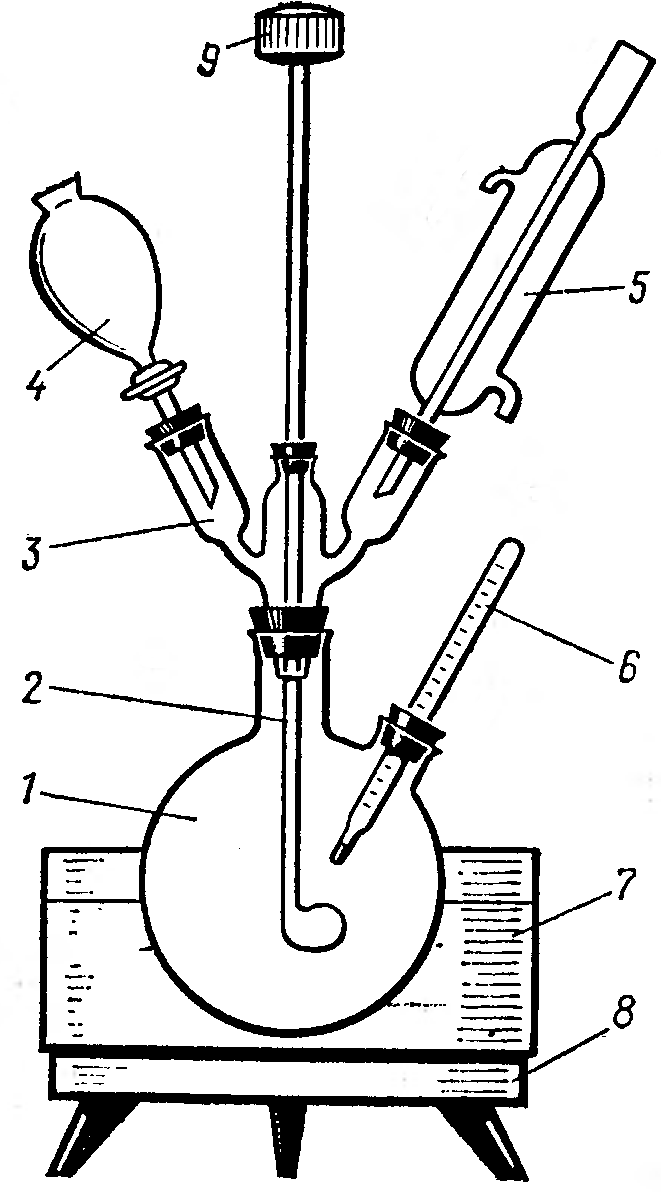
Поликонденсация. В круглодонную колбу емкостью 50 мл помещают 7,5 г фенола и 5 мл 40% - ного раствора формальдегида (рис. 11.1).
|
Рис. 11.1. Прибор для синтеза смол: 1-колба, 2-мешалка, 3-крестовина, 4-капельная воронка, 5-обратный холодильник, 6-термометр, 7-водяная баня, 8-электрическая плитка, 9-мотор |
Смесь взбалтывают до растворения фенола. После полного растворения в раствор вводят катализатор (2 – 3 капли соляной кислоты). Колбу с реакционной смесью закрывают пробкой с вставленным в нее обратным холодильником и осторожно нагревают до кипения (на водяной бане) и процесс проводят при температуре 371 – 373 К. Через 20 – 30 минут от начала кипения раствор мутнеет и расслаивается. Перемешивание продолжают еще 10 – 15 минут. Смесь выливают в предварительно взвешенную фарфоровую чашку. После отстаивания верхний слой, надсмольную воду сливают осторожно в специальную емкость (запрещается выливать в раковину!). Смолу промывают теплой водой до нейтральной реакции по метиловому оранжевому.
Сушка смолы. Для высушивания смолы чашку помещают в сушильный шкаф и нагревают до 180 – 200 0С. После охлаждения для определения выхода продукта на взятый фенол и формальдегид чашку со смолой взвешивают.
Для установления линейного строения полимера 1 г полученного вещества измельчают, помещают в пробирку, приливают 10 мл этилового спирта или ацетона и нагревают. Смесь взбалтывают через каждые 5 – 10 минут в течение 1 – 1,5 часа. Смолы, имеющие линейные структуру, растворяются.
|
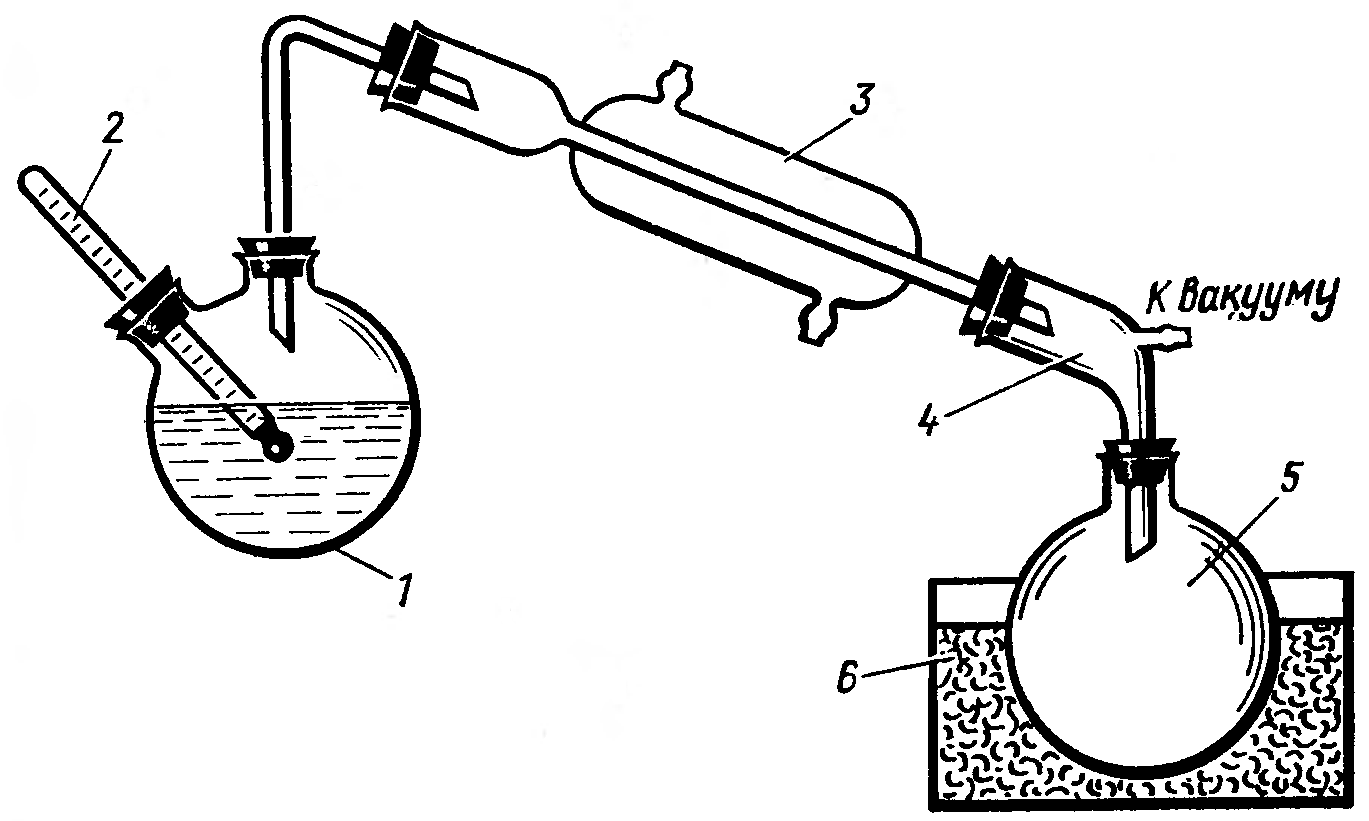
Рис. 11.2. Прибор для сушки смолы: 1-колба, 2-капилляр,3-холодильник, 4- аллонж с отводом, 5-приемник, 6-баня со льдом. |
Определение скорости отверждения. Отверждение новолачных смол проводят на металлической плите, помещенный на электрическую плитку и нагретой до температуры 433 К. 0,5 г измельченной в поршок смолы предварительно смешивают в ступке с уротропином (СН2)6N4 (~ 15% от массы смолы), а затем помещают на плиту так, чтобы площадь соприкосновения была не больше 1 см2. Как только порошок перенесен, его начинают перемешивать стеклянной палочкой и замечают время по секундомеру. За конец отверждения принимают то время, когда смола перестанет тянуться за палочкой и образуется твердая корка.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 |