t, мин | 0 | 20 | 40 | 60 | 80 | 120 | 140 | 160 | 180 | 200 |
cA, моль/м3 | 796 | 478 | 299 | 185 | 116 | 45 | 28 | 18 | 11 | 7 |
2. Реакция омыления пропилацетата щелочью относится к реакциям второго порядка. По данным, приведенным в таблице, определите величины констант скоростей этой реакции при указанных температурах и энергию активации.
283 К | 293 К | ||
Время, | 0 | 18 | 18 |
Концентрация эфира, | 50 | 27,6 | 23 |
Концентрация щелочи, | 30 | 7,6 | 3 |
3. Определите величины констант скоростей прямой и обратной реакций
транс-CHCl=CHCl D цис –CHCl=CHCl
при 573 К на основании данных о концентрации транс-CHCl=CHCl в различные моменты времени
Время, с | 0 | 500 | 1500 | ∞ |
Концентрация, % | 95 | 84,6 | 76,2 | 41,9 |
4. Запишите уравнения ионных равновесий, найдите концентрацию всех типов частиц и рассчитайте величину рН
а) в водном растворе миндальной кислоты, концентрации 10 моль/м3;
б) в водном растворе фтористого калия, концентрации 0,005 моль/л.
5. Определите при 298 К растворимость бромида серебра
а) в воде; б) в водном растворе нитрата калия, 0,1 моль/л;
в) в водном растворе бромида калия 0,2 моль/л.
6. При 298 К удельное сопротивление водного раствора пропионовой кислоты (концентрации 0,004 моль/л) составляет 113,6 Ом·м. Рассчитайте константу ионизации кислоты и сравните ее со справочными данными.
7. Схематичное изображение двух электродов приведено ниже:
Pb, PbCl2 çCl - Cu+çCu
![]() 0,5 моль/л
0,5 моль/л ![]() = 0,1 моль/л
= 0,1 моль/л
Укажите, к какому типу они относятся, составьте из них гальванический элемент, запишите уравнения электродных реакций и итоговую реакцию. Вычислите при 298 К электродвижущую силу гальванического элемента.
Рейтинговое домашнее задание
1. Для гомогенной реакции A1 + A2 +A3 = B дана зависимость концентрации вещества A1 ( в моль/м3 ) от времени ( в мин) при начальных концентрациях A2 и A3 значительно превышающих начальную концентрацию вещества A1 .
Постройте кинетическую кривую 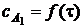 и определите по ней дифференциальным методом частный порядок реакции по веществу A1 и эффективную константу скорости реакции.
и определите по ней дифференциальным методом частный порядок реакции по веществу A1 и эффективную константу скорости реакции.
Время, мин | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 |
Концентрация, моль/м3 | 250 | 160 | 95 | 69 | 50 | 27 | 9 | 1 |
2. Для реакции, протекающей в газовой фазе при постоянном объеме, согласно стехиометрическому уравнению A = B + C + D дана зависимость общего давления газовой смеси от времени.
t, мин | 0 | 5 | 10 | 15 | 20 |
p, Па | 41000 | 52100 | 61670 | 69950 | 77110 |
Полагая, что реакция описывается уравнением первого порядка, выразите константу скорости реакции через общее давление и рассчитайте ее величину.
3. Найдите константу Михаэлиса и максимальную скорость гидролиза аденозинтрифосфата, катализируемого миозином по данным о начальной скорости гидролиза wo, моль/(л×с) от концентрации субстрата ![]() , моль/л.
, моль/л.
wo×105, моль/(л×с) | 0,18 | 0,13 | 0,08 | 0,05 | 0,02 |
| 0,09 | 0,024 | 0,009 | 0,004 | 0,0015 |
4. Постройте и проанализируйте распределительную диаграмму фосфорной кислоты.
5. По значениям стандартных условных электродных потенциалов вычислите при 298 К а) величину произведения растворимости 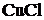 и б) величину константы нестойкости комплексного иона
и б) величину константы нестойкости комплексного иона  . Запишите схему электрохимической цепи, уравнения электродных реакций и итоговую реакцию.
. Запишите схему электрохимической цепи, уравнения электродных реакций и итоговую реакцию.
6. При 300 К был составлен гальванический элемент
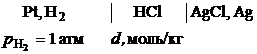
и при различных значениях концентрации раствора соляной кислоты (d,моль/кг) измерена его ЭДС (Е, В). Найдите по этим данным величину среднего ионного коэффициента активности в растворе соляной кислоты концентрации 0,008 моль/кг.
моль/кг | 0,001 | 0,002 | 0,005 | 0,01 | 0,02 | 0,05 | 0,1 | 0,2 | 0,5 |
E, В | 0,579 | 0,544 | 0,498 | 0,464 | 0,429 | 0,385 | 0,351 | 0,318 | 0,271 |
Вариант 21
Обязательное домашнее задание
1. Для гомогенной реакции, протекающей согласно стехиометрическому уравнению 2A ® B имеются данные по зависимости концентрации вещества A (в моль/м3) от времени (в мин). Постройте кинетическую кривую cA = f(t). Определите графически по кинетической кривой, а также по зависимостям в соответствующих координатах (интегральным методом), к какому порядку – первому или второму, относится данная реакция, определите величину константы скорости реакции и время полупревращения.
t, мин | 0 | 20 | 40 | 60 | 80 | 100 | 140 | 160 | 180 | 200 |
cA,моль/м3 моль/м3 | 992 | 620 | 395 | 247 | 156 | 99 | 40 | 25 | 16 | 10 |
2. Реакция омыления пропилацетата щелочью относится к реакциям второго порядка. По данным, приведенным в таблице, определите величины констант скоростей этой реакции при указанных температурах и энергию активации.
283 К | 293 К | ||
Время, | 0 | 20 | 20 |
Концентрация эфира, | 50 | 26,8 | 22,5 |
Концентрация щелочи, | 30 | 6,8 | 2,5 |
3. Определите величины констант скоростей прямой и обратной реакций
транс-CHCl=CHCl D цис –CHCl=CHCl
при 573 К на основании данных о концентрации транс-CHCl=CHCl в различные моменты времени
Время, с | 0 | 200 | 1200 | ∞ |
Концентрация, % | 95 | 90 | 78 | 41,9 |
4. Запишите уравнения ионных равновесий, найдите концентрацию всех типов частиц и рассчитайте величину рН

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |




