Федеральное агентство по образованию
ГОУ ВПО «Уральский государственный технический университет - УПИ»
ФИЗИЧЕСКАЯ ХИМИЯ
Сборник задач домашних заданий
по курсам «Физическая химия (2 часть)» и «Экспериментальное исследование физико-химических закономерностей»
для студентов химико-технологического факультета
и факультета строительного материаловедения
Екатеринбург 2007
УДК 544(076)С79
Составитель:
Научный редактор доц., к. х.н.
Физическая химия. Сборник задач домашних заданий по курсам «Физическая химия» (2 часть) и «Экспериментальное исследование физико-химических закономерностей»: сборник задач для студентов химико-технологического факультета и факультета строительного материаловедения / - Екатеринбург: ГОУ ВПО УГТУ-УПИ, 2007. 75с
В данном пособии приведено 24 варианта домашних заданий для студентов химико-технологического факультета и факультета строительного материаловедения по двум курсам: «Физическая химия» (2 часть) и «Экспериментальное исследование физико-химических закономерностей». В каждом варианте имеется 13 задач, которые составляют два домашних задания по физической химии (одно по химической кинетике, второе по электрохимии) и одно задание по курсу «Экспериментальное исследование физико-химических закономерностей». Точное указание, к какому именно домашнему заданию относится каждая задача приведено в начале сборника. Кроме того, все задачи разделены по уровню сложности на два больших класса: первый – обязательный для решения, второй – желательный, содержащий более сложные задачи. Соответственно этому делению полное домашнее задание разделено на ОДЗ (обязательное домашнее задание) и РДЗ (рейтинговое домашнее задание).
Указаны требования к оформлению домашнего задания, ссылки на использованную литературу.
Библиогр.: 5 назв.
Подготовлено кафедрой «Физическая и коллоидная химия».
© ГОУ ВПО Уральский государственный
технический университет – УПИ, 2007
Пояснения к домашним заданиям
Соответствие задач типу домашнего задания приведено ниже.
Химическая кинетика (ДЗ-1) | Электрохимия (ДЗ-2) | Экспериментальное исследование физико-химических закономерностей | ||||
ОДЗ | РДЗ | ОДЗ | РДЗ | ОДЗ | РДЗ | |
Номера задач | 1; 2 | 2; 3 | 4; 5: 7 | 4; 5 | 3; 6 | 1; 6 |
Сборник задач предназначен для самостоятельной работы студентов по усвоению материала курса физической химии. Начинать работу нужно с решения задач обязательного домашнего задания (ОДЗ). Решение обязательного домашнего задания вместе с отчетами по прохождению лабораторных работ является допуском до экзамена по физической химии. При оформлении решений задач ОДЗ учтите, что задачи можно сдавать по мере решения каждой задачи, а не все задачи единовременно, поэтому оформлять их лучше на отдельных листах из тетради, а не в целой тетради. Вместо условия задач можно приложить ксерокопию варианта домашнего задания. Краткое условие задачи обязательно. Расчет производится в СИ.
Для углубленного изучения курса нужно решить рейтинговое домашнее задание (РДЗ). В этом виде домашнего задания сгруппированы более сложные задачи, требующие пояснений при решении, графических отображений зависимостей, анализа полученных результатов.
Требования к оформлению этого вида задания (РДЗ).
1. Рейтинговое домашнее задание сдается на проверку целиком.
2. Запись решения задач осуществляется на листах бумаги формата А4, с одной стороны листа. Листы не сшиваются, и без всяких скрепок сдаются преподавателю на проверку в файл-папке.
3. Титульного листа не делается, однако на каждом листе сверху (2 см) проводится горизонтальная черта, над которой указывается необходимая информация: Например, гр. Х-359, РДЗ - 4, задача 3, лист 2.
(РДЗ-4 – означает 4 вариант рейтингового домашнего задания, лист 2 - обозначает номер листа, соответствующего решению 3 задачи, а не общее количество листов).
4. Допускается полное условие задачи приводить в виде ксерокопии домашнего задания Вашего варианта. Краткое условие задачи обязательно.
5. В начале решения нужно привести необходимые уравнения и формулы с пояснениями обозначений величин и смысла формул. Уравнения нужно пронумеровать. Уместны словесные связки между формулами, чтобы была понятна логика решения задачи. Искомые величины нужно найти в общем виде в буквенных обозначениях. При подстановке данных обязательно получение необходимых размерностей. Во все расчетные формулы должны входить только те величины, которые заданы в условии.
6. Рисунки выполняются с использованием чертежных принадлежностей на миллиметровой бумаге. На плоскости рисунка допускается лишь цифровое или буквенное обозначение линий (если их больше одной) и необходимые для решения задачи графические построения. Названия рисунков и расшифровка обозначений приводятся внизу. Нумерация уравнений, таблиц и рисунков относится непосредственно к решаемой задаче.
Решение рейтингового домашнего задания является необходимым условием получения студентом экзаменационной оценки досрочно, до сессии.
Вариант 1
Обязательное домашнее задание
1. Для гомогенной реакции, протекающей согласно стехиометрическому уравнению 2A ® B имеются данные по зависимости концентрации вещества A (в моль/м3) от времени (в мин). Постройте кинетическую кривую cA = f(t). Определите графически по кинетической кривой, а также по зависимостям в соответствующих координатах (интегральным методом), к какому порядку – первому или второму, относится данная реакция, определите величину константы скорости реакции и время полупревращения.
t, мин | 0 | 20 | 40 | 60 | 80 | 100 | 140 | 160 | 180 | 200 |
cA,моль/м3 моль/м3 | 992 | 620 | 395 | 247 | 156 | 99 | 40 | 25 | 16 | 10 |
2. Реакция омыления этилацетата щелочью относится к реакциям второго порядка. По данным, приведенным в таблице, определите величины констант скоростей этой реакции при указанных температурах и энергию активации.
273 К | 293 К | ||
Время, | 0 | 5 | 5 |
Концентрация эфира, | 25 | 20,1 | 11,2 |
Концентрация щелочи, | 40 | 35,1 | 26,2 |
3. Реакция изомеризации этилбензола протекает при 600 К и 1 атм по схеме:
![]() м- ксилол
м- ксилол
этилбензол о- ксилол
п - ксилол
Через 5 секунд от начала опыта определены концентрации всех присутствующих в системе веществ, моль/л: этилбензол – 22; м-ксилол – 4,8;
о-ксилол - 11,5; п-ксилол – 4,2. Найдите величины констант скоростей каждой из стадий этой параллельной реакции.
4. Запишите уравнения ионных равновесий, найдите концентрацию всех типов частиц и рассчитайте величину рН
а) в водном растворе уксусной кислоты, концентрации 10 моль/м3;
б) в водном растворе цианистого калия, концентрации 0,01 моль/л.
5. Определите при 298 К растворимость сульфата серебра
а) в воде; б) в водном растворе нитрата калия, 0,1 моль/л;
в) в водном растворе азотнокислого серебра 0,2 моль/л.
6. Удельное сопротивление водного раствора трихлоруксусной кислоты (концентрации 0,001 моль/л) при 298 К составляет 26,38 Ом·м. Рассчитайте константу ионизации кислоты и сравните ее со справочными данными.
7. Схематично изображены два электрода.
Sn4+,Sn2+çPt Zn2+çZn
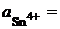 0,1 моль/.л;
0,1 моль/.л; ![]() 0,5 моль/л
0,5 моль/л 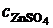 = 0,01 моль/л
= 0,01 моль/л
Укажите, к какому типу относится каждый из них, составьте из них гальванический элемент, запишите уравнения электродных реакций и итоговую реакцию. Вычислите при 298 К ЭДС гальванического элемента.
Рейтинговое домашнее задание
1. Для гомогенной реакции A1 + A2 +A3 = B дана зависимость концентрации вещества A1 ( в моль/м3 ) от времени ( в мин) при начальных концентрациях A2 и A3 значительно превышающих начальную концентрацию вещества A1 .
Постройте кинетическую кривую 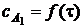 и определите по ней дифференциальным методом частный порядок реакции по веществу A1 и эффективную константу скорости реакции.
и определите по ней дифференциальным методом частный порядок реакции по веществу A1 и эффективную константу скорости реакции.
Время, мин | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 87 |
Концентрация, моль/м3 | 235 | 188 | 144 | 103 | 70 | 43 | 25 | 1 |
2. Для реакции, протекающей в газовой фазе при постоянном объеме, согласно стехиометрическому уравнению A = B + C + D дана зависимость общего давления газовой смеси от времени.
t, мин | 0 | 5 | 10 | 15 | 20 |
p, Па | 40000 | 49800 | 58360 | 65870 | 72470 |
Полагая, что реакция описывается уравнением первого порядка, выразите константу скорости реакции через общее давление и рассчитайте ее величину.
3. Известны начальные скорости wo, моль/(л×с) разложения гидроперекиси тетралина под действием фермента на субстрат для ряда концентраций субстрата ![]() , моль/л. Найдите константу Михаэлиса и максимальную скорость каталитического разложения гидроперекиси тетралина по этим данным
, моль/л. Найдите константу Михаэлиса и максимальную скорость каталитического разложения гидроперекиси тетралина по этим данным
wo×105, моль/(л×с) | 4,2 | 3,7 | 2,8 | 2,4 | 1,6 |
| 0,840 | 0,185 | 0,070 | 0,048 | 0,023 |
4. Постройте и проанализируйте распределительную диаграмму борной кислоты.
5. По значениям стандартных условных электродных потенциалов вычислите при 298 К а) величину произведения растворимости 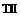 и б) величину константы нестойкости комплексного иона
и б) величину константы нестойкости комплексного иона 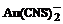 . Запишите схему электрохимической цепи, необходимой для вычислений, уравнения электродных реакций и итоговую реакцию.
. Запишите схему электрохимической цепи, необходимой для вычислений, уравнения электродных реакций и итоговую реакцию.
6. При 300 К был составлен гальванический элемент
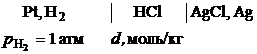
и при различных значениях концентрации раствора соляной кислоты (d,моль/кг) измерена его ЭДС (Е, В). Найдите по этим данным величину среднего ионного коэффициента активности в растворе соляной кислоты концентрации 0,007 моль/кг.
d,моль/кг | 0,002 | 0,005 | 0,01 | 0,02 | 0,05 | 0,1 | 0,2 | 0,5 |
E, В | 0,544 | 0,498 | 0,464 | 0,429 | 0,385 | 0,351 | 0,318 | 0,271 |
Вариант 2
Обязательное домашнее задание
1. Для гомогенной реакции, протекающей согласно стехиометрическому уравнению 2A ® B имеются данные по зависимости концентрации вещества A (в моль/м3) от времени (в мин). Постройте кинетическую кривую cA = f(t). Определите графически по кинетической кривой, а также по зависимостям в соответствующих координатах (интегральным методом), к какому порядку – первому или второму, относится данная реакция, определите величину константы скорости реакции и время полупревращения.
t, мин | 0 | 10 | 30 | 50 | 70 | 90 | 110 | 130 | 150 | 170 |
cA,моль/м3 моль/м3 | 898 | 639 | 424 | 268 | 167 | 105 | 67 | 40 | 26 | 16 |
2. Реакция омыления этилацетата щелочью относится к реакциям второго порядка. По данным, приведенным в таблице, определите величины констант скоростей этой реакции при указанных температурах и энергию активации.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |




