магний гидроксонитрата: МgOHNO3 → MgOH+ + NO3¯
MgOH+ ↔ Мg2+ + OH-
Задание 4. Закончить уравнения реакций и назвать продукты:
а) 2NH3 + H2SO4 ® (NH4 )2SO4 в) N2O5 + CaO ® Ca(NO3)2
аммоний сульфат кальций нитрат
б)AlCl3+3AgNO3® Al(NO3)3+3AgCl; г) Cr(OH)3+NaOH® NaCrO2+2H2O
алюминий серебро метахромит вода
нитрат хлорид натрия
Задание 5. Найти массу, объем, число молекул, которые содержатся в 5 моль N2.
Решение:
М(N2)=28г/моль; V=Vm∙n=22,4∙5=112л; m=M∙n=28∙5=140г;
Nмол=NA∙n=6,02∙ 1023 ∙5=3,1∙1024молекул.
Задание 6.Рассчитать молярные массы эквивалентов:
а) в соединениях: CrO3: Мэкв(CrO3 )= 52∙1/6+16∙1/2=16,7г/моль;
Mn(OH4): Мэкв( 1/4Mn( OH)4 )= 123∙1/4=30,7г/моль;
HNO2: Мэкв(HNO2)=1∙47=47г/моль;
Ca3(PO4)2 : Мэкв(1/6 Ca3(PO4)2)= 310∙1/6=51,7г/моль.
б) по реакции: N2O5 + Ca(OH)2 ® Ca(NO3)2 + 2H2O
Мэкв(1/2N2O5)= 108∙1/2=54г/моль
Задание 7. Получить и назвать соли, которые образуются при взаимодействии Fe(OH)2 и HNO2.
Ответ:Fe(OH)2 + HNO2 → FeOHNO2 + H2O
железо(11) гидроксонитрит;
Fe(OH)2 +2HNO2 → Fe(NO2)2 + 2H2O
железо(11) нитрит.
Задание 8. задача. Неизвестный металл растворили в избытке соляной кислоты, в результате чего образовалась соль массой 27,2г и выделился газ, объем которого при температуре 19°С и давлении 104 кПа составил 4,65л. Определить металл и вычислить значение его массы.
решение.
с соляной кислотой с выделением газа Н2 реагируют металлы, которые в электрохимическом ряду напряжений находятся до водорода.
Найдём объём выделившегося газа при нормальных условиях по формуле объединенного газового закона Бойля-Мариотта и Гей-Люссака:
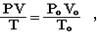
где Рo, Vo, Тo - давление, объём газа и температура при нормальных условиях (Рo = 101,3 кПа, Тo = 273К).
104 ∙ 4,65/(273+19) = 101,3 ∙ Vo /273; Vo = 4,46л.
По закону эквивалентов: отношения масс веществ вступивших в реакцию прямо пропорционально отношению молярных масс (или объёмов) их эквивалентов:
m1/m2 = Mэкв1/ Mэкв2.
Эквивалентный объём водорода равен 11,2 л/моль. Молярная масса эквивалента хлорида металла равна 35,5 + Mэкв ме
27,2/4,46 = (35,5 + Mэкв ме) / 11,2; Mэкв ме = 32,5 г/моль
Найдём малярную массу металла.
Если валентность металла равна 1, то М = 1∙32,5 = 32,5 г/моль такого металла нет.
Если валентность металла равна 2, то М = 2∙32,5 = 65 г/моль это цинк.
Zn + 2HCl → ZnCl2 + H2
найдём массу растворённого металла 4,46∙65/22,4 = 12,94г.
Ответ: металл цинк, М(Zn) = 65г/моль.
Задание 9. Задача. Неизвестное серосодержащее вещество массой 0,222г сожгли в избытке кислорода, в результате чего образовались углекислый газ массой 0,396г и вода массой 0,162г. Вся сера, содержащаяся в исходном веществе массой 0,074 г, была переведена полностью в сульфат бария, масса которого оказалась равной 0,1165 г. Определить молекулярную формулу исходного вещества, если относительная плотность его паров по воздуху равна 5,1.
Решение:
Уравнение горения газообразного соединения Х:
SХ + О2 → СО2 + Н2О + SO2.
1) Найдём молярную массу вещества М= 5,1∙29= 148г/моль
2) Найдем состав вещества:
x 0,396г y 0,162г z 0,1165г
С → СО2 2Н → Н2О S → BaSO4
12 г/моль 44 г/моль 2 18 г/моль 32 г/моль 233 г/моль
x = 0,108г С y= 0,018г Н z= 0,016г S
в 0,074г вещества
пересчитаем содержание серы на 0,222г вещества: 0,222∙0,016/0,074=0,048г S
Найдем массу элементов: 0,108 + 0,018 + 0,048 = 0,174г. Масса элементов меньше, чем масса вещества, поэтому в состав ещё входит кислород. m(O) = 0,222 – 0,174 = 0,048г.
3) Найдём мольные соотношения элементов: CxHySzOn
x : y : z : n = 0,108/12 : 0,018/1 : 0,048/32 : 0,048/16 =
= 0,009 : 0,018 : 0,0015 : 0,003 = 6 : 12 : 1 : 2
Получим простейшую формулу C6H12SO2
4) Найдём молярную массу М(C6H12SO2) = 6∙12+12∙1+32+2∙16= 148г/моль. соответствует молярной массе истинной формуле
Ответ: молекулярная формула исходного вещества C6H12SO2.
Задание 10. Осуществить превращения:
углерод ® оксид углерода(IV) ® магний гидрокарбонат ® магний карбонат ® оксид углерода(IV) ® оксид углерода(II)
1) C + О2 ® CO2
2) 2CO2 + Mg(OH)2 ® Mg(HCO3)2
3) Mg(HCO3)2 + Ca(OH)2 ® MgCO3 + CaCO3 + 2H2O
4) MgCO3 ® CO2 + MgO
5) CO2 + C ® 2CO
ВАРИАНТ 1
1. Закон кратных отношений.
2. Химические свойства основных оксидов.
3. Написать диссоциацию следующих соединений:
а) барий гидроксида, б) азотной кислоты, в) натрий карбоната,
г) кальций гидроксохлорида, д) калий гидросульфида.
4. Закончить уравнения реакций и назвать соединения:
а) AlCl3 + NaOH ® в) Pb(NO3)2+ Na2SO4 ®
б) CaCO3 + HCl ® г) Cr(OH)3 + NaOH®
5. Рассчитать количество моль, объем, число молекул, которое содержится в 10 г H2.
6. Рассчитать молярные массы эквивалентов:
а) в соединениях: Al(NO3)3, NO2, H4P2O7, Ba(OH)2
б) по реакции: SO3+ NaOH ® NaHSO4.
7. Получить и назвать все соли, которые образуются при взаимодействии Fе(OH)2 и H3PO4..
8. Рассчитать молярную массу эквивалента неметалла и определить неметалл, его массовая доля в оксиде равна 50%.
9. Оксид неизвестного металла массой 0,80 г превратили в сульфат этого же металла массой 2,68 г. Рассчитать массу хлорида металла, который можно получить из исходного оксида массой 5 г.
10. Осуществить превращения: цинк ® цинкат натрия ® гидроксид цинка ® хлорид цинка.
ВАРИАНТ 2
1. Закон Авогадро
2. Химические свойства кислотных оксидов.
3. Написать диссоциацию следующих соединений:
а) аммоний гидроксида, б)серной кислоты, в)барий нитрата,
г) железо(II) гидроксобромида, д) натрий дигидрофосфата.
4. Закончить уравнения и назвать соединения:
а) BaCl2 + H2SO4 ® в) Na2CO3 + HNO3 ®
б) Al 2O3 + KOH ® г) H2O + Cl2O5 ®
5. Рассчитать число молекул, массу и объем в 2 моль O2 .
6. Рассчитать молярные массы эквивалента:
а) в соединениях: CuSO4 , Cr 2 O3, HNO3 , Al(OH)3
б) по реакции: SO2 + 2NaOH® Na2SO3+ H2O.
7. Получить и назвать все соли, которые образуются при взаимодействии KOH и H3PO4 .
8. Определить формулу вещества и его молярную массу, в котором содержится 16,09% натрия, 4,19% углерода, 6,99% водорода и 72,73% кислорода.
9. Смесь метана, угарного газа и этана общим объемом 100 мл (н. у.) сожгли в избытке кислорода, в результате чего образовались углекислый газ объемом 160 мл (н. у.) и вода массой 0,161г. Вычислить плотность этой смеси.
10. Осуществить превращения: свинец (II)оксид ® плюмбит натрия ® свинец (II) нитрат ® свинец (II) гидроксид.
ВАРИАНТ 3
1. Закон сохранения массы и энергии.
2. Химические свойства амфотерных оксидов.
3. Написать диссоциацию следующих соединений:
а) алюминий сульфата, б) ортофосфорной кислоты, в) натрий гидроксида,
г) калий гидросульфида, д) магний гидроксохлорида.
4. Закончить уравнения реакций и назвать соединения:
а) BeO + Ba(OH)2 ® в) Na + H2O ®
б) NaOH + H3AsO4 ® г) Ca(OH)2 ®t
5. Рассчитать массу, число моль и объем, если имеется 3,01×1023молекул N2.
6. Рассчитать молярные массы эквивалентов:
а) в соединениях: P2O5, H2SO4, Ca(ClO4)2, Cu(OH)2
б) по реакции: BaO + SO3 ® BaSO4.
7. Получить и назвать все соли, которые образуются при взаимодействии Ca(OH)2 и H2SO4.
8. Определить формулу вещества и его молярную массу, в котором содержится 16,09% натрия, 4,19% углерода, 6,99% водорода и 72,73% кислорода.
9. Смесь метана, угарного газа и этана общим объемом 100 мл (н. у.) сожгли в избытке кислорода, в результате чего образовались углекислый газ объемом 160 мл (н. у.) и вода массой 0,161г. Вычислить плотность этой смеси.
10. Осуществить превращения: свинец (II)оксид ® плюмбит натрия ® свинец (II) нитрат ® свинец (II) гидроксид.
Лабораторная работа
“Определение молярной массы эквивалента металла
методом вытеснения водорода из кислоты”
Этот метод применяется для определения молярных масс эквивалентов тех металлов, которые способны вытеснять водород из разбавленных кислот и щелочей.
Приборы и реактивы: прибор для определения молярной массы эквивалента металла, термометр, барометр, мерный цилиндр на 25 мл, навеска металла, соляная кислота (10%-ный раствор).

Рис. 1. 1.Прибор для определения молярной массы эквивалента металла
Прибор для определения молярной массы эквивалента металла методом вытеснения водорода из кислоты состоит из пробири1и двух бюреток 2 и 3, заполненных наполовину водой и соединенных внизу резиновой трубкой (рис.1.1.).
Перед началом работы необходимо испытать прибор на герметичность. Для этого, плотно закрыв пробирку 1 и бюретку 2, необходимо опустить бюретку 3 так, чтобы уровень жидкости в ней был ниже, чем в бюретке 2, и закрепить бюретку 3. Если в течение 1-2 мин уровень воды в бюретках будет неподвижен, то прибор герметичен, можно приступать к работе.
В пробирку 1 налить 5-б мл 10%-ного раствора соляной кислоты и внести в нее навеску металла, завернутую в бумагу. Навеска металла не должна касаться кислоты. Установить бюретку так, чтобы положения нижнего мениска воды в бюретках были на одном уровне (глаз должен находиться на одной прямой с мениском). Записать положения мениска в бюретке 2. Затем наклонить пробирку 1, чтобы металл упал на дно. Наблюдать выделение водорода и вытеснение воды из бюретки 2 в бюретку 3. По окончании реакции следует подождать 5-8 мин, пока газ примет комнатную температуру. После этого привести воду в бюретках к одному уровню, т. е. создать в бюретке 2 давление, равное атмосферному. По положению нижнего мениска воды в бюретке 2 определить и записать объем выделившегося водорода, который равен разности двух отсчетов до и после реакции металла с кислотой. Записать условие опыта: температуру и барометрическое давление.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 |



