Положительное значение φ° имеют окислительно-восстановительные пары, в которых окисленная форма присоединяет электроны легче, чем катион водорода в эталонной паре. Отрицательное значение φ° имеют окислительно-восстановительные пары, в которых окисленная форма присоединяет электроны труднее, чем Н+ в эталонной паре. Следовательно, чем больше (т. е. положительнее) значение φ° данной сопряженной окислительно-восстановительной пары, тем сильнее выражены ее окислительные свойства, а восстановительные свойства - соответственно слабее.
В основе определения направления самопроизвольного протекания окислительно-восстановительных реакций лежит следующее правило: окислительно-восстановительные реакции самопроизвольно протекают всегда в сторону превращения сильного окислителя в слабый сопряженный восстановитель или сильного восстановителя в слабый сопряженный окислитель. Суть окислительно-восстановительных реакций заключается в конкуренции за присоединение электрона между участвующими окислителями. При этом электрон присоединяет та сопряженная пара, окисленная форма которой сильнее его удерживает. Это отражает следующая схема:
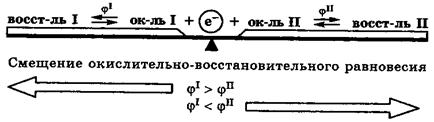
Сопоставляя потенциалы сопряженных пар, участвующих в окислительно-восстановительной реакции, можно заранее определить направление, в котором будет самопроизвольно протекать та или иная реакция. При взаимодействии двух сопряженных окислительно-восстановительных пар окислителем всегда будет окисленная форма той пары, потенциал которой имеет более положительное значение.
Пример. В реакционной смеси содержатся две сопряженные окислительно-восстановительные пары: I2, I - , φ° (I20, I-) = 0, 54 В; S, H2S, (φ°(S0, H2S-2) = 0, 17 В.
Так как первая пара содержит более сильный окислитель (I2), чем вторая пара (S), то в стандартных условиях самопроизвольно пойдет реакция, в которой окислителем будет I2, а восстановителем H2S: I2 + H2S = 2HI + S.
Для определения направления окислительно-восстановительной реакции можно также пользоваться величиной ее ЭДС. ЭДС окислительно-восстановительной реакции в стандартных условиях (Е°) численно равна разности стандартных потенциалов сопряженных окислительно-восстановителъных пар, участвующих в реакции: Е° = φ°ок -φ°восст .
Условием самопроизвольного протекания окислительно-восстано-вительной реакции является положительное значение ее ЭДС, т. е. Е° = φ°ок - φ°восст >0
С учетом этого условия для самопроизвольно протекающей окислительно-восстановительной реакции значение φ окислительно-восстановительной пары, выступающей окислителем, должно быть больше φ второй окислительно-восстановительной пары, играющей роль восстановителя в данной реакции. Так, в рассмотренном выше примере: Е° = φ°ок- φ°восст = 0,54 - 0,17 = 0,37 В
Если Е°=0, то равновероятно протекание окислительно-восстановительной реакции, как в прямом, так и в обратном правлении, и это является условием возникновения химического равновесия для окислительно-восстановительного процесса. Количественной характеристикой протекания любых обратимых процессов является константа равновесия К, которая связана с изменением стандартной энергии Гиббса следующим соотношением: ∆G°= -2,ЗRТ lg К
С другой стороны, изменение стандартной энергии Гиббса связано с ЭДС окислительно-восстановительной реакции соотношением; ∆G° = - zFE° где F = 96 500 Кл/моль; z-число электронов, принимающих участие в элементарном процессе.
Из этих двух уравнений следует: Е° = (2,ЗRТ lg K)/(zF) или lg К = (zFE°)/(2,3RT).
Пользуясь этими выражениями, можно рассчитать константу равновесия любой окислительно-восстановительной реакции, но реальное значение она будет иметь только для тех реакций, ЭДС которых менее 0,35 В, так как при больших ЭДС реакции рассматриваются как практически необратимые. Поскольку ЭДС отдельных стадий окислительно-восстановительных реакций, протекающих в живых системах, обычно не превышает 0,35 В (| Е°| < 0,35 В), то большинство из них практически обратимы, причем обратимость процесса выражена тем сильнее, чем величина | Е° | ближе к нулю.
Окислительно-восстановительные реакции лежат в основе метаболизма любых организмов. В случае аэробного метаболизма основным окислителем является молекулярный кислород, поступающий в процессе дыхания, а восстановителем - органические соединения, поступающие с продуктами питания. При анаэробном метаболизме в его основе лежат преимущественно окислительно-восстановительные реакции, в которых и окислителями, и восстановителями являются органические соединения.
Параллельно с окислительно-восстановительным процессом могут протекать и другие: протолитический, комплексообразование, образование осадка. Совмещенное редокс-протолитическое равновесие наблюдается в так называемых редокс-системах второго типа, в которых перенос электронов сопровождается переносом протонов. Примеры таких систем:
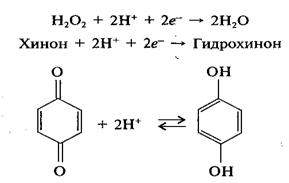
Для расчета редокс-потенциала таких систем используется следующая форма уравнения Нернста:
RT a(Ox)
φ = φ° + ––– 1n ––––––– am (H+)
nF a(Red)
где a(Н+) – активность ионов гидроксония; т – стехиометрический коэффициент перед ионом водорода в полуреакции.
Комплексообразование также в ряде случаев оказывает значительное влияние на величину редокс-потенциала. Влияние лигандного окружения на величину редокс-потенциала объясняется тем, что лиганд связывает окисленную и восстановленную формы по-разному: образующиеся комплексные соединения различаются константами нестойкости.
Измерение электродвижущих сил особым образом составляемых гальванических элементов лежит в основе одного из физико-химических методов анализа – потенциометрии. Потенциометрия – незаменимый во многих случаях метод определения концентрации физиологически активных ионов (Н3О+,K+, Na+, Ca2+, NH4+, Сl–, Вr–, I– и др.) в биологических жидкостях (крови, спинномозговой жидкости и др.) и тканях организма.
Гальванические элементы, используемые в потенциометрии, составляют из измерительного электрода и электрода сравнения. Измерительный электрод должен правильно и воспроизводимо отражать свойства раствора (в частности, активность ионов, концентрации веществ).
Ионно-металлический электрод, представляющий собой металл, опущенный в раствор соли этого металла, функционирует как измерительный электрод. Пример - серебряный электрод Ag | c(Ag+) = х.
В силу многих причин (взаимодействие с водой, образование оксидных пленок и др.) не все металлы могут быть использованы для изготовления электродов, измеряющих активность их катионов. В этом случае часто используют мембранные электроды, способные давать потенциалы, зависящие от активности ограниченного числа ионов, а в некоторых случаях – только одного типа ионов. Такие электроды называют ионоселективными. Примером ионоселективного электрода является стеклянный электрод, потенциал которого зависит от активности ионов Н3О+. Электроды, приготовленные из специальных сортов стекла, могут быть селективны по отношению к ионам натрия, кальция, серебра и др.
Электроды сравнения должны иметь практически постоянный потенциал. Наиболее употребительными электродами сравнения являются каломельный и хлорсеребряный. Потенциалы этих электродов при разных значениях концентрации внутреннего электролита(0,1 моль/л, 1 моль/л, насыщенный раствор) и при разных температурах приводятся в справочниках. Хлорсеребряный электрод представляет собой покрытую слоем хлорида серебра серебряную проволоку, помещенную в раствор хлорида калия. Если в собранном гальваническом элементе измерительный электрод – катод, то хлорсеребряный электрод функционирует как анод: Ag, AgCl | Сl–, с(Сl–) = const || измерительный электрод. В нем протекает полуреакция окисления, в ходе которой образующиеся ионы серебра связываются в малорастворимое соединение: Ag – е– + Сl– → AgCl. Этим предотвращается накопление ионов серебра сверх количества, определяемого растворимостью хлорида серебра в присутствии одноименного иона (постоянство концентрации ионов серебра очень важно, так как от нее зависит потенциал серебряной проволоки, т. е. электрода).
Если же измерительный электрод – анод, то хлорсеребряный электрод функционирует как катод: измерительный электрод || С1–, с(С1–) = const | Ag, AgCl
В нем протекает полуреакция восстановления AgCl + е– →Ag + С1–
Очевидно, что постоянство потенциала хлорсеребряного электрода поддерживает совмещенное редоке-гетерогенное равновесие, а сам электрод можно рассматривать как редокс-гетерогенную буферную систему.
ТЕМА САМОСТОЯТЕЛЬНОЙ РАБОТЫ
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Цель: формирование у студентов знаний об окислительно-восстановительных процессах, электродных потенциалах и ЭДС окислительно-восстановительных реакциях.
Задачи: • изучить методы составления и направление протекания ОВР.
• иметь понятия об электродных потенциалах и гальванических элементах.
• знать условия самопроизвольного и равновесного протекания окислительно-восстановительных реакций.
Методика выполнения блочно-модульных заданий
Задание 1. На теоретические вопросы ответы подготовить по лекциям и учебным пособиям.
Задание 2. Определить степени окисления элементов в соединениях MgCO3, PO33−, ClO3−, (Cl+,Cl+3,Cl+7). Для элемента последней частицы определить окислительно-восстановительные свойства.
Ответ.
Степень окисления – это условный заряд атома, рассчитанный исходя из того, что молекула состоит из ионов. В молекуле сумма степеней окисления всех элементов равна нулю, а в ионе – заряду иона.
Обозначим искомую степень окисления за х и составим уравнения.
Mg +2CхO3-2 +2 + х + 3∙(-2) = 0, откуда х = +4 Mg+2C+4O3-2.
(PхO-24 )3− х + 4∙(-2) = -3, откуда х = +5 (P+5O-24 )3-.
(ClхO3-2)− х + 3∙(-2) = -1, откуда х = +5 (Cl+5O3-2)−
окислительно-восстановительные свойства для элемента последней частицы Cl+5:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 |



