21. Энергия активации. Факторы, определяющие величину энергии активации. Уравнение Аррениуса.
22. Энергия активации и тепловой эффект реакции.
23. Влияние катализаторов на скорость химической реакции.
24. Гомогенные и гетерогенные каталитические реакции.
25. Влияние катализаторов на константу скорости реакции и энергию активации реакции.
26. Ферменты. Каталитические яды. Ингибиторы.
27. Обратимые и необратимые химические реакции. Химическое равновесие.
28. Константа химического равновесия и факторы, определяющие ее величину.
29. Сдвиг химического равновесия. Принцип Ле-Шателье.
30. Значение химического равновесия в природе.
типовой Вариант
часть а (4-5)
1.Определение комплексных соединений, основные положения координационной теории Вернера.
2.Определить степень окисления комплексообразователя: [AuСl4]-; [Co(NH3)6]3+.
3.Получить и назвать комплексное соединение [Cu(NH3)4]Cl2 .Характеристика комплексного соединения (структура, первичная диссоциация, ступенчатая вторичная диссоциация, выражение константы нестойкости суммарной диссоциации комплексного иона)
часть В (6-7)
4.Закон действующих масс. Константа скорости химической реакции.
5.Записать кинетическое уравнение по закону действующих масс для реакции:
{Na2SO3} + 2{HCl} ® 2{NaCl} + {H2O} + (SO2).
Как изменится скорость реакции, если температуру уменьшить на 30оС (g=3)?
6.Записать выражение константы равновесия для реакции
2(SO2) + (O2) « 2(SO3), DH<0
и определить смещение равновесия при понижении давления.
часть с (8-10)
7.Указать тип гибридизации Ао комплексообразователя в ионе [BF4]- и определить его геометрию, магнитные свойства, спиновость и окраску раствора.
8.В системе (СО) + (Сl2) ⇆ (COCl2) равновесные концентрации реагирующих веществ (моль/л): [СО] = 0,02; [Сl2] = 0,5; [COCl2] = 1,2. Вычислите константу равновесия системы и исходные концентрации Сl2 и СО.
ОПОРНЫЙ КОНСПЕКТ ЛЕКЦИЙ модуля №1.
лЕКЦИЯ №1 “Введение. Основные понятия химии. Законы стехиометрии”.
План:
1. Предмет и задачи химии. Химия как наука о веществах и их превращениях.
2. Международная номенклатура неорганических соединений.
3. Основные понятия химии.
4. Основные стехиометрические законы.
5. Химический эквивалент, фактор эквивалентности, молярная масса эквивалента. Закон эквивалентов.
1. Предмет и задачи химии. Химия как наука о веществах и их превращениях
Решение большинства специальных задач базируется на применении основных законов естествознания в условиях практической деятельности человека. Поэтому успешная производственная деятельность немыслима без освоения в той или иной степени наук о природе - в первую очередь, математики, физики и химии.
Курс неорганической химии позволяет студентам глубоко изучить химический состав неорганических веществ, живых организмов и закономерности химических процессов, лежащих в основе химических превращений. Изучение химии позволяет получить современное научное представление о материи и формах её движения, о веществе как одном из видов движущейся материи, о механизме превращения химических соединений, о свойствах технических материалов и применении химических процессов в сельском хозяйстве и в современной экологической практике. В связи с этим представляется необходимым прочное усвоение основных законов химии и теории химии, овладение техникой химических расчётов, выработка навыков самостоятельного выполнения химических экспериментов и обобщения наблюдаемых фактов.
Химия - наука о составе, строении, свойствах и превращениях веществ. Цель изучения химии - освоить современные представления о строениях как атомов и молекул, так и вещества в целом, а также об основных законах, управляющих процессами превращения веществ. В результате необходимо овладеть основами квантово-механического подхода к описанию микромира, строения атомов, молекул и конденсированных форм вещества; понимать обоснование периодического закона; уметь проводить элементарные химико-термодинамические и кинетические расчеты; получить навыки проведения простых химических опытов.
Изучение химического состава неорганических веществ и живых организмов, а также закономерностей химических реакций, лежащих в основе биохимических превращений, дает возможность управлять процессами жизнедеятельности.
В результате изучения дисциплины студент должен закрепить основные химические понятия и законы, усвоить наиболее важные кинетические закономерности химических процессов, изучить свойства коллоидных растворов, свойства биогенных элементов и их соединений, представляющих наибольший интерес для специалистов сельского хозяйства, иметь представление о качественном анализе и основных методах количественного.
2.Международная номенклатура неорганических соединений.
основой химических веществ являются химические соединения. В настоящее время известно около 20 миллионов химических соединений, большинство из них являются органическими. Тем не менее, несколько миллионов химических соединений относятся к неорганическим веществам. Несмотря на столь многочисленный состав, большинство неорганических соединений укладываются в общую схему классификации, которая выглядит следующим образом.
1. Металлы и неметаллы простые вещества
2. ![]() Оксиды
Оксиды
3. Основания сложные
4. Кислоты вещества
5. Соли
Существует связь между указанными классами, что позволяет получать вещества одного класса из веществ другого класса. Такая связь называется генетической. Ее удобно отобразить в виде блок-схемы:
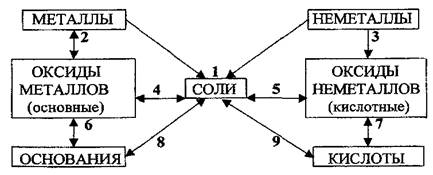
Название сложных неорганических веществ даётся как в соответствии с правилами, принятыми в русскоязычной литературе по химии: название электроотрицательной части (аниона) даётся в именительном падеже, название электроположительной части (катиона) – в родительном падеже(Fe2O3 – оксид железа (III)); а по правилам международной номенклатуре, согласно которой сначала называется катион, а затем анион (Fe2O3- железо(III)-оксид).
Среди неорганических соединений электролитами являются кислоты, основания, соли.
Кислоты - это электролиты, образующие при электролитической диссоциации в качестве катионов только катионы водорода. Число ионов водорода, способных образоваться в результате диссоциации одной молекулы кислоты называется основностью кислоты. Кислоты могут быть одноосновными (НС1, НNО3) и многоосновными (H2SO4, Н2СО3, Н3РО4).
В зависимости от величины степени диссоциации кислоты бывают сильными и слабыми.
Сильные кислоты являются сильными электролитами, диссоциируют практически полностью, в растворе присутствуют только катионы водорода и анионы кислотного остатка, недиссощшрованные молекулы отсутствуют. Примеры сильных кислот: HCl, НВг, HI, HNO3, H2SO4, НСlО3, НСlO4. В ионных уравнениях их формулы пишутся в диссоциированном виде.
Слабые кислоты являются слабыми электролитами, диссоциированы в незначительной степени, в их водных растворах преобладают недиссоциированные молекулы, присутствует также небольшое количество катионов водорода и анионов кислотного остатка. Вследствие этого, в ионных уравнениях формулы таких электролитов следует писать в недиссоциированном виде. Примеры слабых кислот: Н2СО3, H2SiО3, H2S, HClO, Н3РО4, HF, большинство карбоновых кислот.
Диссоциация многоосновных кислот протекает ступенчато, то есть только часть ионов, образовавшихся на первой ступени, диссоциирует дальше. Пример: диссоциация ортофосфорной кислоты в 0,1 М растворе по отдельным ступеням:
Н3РО4 ↔ Н+ + Н2РО4-
Н2РО4-↔Н+ + НРО42-
НРО42-↔H+ + РО43-
Т а б л и ц а 1.1. Формулы и название кислот и кислотных остатков
Название кислот | Формулы кислот | Название кислотных остатков средних солей |
Фтороводородная (плавиковая) | HF | Фторид |
Хлороводородная (соляная) | HCl | Хлорид |
Бромоводородная | HBr | Бромид |
Иодоводородная | HI | Иодид |
Циановодородная | HCN | Цианид |
Сероводородная | H2S | Сульфид |
Селеноводородная | H2Se | Селенид |
(орто) Борная | Н3ВО3 | Ортоборат (ВО2- - метаборат; В4О72- - тетраборат) |
Угольная | H2CO3 | Карбонат |
Метакремниевая | H2SiO3 | Метасиликат |
Ортокремниевая | H4SiO4 | Ортосиликат |
Мышьяковая | H3AsO4 | Арсенат |
Мышьяковистая | H3AsO3 | Арсенит |
Метафосфорная | HPO3 | Метафосфат |
Ортофосфорная | H3PO4 | Ортофосфат |
Пиро(ди)фосфорная | H4P2O7 | Пиро(ди)фосфат |
Фосфористая | H3PO3 | Фосфит |
Фосфорноватистая | H3PO2 | Гипофосфит |
Азотная | HNO3 | Нитрат |
Азотистая | HNO2 | Нитрит |
Серная | H2SO4 | Сульфат |
Сернистая | H2SO3 | Сульфит |
Селеновая | H2SeO4 | Селенат |
Селенистая | H2SeO3 | Селенит |
Хромовая | H2CrO4 | Хромат |
Дихромовая | H2Cr2O7 | Дихромат |
Марганцовая | HMnO4 | Перманганат |
Марганцовистая | H2MnO4 | Манганат |
Хлорноватистая | HClO | Гипохлорит |
Хлористая | HClO2 | Хлорит |
Хлорноватая | HClO3 | Хлорат |
Хлорная | HClO4 | Перхлорат |
Бромноватая | HBrO3 | Бромат |
Иодноватая | HIO3 | Иодат |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 |



