Гидролиз соли, образованной слабым основанием и сильной кислотой, сводится к гидролизу катиона слабого основания. В результате этого концентрация ионов Н+ в растворе становится больше концентрации ионов ОН-, и раствор приобретает кислую реакцию (рН<7).
Обычно гидролиз соли, если он происходит по одному многозарядному иону − катиону или аниону − не идет дальше первой ступени, так как обычно степень гидролиза по второй ступени значительно меньше, чем по первой. Исключением являются соли, образующие трудно растворимые или сильно летучие промежуточные или конечные соединения. Например, в приведенном ниже примере гидролиз трехвалентного катиона идет до второй ступени вследствие образования малорастворимой оксосоли:
Sb3+ + H2O ↔ SbOH2+ + HCl;
SbOH2+ + H2O → Sb(OH)2+ + НСl;
Sb(OH)2Cl → SbOCl↓ + H2O.
SbCl3 + H2O → SbOCl↓ + 2HCl.
2. анионный гидролиз. Соль образована сильным основанием и слабой кислотой, например, Nа2СО3:
СO32- + H2O ↔ HCO3- + ОН-.
Na2СO3+Н2О ↔ NaНСO3 + NaОН;
Гидролиз соли, образованной сильным основанием и слабой кислотой, сводится к гидролизу аниона слабой кислоты. Поэтому в растворе соли Nа2СО3 концентрация ионов ОН - становится больше концентрации ионов Н+, и реакция этого раствора – щелочная (рН>7).
3. Катионно-анионный гидролиз. Соль образована слабой кислотой и слабым основанием, например, СН3СООNН4:
СН3СОО - + NН4+ + Н2О ↔ СН3СООН + NН4ОН;
СН3СООNН4+H2O↔СН3СООН+NН4ОН.
Гидролиз соли, образованной слабой кислотой и слабым основанием, сводится к гидролизу как катиона слабого основания, так и аниона слабой кислоты. Реакция раствора зависит от степени диссоциации (силы электролита) образовавшихся кислоты и основания. Гидролиз соли слабого основания и слабой кислоты обычно проходит с образованием слабой кислоты и слабого основания; рН раствора при этом незначительно отличается от 7 и определяется относительной силой кислоты и основания. Для данной соли она будет близкой к нейтральной (рН≈7), так как степени диссоциации обоих слабых электролитов приблизительно равны.
4. Соли, образованные сильными кислотами и сильными основаниями, например, NаС1, гидролизу не подвергаются, так как их ионы не могут давать с ионами воды Н+ и ОН - слабых электролитов. Гидролиз соли сильного основания и сильной кислоты не протекает: Na2SO4+ H2O → .
5. Особый случай гидролиза − гидролиз галогенангидридов, тиоангидридов и других подобных ковалентных соединений, когда продуктом гидролиза электроположительного атома является гидроксид кислотного характера (то есть кислота):
SbCl5 + 4H2O → H3SbO4 + 5HCl;
SiS2 + 3H2O → H2SiO3 + 2H2S.
В этих случаях гидролиз идет с образованием двух кислот, причем это происходит в молекулярном виде, так как ангидриды в в водном растворе не диссоциируют на катион и анион. Во многих случаях необходимо предотвратить гидролиз. Эта задача решается как обычная задача смещения равновесия: необходимо добавлять в раствор сильную кислоту (при гидролизе по катиону) или щелочь (гидролиз по аниону).
3.Количественные характеристики гидролиза.
Гидролиз, как и диссоциацию, можно охарактеризовать степенью αг (доля гидролизованных единиц) и константой Кг. При этом Кг можно выразить через Кв и Кд слабой кислоты (Кд. к) или основания(Кд. осн). Например, для гидролиза аниона:
А− + Н2О ↔ НА + ОН−
для катиона:
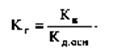
Для соли слабого основания и слабой кислоты:
Между Кг и αг существует такая же связь, как между Кд и αд :
ТЕМА САМОСТОЯТЕЛЬНОЙ РАБОТЫ
РАСТВОРЫ. ГИДРОЛИЗ СОЛЕЙ
Цель: Получение студентами знаний о механизме процессов растворения, свойствах и способах выражения состава растворов, об особенностях растворов сильных и слабых электролитов, а также о гидролизе солей.
Задачи: • Усвоить основные понятия и свойства растворов.
• Иметь представление об электрохимической диссоциации,
силе электролита, ионном произведении воды и рН растворов.
• Понять процесс гидролиза разных типов солей.
Методика выполнения блочно-модульных заданий
Задание 1. На теоретические вопросы ответы подготовить по лекциям и учебным пособиям.
Задание 2. Напишите в ионной форме следующие уравнения:
AgNO3 + KI ® AgI↓ + KNO3;
Ag+ + NO3− + K+ + I− ® AgI↓ + K+ + NO3−;
Ag+ + I− ® AgI↓.
Задание 3. Написать уравнения гидролиза солей в молекулярном и ионном виде: сульфата аммония, карбоната натрия, ацетата аммония.
Ответ.
соль сульфат аммония (NH4)2SO4 образована слабым основанием и сильной кислотой. Гидролиз соли, образованной слабым основанием и сильной кислотой, сводится к гидролизу катиона слабого основания. В результате этого концентрация ионов Н+ в растворе становится больше концентрации ионов ОН− и раствор приобретает кислую реакцию (рН<7):
NH4+ + H2O ↔ NН4ОН + H+;
(NH4)2SO4 + 2Н2О ↔ 2NН4ОН + H2SO4.
Соль карбоната натрия Nа2СО3 образована сильным основанием и слабой кислотой:
СO32- + H2O ↔ HCO3- + ОН;
Na2СO3+Н2О ↔ NaНСO3 + NaОН.
Гидролиз соли, образованной сильным основанием и слабой кислотой, сводится к гидролизу аниона слабой кислоты. Поэтому в растворе соли Nа2СО3 концентрация ионов ОН - становится больше концентрации ионов Н+, и реакция этого раствора – щелочная (рН>7);
Соль ацетата аммония СН3СООNН4образована слабой кислотой и слабым основанием:
СН3СОО - + NН4+ + Н2О ↔ СН3СООН + NН4ОН.
СН3СООNН4+H2O↔СН3СООН+NН4ОН;
Гидролиз соли, образованной слабой кислотой и слабым основанием, сводится к гидролизу как катиона слабого основания, так и аниона слабой кислоты. Реакция раствора зависит от степени диссоциации (силы электролита) образовавшихся кислоты и основания. Для данной соли она будет близкой к нейтральной (рН≈7), так как степени диссоциации обоих слабых электролитов приблизительно равны.
Задание 4. Вычислить рН, если концентрация Н+ равна 10-4 моль/л.
Ответ.
находим величину рН: рН= –lgC(H+); pH= –lg(10-4); pH= 4
Ответ: pH=4.
Задание 5. Коэффициенты растворимости Pb(NO3)2 при 60 и 10 оС соответственно равны 90 г и 46 г на 100 г воды. Какую массу чистого нитрата свинца можно получить при охлаждении его насыщенного раствора от 60 до 10 оС, если на приготовление насыщенного раствора было затрачено 400 мл воды?
Ответ.
найдем массу соли, которая раствориться при 60 оС в 400 мл воды.
m(Pb(NO3)2) = 90∙400/100 = 360 г
найдем массу соли, которая останется при 10 оС в 400 мл воды.
m(Pb(NO3)2) = 46∙400/100 = 184 г
Найдем массу чистого нитрата свинца, которую можно получить при охлаждении его насыщенного раствора от 60 до 10 оС
m(Pb(NO3)2) = 360 -184 = 176 г
ответ: 176 г Pb(NO3)2
Задание 6. Написать уравнение гидролиза гидрокарбоната натрия. По значениям константы гидролиза и константе диссоциации предсказать реакцию среды.(K1H2СO3 = 4,5·10-7; K2HСO3− = 4,8·10-11).
Ответ.
Рассмотрим процессы, происходящие в водном растворе гидрокарбоната натрия:
а) NaHCO3 → Na+ + HCO3− α = 1;
б) HCO3− ↔ H+ + CO32− K2 = 4,8·10-11 процесс диссоциации;
в) HCO3− + H2O ↔ H2CO3 + OH− K1 = 4,5·10-7 процесс гидролиза.
Процесс (а) определяет концентрацию исходных гидролизующихся ионов соли. Процессы (б) и (в) определяют равновесные концентрации Н+ и ОН−. Процессы диссоциации и гидролиза конкурируют.
Рассчитаем константу гидролиза Кг(HCO3−).
Кг(HCO3−) = Кw/К1 = 10-14/(4,5·10-7 ) = 2,2 ·10-8
Так как константа гидролиза больше константы диссоциации HCO3− (2,2 ·10-8 > 4,8·10-11), то процесс гидролиза идёт глубже, чем диссоциация и поэтому ионов ОН− в растворе больше, чем ионов Н+.
Среда раствора данной соли NaHCO3 щелочная. pH раствора NaHCO3 >7
ВАРИАНТ 1
1. Истинные растворы. Растворение как физико-химический процесс. Понятия "растворитель" и "растворенное вещество". Тепловые эффекты при растворении.
2. Закончить и написать в ионной форме следующее уравнение: Pb(NO3)2 + CaI2 ®
3. Написать уравнение гидролиза соли: карбоната натрия, хлорида магния, карбоната алюминия.
4. Найти концентрацию ионов H+ и OH−, если pOH = 4.
5. Какую массу медного купороса и какой объём воды нужно взять, чтобы приготовить 200 г насыщенного при 20°С раствора CuSO4 (s= 12,33 г CuSO4 /100 г воды)?
6. Написать уравнение гидролиза натрий гидрофосфата. По значениям константы гидролиза и константе диссоциации предсказать реакцию среды. (K3H2PO4−=6,3·10-8, K2HPO42−=1,3·10-12, K1H3PO4=7,6·10-3)
ВАРИАНТ 2
1. Электролиты и неэлектролиты. Основные положения теории электролитической диссоциации. Механизм диссоциации.
2. Закончить и написать в ионной форме следующее уравнение: NH4Cl + NaOH ®
3. Написать уравнение гидролиза соли: нитрата магния, сульфида калия, ацетата свинца (II).
4. Найти pH раствора, концентрацию ионов OH−, если концентрация H+ равна 10-5 моль/л.
5. Найдите массу KClO3 выделившегося из раствора массой 200 г с массовой долей соли 32 % при охлаждении его до 0 оС, если коэффициент растворимости соли при 0 оС равен 3,3 г.
6. Написать уравнение гидролиза натрий дигидрофосфата. По значениям константы гидролиза и константе диссоциации предсказать реакцию среды.(K3H2PO4−=6,3·10-8, K2HPO42−=1,3·10-12, K1H3PO4=7,6·10-3)
ВАРИАНТ 3
1. Степень электролитической диссоциации электролитов. Факторы, определяющие величину степени диссоциации (природа растворителя и растворенного вещества, температура, концентрация раствора). Сильные и слабые электролиты.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 |



