В результате гибридизации появляются новые гибридные орбитали, которые ориентируются в пространстве таким образом, чтобы расположенные на них электронные пары (или неспаренные электроны) оказались максимально удаленными друг от друга, что соответствует минимуму энергии межэлектронного отталкивания. Поэтому тип гибридизации определяет геометрию молекулы или иона (рис.4.5.).
Типы гибридизации
Тип гибридизации Геометрическая форма Угол между связями Примеры
sp линейная 180o BeCl2
sp2 треугольная 120o BCl3
sp3 тетраэдрическая 109,5o CH4
sp3d тригонально-бипирамидальная 90o; 120o PCl5
sp3d2 октаэдрическая 90o SF6
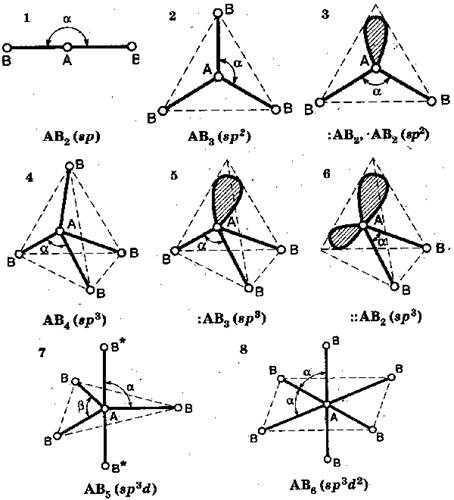
Рис. 4.5. Геометрия молекул по типу гибридизации
В гибридизации участвуют не только связывающие электроны, но и неподеленные электронные пары. Например, молекула воды содержит две ковалентные химические связи между атомом кислорода и двумя атомами водорода (рис.4.6.). Помимо двух пар электронов, общих с атомами водорода, у атома кислорода имеются две пары внешних электронов, не участвующих в образовании связи (неподеленные электронные пары). Все четыре пары электронов занимают определенные области в пространстве вокруг атома кислорода. Поскольку электроны отталкиваются друг от друга, электронные облака располагаются на возможно большем расстоянии друг от друга. При этом в результате гибридизации меняется форма атомных орбиталей, они вытянуты и направлены к вершинам тетраэдра. Поэтому молекула воды имеет угловую форму, а угол между связями кислород-водород равен 104,5o.
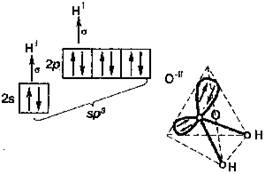
Рис. 4.6. Геометрия молекулы воды
Для предсказания типа гибридизации удобно использовать донорно-акцепторный механизм образования связи: происходит перекрывание пустых орбиталей менее электроотрицательного элемента и орбиталей более электроотрицательного элемента с находящимися на них парами электронов. При составлении электронных конфигураций атомов учитывают их степени окисления − условное число, характеризующее заряд атома в соединении, рассчитанный исходя из предположения ионного строения вещества.
Чтобы определить тип гибридизации и форму химической частицы, поступают следующим образом:
· находят центральный атом и определяют число σ-связей (по числу концевых атомов);
· определяют степени окисления атомов в частице;
· составляют электронную конфигурацию центрального атома в нужной степени окисления;
· если это необходимо, проделывают то же самое для концевых атомов;
· изображают схему распределения валентных электронов центрального атома по орбиталям, при этом, вопреки правилу Гунда, максимально спаривают электроны;
· отмечают орбитали, участвующие в образовании связей с концевыми атомами;
· определяют тип гибридизации, учитывая все орбитали, участвующие в образовании связи, а также неподеленные электроны; если валентных орбиталей недостаточно, используют орбитали последующих энергетических уровней;
· по типу гибридизации определяют геометрию химической частицы.
Наличие π-связей не влияет на тип гибридизации. Однако наличие дополнительного связывания может привести к изменению валентных углов, поскольку электроны кратных связей сильнее отталкиваются друг от друга. По этой причине, например, валентный угол в молекуле NO2 (sp2-гибридизация) увеличивается от 120o до 134o(рис.4.7.).
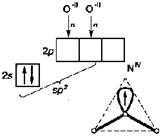
Рис. 4.7. Геометрия молекулы NO2
Кратность связи азот−кислород в этой молекуле равна 1,5, где единица отвечает одной σ-связи, а 0,5 равно отношению числа орбиталей атома азота, не участвующих в гибридизации (1) к числу оставшихся активных электронных пар у атома кислорода, образующих π-связи (2). Таким образом, наблюдается делокализация π-связей (делокализованные связи − ковалентные связи, кратность которых не может быть выражена целым числом).
В случае sp, sp2, sp3, sp3d2 гибридизации вершины в многограннике, описывающем геометрию химической частицы, равноценны, и поэтому кратные связи и неподеленные пары электронов могут занимать любые из них. Однако sp3d-гибридизации отвечает тригональная бипирамида, в которой валентные углы для атомов, расположенных в основании пирамиды (экваториальной плоскости), равны 120o, а валентные углы с участием атомов, расположенных в вершинах бипирамиды, равны 90o. Эксперимент показывает, что неподеленные электронные пары всегда располагаются в экваториальной плоскости тригональной бипирамиды. На этом основании делается вывод, что они требуют больше свободного пространства, чем пары электронов, участвующие в образовании связи. Примером частицы с таким расположением неподеленной электронной пары является тетрафторид серы. Если центральный атом одновременно имеет неподеленные пары электронов и образует кратные связи (например, в молекуле XeOF2), то в случае sp3d-гибридизации именно они располагаются в экваториальной плоскости тригональной бипирамиды.
Идеальная ковалентная связь существует лишь в частицах, состоящих из одинаковых атомов (Н2, N2 и т. д.). Если образуется связь между различными атомами, то электронная плотность смещается к одному из ядер атомов, то есть происходит поляризация связи. Характеристикой полярности связи служит ее дипольный момент. Дипольный момент молекулы равен векторной сумме дипольных моментов ее химических связей (с учетом наличия неподеленных пар электронов). Если полярные связи расположены в молекуле симметрично, то положительные и отрицательные заряды компенсируют друг друга, и молекула в целом является неполярной. Так происходит, например, с молекулой диоксида углерода. Многоатомные молекулы с несимметричным расположением полярных связей (и, следовательно, электронной плотности) являются в целом полярными. Это относится, в частности, к молекуле воды. На результирующее значение дипольного момента молекулы может повлиять неподеленная пара электронов. Так, молекулы NH3 и NF3 имеют тетраэдрическую геометрию с учетом неподеленной пары электронов (рис.4.8.).
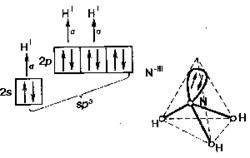
Рис. 4.8. Геометрия молекулы NН3
Степени ионности связей азот −водород и азот −фтор составляют 15 и 19%, соответственно, а их длины - 101 и 137 пм, соответственно. Исходя из этого, можно было бы сделать вывод о большем дипольном моменте NF3. Однако эксперимент показывает обратное. При более точном предсказании дипольного момента следует учитывать направление дипольного момента неподеленной пары.
Таким образом, метод ВС имеет следующие преимущества:
1. Соответствие метода химической традиции (молекула состоит из атомов, локализованная связь принадлежит паре атомов).
2. Простота описания сложных молекул с помощью схем ВС и структурных формул.
3. Возможность описания основных типов молекул и взаимодействий, валентности атомов.
Недостатки метода ВС:
1. Громоздкость, неэкономность математического описания.
2. Неверное описание свойств (магнитных, кратности связей, неполное описание геометрии) молекул простыми СВС и необходимость использования в связи с этим искусственных схем.
3. Преувеличение роли локализованных связей.
5. Метод молекулярных орбиталей
Расчет строения молекул по методу валентных связей очень сложен. Кроме того, этот метод не рассматривает вклад неспаренных электронов в образование связи.
Установлено, что в процессе образования химической связи в некоторых молекулах определенную роль играют не электронные пары, а отдельные электроны. Это наиболее отчетливо видно на примере ионизированной молекулы водорода Н2+, которая получается при электронной бомбардировке молекулярного водорода. Спектральные исследования показывают, что расстояние между ядрами в этой частице составляет 108 пм, а энергия связи равна 2,65 эВ; таким образом, это довольно прочная частица. Поскольку в Н2+имеется только один электрон, то очевидно, что в данной молекуле осуществляется одноэлектронная связь. Неспаренные электроны имеются во многих многоатомных частицах. К таким частицам относятся свободные радикалы. Свободные радикалы – это частицы, содержащие неспаренные электроны. Непарный электрон в свободных радикалах обозначают точкой около химической формулы, например·СН3. Радикалы обладают высокой реакционной способностью. Неспаренные электроны имеются также в некоторых устойчивых молекулах: NO, NO2, СlO2, O2.
Строение молекулы кислорода представляет особый интерес для теории химической связи. Атом кислорода имеет два неспаренных электрона, поэтому по методу валентных связей можно было бы ожидать, что при соединении двух атомов О сформируются две электронные пары и неспаренных электронов в молекуле О2 не будет. Однако исследование магнитных свойств кислорода свидетельствует о том, что в молекуле O2 есть два неспаренных электрона. Ряд исследователей предприняли попытки усовершенствовать метод валентных связей и сделать его пригодным для истолкования этих фактов. Однако более плодотворным оказался другой подход к объяснению и расчету ковалентной связи, получивший название метода молекулярных орбиталей (сокращенное обозначение – метод МО). Значительный вклад в его разработку внес Р. Малликен (США). В настоящее время метод МО является лучшим способом квантово-химической трактовки ковалентной связи. Если в расчетах Гейтлера и Лондона используется волновая функция, которая описывает движение обоих электронов в молекуле Н2, то метод молекулярных орбиталей исходит из волновых функций отдельных электронов. Таким образом, считается, что каждый электрон в молекуле находится на определенной молекулярной орбитали, описываемой соответствующей волновой функцией. Каждой молекулярной орбитали отвечает определенная энергия. На одной молекулярной орбитали могут находиться два электрона с противоположно направленными спинами.
Обычно молекулярные одноэлектронные волновые функции выражают в виде линейных комбинаций волновых функций электронов в атомах, из которых образована молекула. Этот вариант метода МО сокращенно обозначают МО ЛКАО (по начальным буквам слов "линейная комбинация атомных орбиталей"). Таким образом, метод молекулярных орбиталей показывает, что при связывании двух атомов в молекулу реализуются два состояния электрона – две молекулярные орбитали: одна с более низкой энергией E1, а другая с более высокой энергией E2. Это можно иллюстрировать энергетической диаграммой, представленной на рис. 4.9; такие диаграммы часто используют в методе МО. Квадрат (его часто заменяют кружком) около уровня энергии означает квантовую ячейку – орбиталь, которая может быть занята одним электроном или двумя электронами с противоположно направленными спинами (иногда квантовые ячейки не изображают, а непосредственно на линиях, показывающих уровни энергии, ставят стрелки, символизирующие спин электронов).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 |



