_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ __________________________________________________________________________________________________________________________________________________________________________Молярная масса эквивалента кислорода, водорода формулы)_________________________________________________________________________________________________________________________________________________________________ _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Молярные объемы эквивалентов водорода, кислорода (формулы)________________________________________________________________________________________________________________________________________________________________ _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________Закон эквивалентов (математическое выражение)_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
_____________________________________________________________________________________
_____________________________________________________________________________________
_____________________________________________________________________________________
Выполнение работы:
- Проверьте герметичность прибора: присоединив пробирку к эвдиометру, опустите уравнительный сосуд на 20-25 см ниже его первоначального положения. Если прибор герметичен, уровень воды в градуированном сосуде, несколько понизившись в начальный момент, в дальнейшем остается постоянным. Отсоединив пробирку, установите уравнительный сосуд так, чтобы уровень воды в градуированном сосуде совпал с верхней меткой шкалы - V1 (уровень отсчитывается по нижнему мениску жидкости).
V1 =:___________________________________
- в бумагу, на которой проводилось взвешивание, таким образом, чтобы получившийся Взвесьте на технохимических весах 0.12-0.15 г металлической стружки (m) и заверните металл сверток мог свободно перемещаться в пробирке и был открыт с одного конца для обеспечения доступа кислоты к металлу.
m =_____________________________________________
- Отмерьте мерным цилиндром 10 мл соляной кислоты и залейте ее в пробирку. Держа пробирку наклонно, поместите в верхнюю часть ее сверток с металлом и присоедините к эвдиометру. Держа пробирку наклонно, поместите в верхнюю часть ее сверток с металлом и присоедините к эвдиометру. Стряхните сверток с металлом в кислоту. В процессе химической реакции следите за тем, чтобы весь металл прореагировал с соляной кислотой. После окончания реакции охладите пробирку до комнатной температуры.
Опустите уравнительный сосуд до уровня воды в градуированном сосуде. Снимите показание уровня воды - V2.
V2 =_____________________________________________
Температура воздуха в лаборатории
t = ___________________________________________________
5. Атмосферное давление
P = ______________________________________________
- По таблице зависимости давления пара от температуры (приложение 1) определите давление насыщенного водяного пара ( h ).
Давление насыщенного водяного пара при различных температурах
t,0C | h, мм рт ст | t,0C | h, мм рт ст | t,0C | h, мм рт ст |
0 | 4,58 | 20 | 17,54 | 35 | 42,18 |
10 | 9,21 | 21 | 18,65 | 40 | 55,32 |
11 | 9,84 | 22 | 19,83 | 45 | 71,88 |
12 | 10,52 | 23 | 21,07 | 50 | 92,51 |
13 | 11,23 | 24 | 22,38 | 55 | 118,0 |
14 | 11,99 | 25 | 23,76 | 60 | 149,4 |
15 | 12,79 | 26 | 25,21 | 65 | 187,5 |
16 | 13,63 | 27 | 26,74 | 70 | 233,7 |
17 | 14,53 | 28 | 28,35 | 80 | 355,1 |
18 | 15,48 | 29 | 30,04 | 90 | 525,8 |
19 | 16,48 | 30 | 31,82 | 100 | 760,0 |
6. Давление насыщенного водяного пара
h = _____________________________________
- Рассчитайтеобъем выделившегося водорода
7. V = V1 - V2 _____________________________
- Проведите расчет молярной массы эквивалента металла.
8. Расчеты:
а) объем выделившегося водорода, приведенный к н. у. :
Vo = ![]() = .......
= .......
б) молярная масса эквивалента металла
МЭ (эксп.) = ![]() =
=
в) молярная масса металла М = МЭ ⋅ В
в) теоретическое значение молярной массы эквивалента металла:
1МЭ (теор.) = М (M) / B = .....
г) абсолютная ошибка эксперимента
А = МЭ (теор.) - МЭ (эксп.)
д) относительная ошибка эксперимента
K =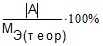
- Расчеты:
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Вывод:
______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Задачи по теме «Химический эквивалент»
Оксид металла содержит 10,00 г металла и 8,88 г кислорода. Определите молярную массу эквивалента металла. Гидрид металла содержит 2,02 г водорода и 13,88 г металла. Определите молярную массу эквивалента металла. При сгорании 53,96 г металла образуется 101,96 г оксида металла. Определите молярную массу эквивалента металла. 72 г гидрида металла содержат 3,03 г водорода. Определите молярную массу эквивалента металла. 4,80 г кальция и 7,85 г цинка вытесняют из кислоты одинаковые количества водорода. Вычислите молярную массу эквивалента цинка, если молярная масса эквивалента кальция равна 20,0 г/моль. Определите молярные массы эквивалентов металла и серы, если 4,86 г металла образуют 5,22 г оксида и 5,58 г сульфида.Оценка работы:
Подготовка |
Выполнение |
Оформление |
Дата: __________________ Подпись преподавателя: ____________________________

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



