
РОССИЙСКИЙ УНИВЕРСИТЕТ ДРУЖБЫ НАРОДОВ
Кафедра общей химии
ЖУРНАЛ ЛАБОРАТОРНЫХ РАБОТ
по курсу “Химия”
для студентов, потоков ИАБ-1, ИДБ-1, ИМБ-1, ИРС - 1, ИСБ-1, ИХБ-1
Студент(ка) ___________________________________________
Группа ___________________________________________
Преподаватель__________________________________________
Журнал сдан_______________________
Москва, ______________уч. год
УДК 54
У т в е р ж д е н о
РИС Ученого Совета
Российского университета дружбы народов
,
ЖУРНАЛ ЛАБОРАТОРНЫХ РАБОТ и семинарских занятий по курсу “Химия”
Для студентов, потоков ИАБ-1, ИДБ-1, ИМБ-1, ИРС - 1, ИСБ-1, ИХБ-1
Подготовлены на кафедре общей химии.
М.: Издательство РУДН, 2013. - с.
©, , 2013
© Издательство Российского университета дружбы народов, 2013г.
Правила техники безопасности при работе
в химической лаборатории
В химической лаборатории студенты должны научиться работать аккуратно и соблюдать правила техники безопасности:
Каждый студент должен знать:
Своё рабочее место в лаборатории. Правила хранения реактивов и работы с ними. Правила работы с легковоспламеняющимися жидкостями, легколетучими и токсичными веществами, концентрированными растворами кислот и щелочей. Нагревательные приборы в лаборатории и электрооборудование. Устройство и правила работы с газовой горелкой. Состав горючего газа. Средства пожаротушения в химической лаборатории. Индивидуальные средства защиты, используемые в химической лаборатории.Общие правила
Работа с химическими реактивами
Реактивы хранят в склянках с закрытыми пробками. Нельзя высыпать обратно в склянку реактив, случайно рассыпанный на столе. Растворы реактивов хранят в специальных склянках со стеклянными или пластмассовыми пробками. Выливать обратно в склянку взятый раствор нельзя. Остатки растворов, содержащие вредные или ценные вещества, нельзя выливать в раковины. Такие растворы сливают в специальные сосуды. Сухие вещества набирают чистым шпателем или стеклянной лопаточкой. Нельзя одновременно пользоваться одним и тем же шпателем для отбора разных реактивов. Нельзя класть шпатель непосредственно на стол, используйте чистый лист бумаги. Жидкие реактивы следует осторожно наливать из склянок; при этом склянки следует держать этикетками вверх, чтобы предохранить их от обливания и порчи. Склянки с растворами реактивов после использования следует сразу закрывать пробкой ( при этом нельзя путать пробки от разных склянок) и ставить на то же место, откуда они были взяты. При разбавлении водой концентрированных минеральных кислот (особенно серной), концентрированных растворов щелочей, выделяющих при этом тепло, следует приливать их тонкой струёй в холодную воду при одновременном помешивании. При нагревании жидкостей в пробирках следует держать пробирку отверстием от себя и людей, работающих рядом. При распознавании по запаху выделяющихся газов следует нюхать газ осторожно, издали, направляя его струю движением руки от сосуда к себе.Работа с газовой горелкой
Для нагревания в лаборатории применяют газовые горелки, в которых сжигают природный газ (в основном метан - СН4). Необходимо помнить, что утечка газа не допускается. Следите за правильным использованием газовой горелки.
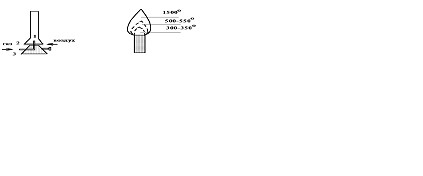
Рис.1. Горелка Теклю и строение пламени:
1 - Трубка;
2- диск, регулирующий подачу воздуха;
3- подставка;
Газовая горелка Теклю (рис.1) состоит из трубки (1), диска (2) и подставки (3). На боковой патрубок одевается каучуковая трубка, которая через газовый кран соединяет горелку с газовой сетью (трубой). Диск, который может вращаться по боковой нарезке, образуя различной величины зазор (щель) с трубкой, служит для регулирования притока воздуха в горелку. При недостаточном доступе воздуха происходит неполное сгорание газа, отчего пламя светится и коптит. Таким пламенем пользоваться нельзя. Для зажигания горелки нужно открыть газовый кран и поднести к верхней части трубки зажженную спичку. Чтобы выключить (потушить) горелку, необходимо закрыть газовый кран. Нельзя тушить горелку, задувая пламя. При слишком большом притоке воздуха пламя может погаснуть в верхней части горелки и “проскочить“ внутрь горелки, к самому отверстию подставки. “Проскок” пламени необходимо ликвидировать, для чего закрыть газовый кран, дать горелке остыть, поворотом диска уменьшить доступ воздуха и вновь зажечь её. В правильно отрегулированном пламени горелки можно различить три зоны: внутреннюю, среднюю и наружную, имеющие различные температуры.
Первая помощь при ожогах и порезах
Работающий в лаборатории должен знать, где находится аптечка первой помощи. При ожогах водяным паром, горячими предметами, брызгами горячей воды и т. д. смазывают пораженное место 5-10% раствором перманганата калия. При попадании кислоты или щелочи на руки (одежду) следует смыть их водой, а затем кислоту нейтрализовать 5% раствором гидрокарбоната натрия, а щелочь - 5% раствором борной кислоты или 2% раствором уксусной кислоты. При попадании химических реактивов на лицо или в глаза необходимо сразу промыть их большим количеством воды, а затем, если необходимо, обратиться за помощью в поликлинику.При порезах необходимо убедиться, нет ли в ране осколков стекла. При небольших порезах края порезов смазывают йодной настойкой, останавливают кровотечение, залив рану 10% раствором хлорида железа (III) или 3% раствором перекиси водорода, затем накладывают стерильную повязку.
Правила оформления работы в лабораторном журнале.
Название работы. Цель работы. Краткое теоретическое введение (основные законы и формулы, уравнения или графики, относящиеся к теме лабораторной работы). Экспериментальная часть:- конкретное задание на лабораторную работу; проведенный эксперимент в виде уравнений реакций, таблиц, графиков; наблюдения, расчёты по экспериментальным данным (если требуется).
Примечание.
Результаты эксперимента должны быть подписаны преподавателем. Все записи в тетради должны быть выполнены чернилами, графики – на миллиметровой бумаге только карандашом. Каждый график должен быть озаглавлен.
ЗАНЯТИЕ №1. Семинар №1
Основные классы химических Cоединений. Основные законы химии
Теоретические вопросы
Основные законы и понятия химии. Закон сохранения материи. Основные положения атомно-молекулярного учения. Законы сохранения массы, постоянства состава, кратных отношений, эквивалентов, простых объемных отношений, Авогадро. Уравнение Клапейрона-Менделеева. Основные понятия химии: атом, молекула, простое и сложное вещество, моль, мольная масса, относительная молекулярная и атомная масса. Основные классы химических соединений: простые вещества, сложные вещества (оксиды, основания, кислоты, соли).
Задачи
Осуществите превращения:
Ca → CaO → Ca(OH)2 → CaCl2 → CaSO4
S → SO2 → SO3 → H2SO4 → Na2SO4 → BaSO4
Fe → FeCl2 → Fe(OH)2 → Fe(OH)3 → Fe2O3 → Fe
C → CO2 → Na2CO3 → NaHCO3 → CO2 → CO
H2 → HCl → HNO3 → Cu(NO3)2 → Cu → CuSO4
Определите молярные массы следующих веществ: KNO3, Ba(OH)2, Al2(SO4)3, CuSO4.2H2O. Вычислить молекулярную массу бензола, зная. Что масса 600 мл его паров при 870С и давлении 83,2 кПа равна 1,30 г. Найти массу серной кислоты, необходимую для полной нейтрализации 40 г. гидроксида натрия. Найти объем 120 г газа, если его плотность по воздуху равна 3,2. Масса 250 мл газа при н. у. равна 0.903 г. Вычислить молярную массу газа и его плотность по воздуху. Сколько молей кислорода находится в 20 л воздуха, если его объемное содержание в воздухе составляет 32 % (н. у.). 0, 260 л газа при н. у. имеют массу 0,824 г. Вычислить молярную массу и плотность газа по воздуху (Dвозд). Газ при 150С и давлении 100кПа занимает объем равный 2л. Какой объем займет газ при нормальных условиях? Вычислить какой объем (н. у.) займет 1 г. H2, CH4, CO. Найти молекулярную формулу вещества, содержащего 93,75% по массе углерода и 6,25% по массе водорода, если плотность этого вещества по воздуху равна 4,41. Вещество содержит (по массе) 26,53% калия, 35,37% хрома и 38,10% кислорода. Найти его простейшую формулу.
ЗАНЯТИЕ №2. Лабораторная работа 1
ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА МЕТАЛЛА
Дата:_____________________________________________________
Цель работы: _________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Краткая теория:
Запишите:
Химический эквивалент(определение)____________________________________________
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________ __________________________________________________________________________________________________________________________________________________________Молярные массы эквивалентов кислот, оснований, солей (формулы)___________________

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



