_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Точка эквивалентности (определение). _________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Выполнение работы:
Уравнение реакции:
Порядок выполнения работы.
1. Ознакомьтесь с установкой для титрования. Она состоит из бюретки, закрепленной в штативе. Капиллярный конец бюретки присоединен к ней резиновым шлангом с зажимом. Цена деления шкалы бюретки 0,1 мл. Она позволяет измерять точные фиксированные объемы (раствор заполняется до метки в верхней части пипетки).
2. Промойте бюретку раствором соляной кислоты: через воронку залейте в бюретку раствор кислоты выше нулевой отметки и затем слейте его полностью в стакан, ослабив для этого зажим бюретки.
3. Снова заполните бюретку раствором кислоты и заполните ее капиллярный конец, загнув его вверх для облегчения удаления воздуха.
4. Установите уровень раствора кислоты на нулевой метке.
5. В коническую колбу отмерьте из общей бюретки или пипеткой 10,0 мл стандартного раствора гидроксида натрия, добавьте цилиндром 25-30 мл дистиллированной воды и 2-3 капли метилоранжа, который в присутствии щелочи окрасится в желтый цвет.
6. Подставив колбу под бюретку, проводите титрование: добавляйте по каплям раствор кислоты, непрерывно перемешивая раствор. Титрование окончено, когда добавление очередной капли раствора NaOH изменит окраску раствора в колбе на оранжевую (красный цвет раствора означает, что добавлен избыток кислоты, титрование необходимо повторить).
7. Запишите объем кислоты в бюретке в таблицу с точностью до 0,1 мл.
8. Повторите титрование еще два раза, каждый раз доливая раствор кислоты в бюретке до нулевого уровня. Расхождение между измеренными объемами кислоты не должно превышать 0,1- 0,2 мл.
№ опыта | 1 | 2 | 3 |
Объем раствора щелочи, мл | 10 | 10 | 10 |
Объем раствора кислоты, V, мл |
Концентрация раствора NaOH, CN (NaOH) = .......
Расчеты:
1) средний объем кислоты:
VHCl = ![]() = ...
= ...
2) концентрация раствора кислоты:
CN HCl = 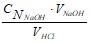 = ...
= ...
Рассчитайте молярную концентрацию эквивалента раствора соляной кислоты с точностью до 0,0001.
Вывод:
_________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Оценка работы:
Подготовка |
Выполнение |
Оформление |
Дата: __________________ Подпись преподавателя:
Типовые задачи.
При стандартизации раствора NaOH на титрование 10 мл его пошло 12,5 мл 0,0967 N раствора H2SO4. Вычислите концентрацию раствора NaOH. Какой объем 15% раствора серной кислоты (плотность 1,10 г/мл) потребуется для полного растворения 24,3 г магния? Для полного осаждения сульфата бария из 100 г 15% (по массе) раствора хлорида бария потребовалось 14,4 мл раствора серной кислоты. Найти молярную концентрацию эквивалента (нормальность) раствора кислоты. Какой объем 0,3 Н раствора кислоты требуется для нейтрализации раствора, содержащего 1,4 г гидроксида калия?
Занятие № 7. Коллоквиум №1
Вопросы для подготовки к коллоквиуму №1
Для успешной сдачи коллоквиума необходимо знать определения указанных понятий, формулировки и математические выражения законов и правил, уметь их применять, иллюстрировать важнейшие химические свойства элементов и их соединений и важнейшие промышленные процессы уравнениями реакций, уметь решать типовые задачи.
Темы коллоквиума №1
Основные законы и понятия химии.
Закон сохранения массы. Закон постоянства состава. Атом. Молекула. Химический элемент. Относительные атомная и молекулярная массы. Число Авогадро. Моль. Эквивалент. Молярная масса. Молярная масса эквивалента. Молярный объем газа. Эквивалентный объем газа. Закон эквивалентов. Газовые законы: закон Бойля-Мариотта, закон Гей-Люссака, уравнение состояния идеального газа, уравнение Клайперона-Менделеева. Химические формулы. Химические уравнения.
Строение атома и периодический закон .
Ядро атома. Элементарные частицы: протоны, нейтроны, электроны. Изотопы. Строение электронных оболочек атома. Квантовые числа. Атомные орбитали. Правила заполнения электронных орбиталей: принцип Паули, правило Хунда, правила Клечковского. Периодический закон (формулировкa и современная формулировка). Периодическая система элементов. Период, группа, подгруппа. Энергия ионизации. Энергия сродства к электрону. Относительная электроотрицательность. Изменениe свойств элементов в периодах и группах.
Химическая связь.
Энергия связи. Длина связи. Ковалентная связь. Обменный и донорно-акцепторный механизмы образования ковалентной связи. Характеристики ковалентной связи: полярность, направленность, кратность, насыщаемость. σ- и π-связи. Гибридизация орбиталей. Полярность связей и полярность молекул. Методы описания ковалентной связи. Метод валентных связей. Метод молекулярных орбиталей. Связывающие и разрыхляющие молекулярные орбитали. Порядок связи. Образование молекул H2, N2, O2, и молекулярных ионов Н2+, Не2+, О2-, О22- по методу МО. Ионная, координационная, металлическая, водородная связи. Силы межмолекулярного взаимодействия.
Химическаяи термодинамика.
Гомогенная система. Гетерогенная система. Фаза. Энтальпия реакции. Тепловой эффект реакции. Закон Гесса. Экзотермический и эндотермический процессы. Энергетические диаграммы экзотермической и эндотермической реакции.
Типовые задачи
Тема 1. Основные понятия и законы химии
1. Найдите массу 2 1023 молекул оксида углерода (IV).
2. Сколько молекул водорода содержится в 56 л его при нормальных условиях?
3. Какой объем занимают при нормальных условиях 1,5 1023 молекул хлороводорода?
4. При 170С и давлении 104 кПа (780 мм рт. ст.) масса 624 мл газа составляет 1,56 г. Вычислить молярную массу газа.
5. Масса колбы вместимостью 750 мл, наполненной при 270С кислородом, равна 83,3 г. Масса пустой колбы составляет 82,1 г. Определить давление кислорода в колбе.
6. В стальном баллоне вместимостью 6 л находится кислород. Температура его составляет 00С, а давление – 30,4 МПа. Какой объем кислорода можно получить из этого баллона при нормальных условиях?
7. Газометр вместимостью 20 л наполнен газом, плотность которого по воздуху составляет 0,40, температура – 170С, а давление – 103,3 кПа (774,8 мм рт. ст.). Вычислить массу газа в газометре.
8. Какой объем водорода при температуре 170С и давлении 102,4 кПа выделится при растворении 1,5 кг цинка в соляной кислоте?
9. Какая масса природного известняка, содержащего 90% по массе карбоната кальция, потребуется для получения 7 т негашеной извести (оксида кальция)?
10. Найти молекулярную формулу вещества, содержащего 93,75% по массе углерода и 6,25% по массе водорода, если плотность этого вещества по воздуху равна 4,41.
11. Найти молекулярную формулу масляной кислоты, содержащей (по массе) 54,5% углерода, 36,4% кислорода, а остальное – водород, если плотность ее паров по водороду равна 44.
12. Вещество содержит (по массе) 26,53% калия, 35,37% хрома и 38,10% кислорода. Найти его простейшую формулу.
Тема 2. Закон эквивалентов
1. Оксид металла содержит 10,00 г данного металла и 8,88 г кислорода. Определить молярную массу эквивалента металла.
2. Гидрид металла содержит 2,02 г водорода и 13,88 г металла. Определить молярную массу эквивалента металла.
3. При сгорании 53,96 г металла образуется 101,96 г оксида металла. Определить молярную массу эквивалента металла.
4. 72 г гидрида металла содержат 3,03 г водорода. Определить молярную массу эквивалента металла.
5. 4,80 г кальция и 7,85 г цинка вытесняют из кислоты одинаковые количества водорода. Вычислить молярную массу эквивалента цинка, если молярная масса эквивалента кальция равна 20,0 г/моль.
6. Определить молярные массы эквивалентов металла и серы, если 4,86 г металла образуют 5,22 г оксида и 5,58 г сульфида.
7. 4,00 г некоторого металла соединяются с 35,56 г брома и с 7,12 г серы. Определить молярные массы эквивалентов металла и брома, если молярная масса эквивалента серы равна 16,0 г/моль.
8. При взаимодействии 0,595 г некоторого вещества с 0,275 г хлороводорода получено 0,440 г соли. Определить молярные массы эквивалентов вещества и образовавшейся соли.
9. 0,752 г алюминия при взаимодействии с кислотой вытеснили 0,936 л водорода, измеренного при нормальных условиях. Определить эквивалентный объем водорода, если молярная масса эквивалента алюминия равна 8,99 г/моль.
10. На восстановление 11,75 г оксида металла потребовалось 2800 мл водорода, измеренного при нормальных условиях. Определить молярные массы эквивалентов оксида и металла.
11. Некоторое количество металла, молярная масса эквивалента которого равна 27,9 г/моль, вытесняет из кислоты 700 мл водорода, измеренного при нормальных условиях. Определить массу металла.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



