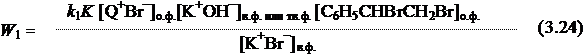Таблица 3.13
Выходы α-бромстирола (1), b–бромстирола (2) и фенилацетилена (3) в системах «ж/т» в присутствии катализаторов межфазного переноса и аминов (Скат)о. ф. = 1×10–3 моль/л; (Самина)о. ф. = 1·10–3 моль/л, (СSub)о. ф. = 0,8 моль/л;
t = 8 мин; Vо. ф. = 4 мл; nKOH = 0,025 моль; dКОН ≤ 0,4 мм; Т = 70 °С.
Катали-затор | № | Сокатализатор | 1 | 2 | 3 | kS | Dk∙102, мин–1 |
ДДТМАБ | 1 | — | 58,4 | 2,0 | следы | ||
2 | С5Н5N | 83,2 | 2,6 | - // - | 1,7 | 3,1 | |
3 | (С2Н5)3N | 89,0 | 2,6 | - // - | 1,9 | 3,8 | |
4 | С2Н5(СН3)2N | 91,2 | 2,8 | - // - | 2,2 | 4,1 | |
ГДТМАБ | 1 | — | 65,5 | 2,1 | следы | ||
2 | С5Н5N | 85,7 | 2,4 | - // - | 1,9 | 2,5 | |
3 | (С2Н5)3N | 92,6 | 3,7 | - // - | 1,9 | 3,4 | |
4 | С2Н5(СН3)2N | 96,0 | 3,9 | - // - | 2,1 | 3,4 | |
ТОАБ | 1 | — | 76,5 | 2,9 | следы | ||
2 | С5Н5N | 95,4 | 3,3 | - // - | 1,9 | 2,4 | |
3 | (С2Н5)3N | 92,9 | 3,7 | 3,4 | 1,9 | 2,0 | |
4 | С2Н5(СН3)2N | 84,4 | 3,8 | 11,8 | 2,1 | 1,0 |
В системах «ж/т» для составления смесей использовали ДДТМАБ, ГДТМАБ и ТОАБ, зарекомендовавшие себя как эффективные катализаторы межфазного переноса (рис. 3.1б), с одной стороны, и все исследованные карбоновые кислот, фенолы, спирты и амины, с другой стороны.
В системах «ж/ж» при составлении смесей использовали те же вещества, за исключением ТОАБ, активность которого в системах «ж/ж» крайне низка из-за растворимости в водной фазе (табл. 3.6).
Для всех исследованных смесей рассчитан коэффициент синергизма действия kS по уравнению 3.10.
Для составления сопоставления активности смесей катализаторов с активностью межфазного катализатора, являющегося наиболее активным компонентом в смеси, было рассчитано изменение эффективной константы псевдопервого порядка Dk в предположении что:
|
Dk = k2 − k1, (3.18)
где k2 и k1 — константы скорости для реакций в присутствии межфазного катализатора и смеси катализаторов, соответственно.
Согласно данным табл. 3.7 – 3.13 как в системах «ж/ж», так и в системах «ж/т» для всех исследованных смесей наблюдается эффект синергизма действия: kS >1, причем активность синергетических смесей выше активности наиболее активного компонента — межфазного катализатора: Dk > 0.
При анализе данных, представленных в таблицах 3.7 – 3.13, можно отметить ряд закономерностей. Для каждого типа сокатализатора и типа системы характерен определенный интервал значений kS (табл. 3.15).
Для систем «ж/т» характерны более высокие значения kS, чем для систем «ж/ж». Для каждого типа сокатализатора характерна внутренняя закономерность: значения kS возрастают с уменьшением силы кислоты и усилением силы сопряженного основания. В зависимости типа кислотного сокатализатора интервалы значений kS смещаются в сторону более высоких значений в следующем ряду:
карбоновые кислоты < фенолы < спирты,
т. е. в этом случае также наблюдается увеличение значений kS с уменьшением силы кислоты и увеличением силы сопряженного основания. Для анионов, являющихся слабыми органическими основаниями, в системах «ж/т» значения kS близки по величине к интервалам значений kS, полученных для карбоновых кислот и фенолов.
Таблица 3.14
Интервалы значений kS.
№ | Тип сокатализатора | Тип системы | kS |
1 | Карбоновые кислоты | «ж/ж» | 1,3 – 2,4 |
«ж/т» | 1,5 – 2,5 | ||
2 | Фенолы | «ж/ж» | 1,6 – 2,6 |
«ж/т» | 1,8 – 2,7 | ||
3 | Спирты | «ж/ж» | 1,9 – 2,7 |
«ж/т» | 2,2 – 2,9 | ||
4 | Амины | «ж/ж» | 1,7 – 2,2 |
На основании полученных закономерностей для объяснения синергизма действия солей тетраалкиламмония Q+Br− и органических кислот НА (карбоновых кислот, фенолов, спиртов) можно предложить следующую схему механизма их действия:
Схема 3.7
![]()
![]()

Согласно схеме 3.7, эффект синергизма действия катализаторов может быть обусловлен следующими причинами.
Во-первых, перенос иона ОН− из водной щелочной или твердой фазы КОН на ПРФ в виде ионных пар Q+OH− (ур. 3.7) способствует не только протеканию стадии дегидробромирования субстрата на ПРФ (ур. 3.8), но и стадии нейтрализации кислоты НА на ПРФ (ур. 3.19). Это приводит к смещению равновесия вправо и увеличению концентрации органического основания А− в объеме органической фазы. Такой эффект гипотетически равносилен увеличению силы кислоты при сохранении основности сопряженного основания. Естественно, что значение этого эффекта возрастает при переходе к кислотам с более низкими значениями Kа, что равносильно компенсации снижения концентрационного фактора.
Во-вторых, липофильный катион Q+ способствует переносу аниона основания А− в органическую фазу в составе ионной пары Q+А−. В этом случае его взаимодействие с субстратом (ур. 3.20) будет происходить в органической фазе, а не на ПРФ, что, возможно, является более благоприятным для реализации переходного состояния механизма Е2 реакции элиминирования.
Для реакций, протекающих в присутствии солей тетраалкиламмония и аминов, являющихся слабыми основаниями, может быть предложена следующая схема механизма синергетического действия:
Схема 3.8
![]()
|
В присутствии оснований (схема 3.8), также как и в присутствии кислот (схема 3.7), механизм синергетического действия обусловлен эффектом переноса иона OH− на ПРФ (ур. 3.7) и возможностью протекания реакции в объеме органической фазы (ур. 3.14). Однако, в отличие от механизма в присутствии [НА] (схема 3.7), катион Q+ не влияет на перенос основания (:В) в органическую фазу (ур. 3.21) и, соответственно, его растворимость в органической фазе. Рассмотренная схема механизма (схема 3.7) соответствует каталитическому циклу (лит. обзор схема 1.5, с. 27), предложенному Макошей для объяснения влияния спиртов на механизм реакции элиминирования в условиях МФК [91].
Следует отметить, что максимальная величина коэффициента синергизма действия kS соответствует соотношению Q+Br− : НА = 1 : 1 в соответствии со стехиометрией (ур. 3.19). Если [Q+Br−]ПРФ >> [НА]о. ф., то дегидробромирование субстрата будет происходить на ПРФ (схема 3.3, ур. 3.8). Если [Q+Br−]ПРФ << [НА]о. ф., то депротонирование НА будет происходить под действием щелочи КОН (схема 3.5, ур. 3.11).
В условиях МФК только в присутствии межфазного катализатора Q+Br− в соответствии со схемой 3.3 для скорости реакции (W1), с учетом ур. 3.8, можно записать следующее выражение:
![]()
С учетом ур. 3.7 получим выражение для концентрации [Q+ОН−]ПРФ:
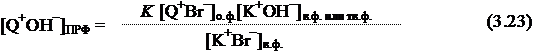
подставив 3.23 в 3.22, получим:
В условиях МФК в присутствии межфазного катализатора Q+Br− и органической кислоты НА в соответствии со схемой 3.7 для скорости реакции (W2), с учетом ур. 3.20, можно записать следующее выражение:
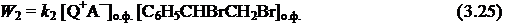
С учетом ур. 3.7 и 3.19 получим выражение для концентрации [Q+А−]о. ф.:

Подставив 3.26 в 3.25, получим:
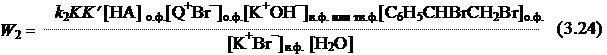
Влияние концентрации субстрата.
Согласно ур. 3.24 и 3.27, в обоих случаях для скорости реакции должен наблюдаться первый порядок по субстрату.
В работе проведено изучение эффективности реакции дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т» в присутствии ГДТМАБ и органических оснований для различных концентраций в области малых концентраций субстрата в органической фазе.
На рис. 3.8 представлены зависимости выхода a-бромстирола за 8 минут реакции без добавки о-крезола (кр. 1) и с добавкой о-крезола (кр. 2) от начальной концентрации субстрата в органической фазе в системах «ж/ж» и «ж/т», содержащих ГДТМАБ в качестве межфазного катализатора.

На рис. 3.9 представлены аналогичные зависимости для систем без добавки спирта (кр. 1) и с добавкой 2-метилбутанола-2 (кр. 2).

Как видно из рис. 3.8 и 3.9, в системах «ж/ж» и «ж/т» как в отсутствие добавки, так и в присутствии добавок о-крезола и 2-метилбутанола-2 реакция имеет линейную зависимость выхода продукта (за 8 минут) от концентрации субстрата. Расчет в логарифмических координатах показал, что во всех случаях порядок реакции по субстрату близок к 1 ± 0,02, что согласуется с ур. 3.24 и 3.27.
Влияние температуры.
В соответствии с ур. 3.24, для систем МФК/ОН− (в отсутствии добавки кислоты НА) влияние увеличения температуры на скорость реакции W1 будет определяться увеличением константы скорости k1, связанным с увеличением реакционной способности реагентов, и уменьшением константы равновесия K, связанным с десорбцией межфазного катализатора с ПРФ.
В соответствии с ур. 3.27, для систем, содержащих межфазный катализатор Q+Br− и кислотную добавку НА, влияние увеличения температуры на скорость реакции W2 будет определяться увеличением константы скорости k2, уменьшением константы равновесия K, а также уменьшением константы равновесия K¢ для реакции нейтрализации НА (ур. 3.19).
На рис. 3.10-а представлены данные по влиянию температуры на эффективность реакции дегидробромирования 1,2-дибром-1-фенилэтана по первой стадии в системах «ж/ж» в присутствии межфазных катализаторов ТОАБ, ДДТМАБ и ГДТМАБ без добавок спирта (кр. 1, 2, 3, соответственно) и с добавками 2-метилбутанола-2 (кр. 1¢, 2¢, 3¢, соответственно).
На рис. 3.11-а аналогичные системы представлены для системы «ж/т».
Результаты расчета эффективных значений энергий активации по температурным зависимостям в Аррениусовских координатах (рис. 3.10-б и 3.11-б) представлены в таблице 3.15.
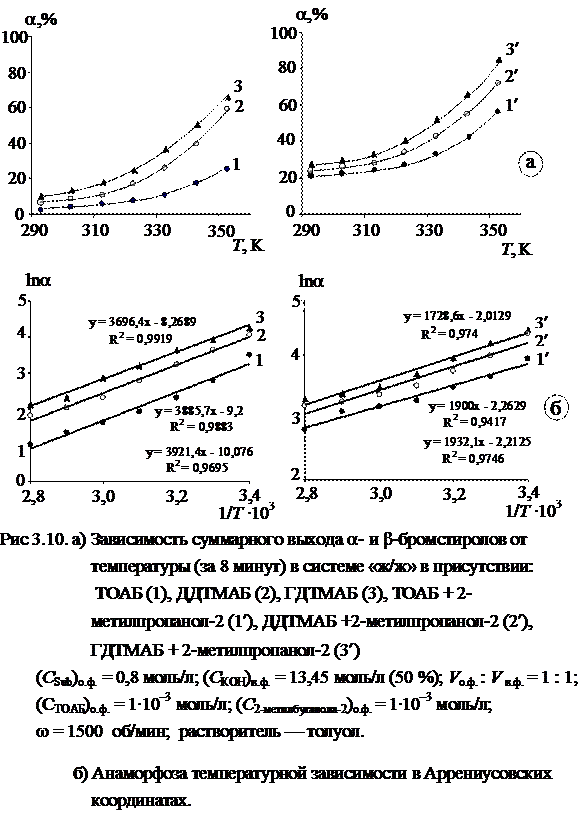

Таблица 3.15
Эффективные энергии активации реакции дегидробромирования 1,2-дибром-1-фенилэтана по первой стадии.
№ | Катализатор | Сокатализатор | ЕА, кДж / моль ∙ K | |
Система «ж/ж» | Система «ж/т» | |||
1 | ТОАБ | — | 32,6 | 29,1 |
2-метилбутанол-2 | 16,1 | 11,5 | ||
2 | ДДТМАБ | — | 32,3 | 30,2 |
2-метилбутанол-2 | 15,8 | 12,1 | ||
3 | ГДТМАБ | — | 30,7 | 31,5 |
2-метилбутанол-2 | 14,4 | 13,1 |
Согласно данным табл. 3.15, для всех межфазных катализаторов в присутствии добавок спирта эффективная энергия активации ЕА уменьшается в среднем в 2 раза в системах «ж/ж» и в 2,5 раза в системах «ж/т». Снижение ЕА в присутствии добавок спирта, по-видимому, обусловлено уменьшением величины K¢ для реакции нейтрализации спирта, что согласуется с ур. 3.24 и 3.27, а также предложенной схемой механизма синергетического действия катализаторов (схема 3.7).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |