Продукты нуклеофильного замещения в исследованных системах не обнаружены.
Образование a-бромстирола в качестве основного продукта свидетельствует о том, что в условиях МФК реакция протекает по механизму Е1сВ или по механизму Е2 с Е1сВ-подобным переходным состоянием.
Сопоставление с данными об эффективности реакции дегидробромирования в классической гомогенной системе с трет-бутилатом калия в качестве основания и трет-бутиловым спиртом в качестве растворителя [41], показало, что существенным преимуществом элиминирования 1,2-дибром-1-фенилэтана в условиях МФК в системах «ж/ж» и «ж/т» является возможность получения a-бромстирола с высокой селективностью (94-96 %). Этот результат согласуется с известными литературными данными о получении a‑бромстирола в системе «бензол – 1,2-дибром-1-фенилэтан – аликват 336» с выходом 83 % за 3 ч реакции [106] и в системе, содержащей водный раствор КОН и катамин АБ, с селективностью 85 % по a-бромстиролу и 5 % по b‑бромстиролу [50].
Кроме того, системы МФК обладают явными технологическими преимуществами: использование дешевой щелочи, отсутствие пожароопасности, связанной с использованием щелочных металлов.
1.1 Влияние природы межфазных катализаторов и их липофильности на эффективность реакции дегидробромирования.
Как отмечено в литературном обзоре [см с. 5-8], в системах «ж/ж» в случае реакций, протекающих по экстракционному механизму МФК, наблюдается взаимосвязь между каталитической активностью межфазных катализаторов и их растворимостью в органической фазе [5], а для реакций, протекающих с участием ПРФ, не исключена возможность, что каталитическая активность тетраалкиламмониевых солей симметричного строения коррелирует с их поверхностной активностью [40]. Анализ эффективности действия межфазных катализаторов различной природы в системах МФК/ОН– с твердыми щелочами в литературе практически отсутствует.
В настоящей работе проведен анализ каталитической активности бензо-15-краун-5-эфира, полиэтиленгликоля (ПЭГ) и ряда солей тетраалкиламмония. Данные по влиянию природы межфазных переносчиков на процесс дегидробромирования 1,2-дибром-1-фенилэтана в двухфазных системах «ж/ж» с 50 %-ным раствором КОН (а) и «ж/т» с твердым мелкодисперсным КОН (б) представлены на рис. 3.1. Следует отметить, что в качестве кинетической характеристики процесса использовали выходы продуктов за 8 минут протекания реакции. За это время для всех исследованных межфазных катализаторов не наблюдалось образование сколько-нибудь значительных количеств фенилацетилена, что свидетельствует о том, что исследованные каталитические системы эффективны только на первой стадии дегидробромирования 1,2‑дибром-1-фенилэтана. Выход побочного продукта первой стадии дегидробромирования (b-бромстирол) во всех опытах не превышал 2-5 %, что позволяет судить о каталитической активности межфазных катализаторов по выходу основного продукта (a-бромстирол) за указанный промежуток времени. Как видно из рис. 3.1 выход a-бромстирола без добавок межфазного катализатора не превышает 2,8 % в системе «ж/ж» и 6,8 % в системе «ж/т».
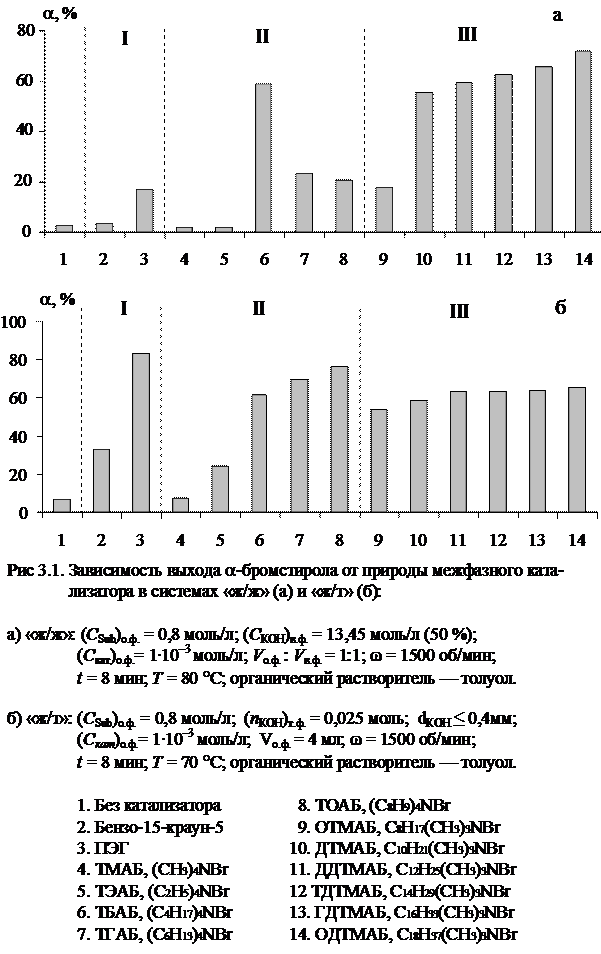
Первая группа катализаторов (I) включает краун-эфир и полиэтиленгликоль (ПЭГ), являющийся линейным аналогом краун-эфира. Для этих катализаторов характерна низкая активность в системах «ж/ж» (рис. 3.1-а), что, по-видимому, обусловлено их высокой способностью растворяться в щелочной водной фазе и, соответственно, слабой поверхностной активностью на границе раздела фаз. В системах «ж/т» (рис. 3.1-б) их каталитическая активность существенно выше, причем ПЭГ является более активным по сравнению с бензо-15-краун-5-эфиром, его активность в этом случае (83,3 %) существенно превышает и активность солей тетраалкиламмония. Можно предположить, что в системах «ж/т» для ПЭГ характерны два механизма действия.
Во-первых, ПЭГ способен координировать катион калия с образованием липофильного катиона Q+ и, соответственно, ионной пары Q+OH–, обеспечивая механизм переноса OH– из твердой фазы КОН на ПРФ с образованием «омега»-фазы, в которой осуществляется взаимодействие комплекса [ПЭГ • К+ • OH– ] с субстратом:
Схема 3.1
![]()

Во-вторых, в системах «ж/т», где вода появляется только в результате образования в ходе реакции, негидратированные молекулы ПЭГ в органической фазе способны проявлять основные свойства и обеспечивать перенос молекулы галогеноводорода от молекулы субстрата к ПРФ, обеспечивая протекание стадии депротонирования субстрата в объеме органической фазы:
Схема 3.2
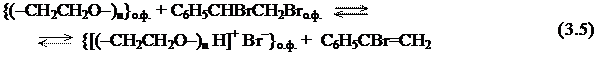
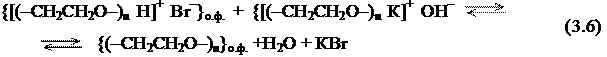
В работе также исследовалась каталитическая активность классических катализаторов межфазного переноса — солей тетраалкиламмония, которые условно разбиты на две группы (рис. 3.1): II — соли с катионом симметричного строения, III — соли с катионом, у которого один из радикалов является длинноцепочечным.
Соли с длинноцепочечными радикалами (III) проявляют достаточно высокую и практически одинаковую активность как в системах «ж/ж» (рис. 3.1‑а), так и в системах «ж/т» (рис. 3.1-б). Активность этих солей увеличивается в обоих типах систем с увеличением длины углеводородного радикала в ряду С8 < С10 < С12 < С14 < С16 < С18. Поведение солей с катионом симметричного строения (II) не столь однозначно. В системах «ж/т» (рис 3.1-б) активность катализаторов возрастает с увеличением длины алкильных заместителей в ряду С1 < С2 < С4 < С6 < С8. В системах «ж/ж» (рис. 3.1-а) проявляется экстремальная зависимость от длины алкильных заместителей: С1 < С2 < С4 > > С6 > С8. Таким образом, активность таких межфазных катализаторов как тетрагексиламмоний бромид (ТГАБ) и тетраоктиламмоний бромид (ТОАБ) в системах «ж/т» существенно превышает их активность в системах «ж/ж».
Как было отмечено в литературном обзоре [см. с. 9], на эффективность межфазного переноса может влиять доступность положительного заряда на атоме азота в катионе тетраалкиламмония для анионов разного размера в зависимости от размера алкильных заместителей. В работе [41] высказано предположение, что в системах «ж/ж» взаимодействие объемных гидратированных ионов OH– с катионами тетраалкиламмония симметричного строения с достаточно большой длиной алкильных заместителей приводит к образованию «рыхлых» ионных пар и снижению эффективности межфазного переноса, тогда как в системах «ж/т», содержащих негидратированные и, соответственно, малые по размеру ионы OH–, этот эффект не проявляется.
На наш взгляд специфические отличия в поведении солей тетраалкиламмония с катионами симметричного строения и с катионом, содержащим один длинноцепочечный радикал, нехарактерные для систем с экстракционным механизмом МФК, обусловлены тем, что реакция дегидробромирования 1,2-дибром-1-фенилэтана в двухфазных системах протекает по механизму МФК с участием ПРФ:
Схема 3.3
![]()
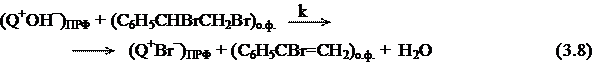
В соответствии с этим механизмом скорость реакции зависит от величины площади ПРФ. В системах «ж/ж» скорость реакции зависит от поверхности раздела фаз образующейся эмульсии и, следовательно, от поверхностной активности и эмульгирующей способности межфазного катализатора.
Экспериментально было отмечено, что наиболее высокая активность в системах «ж/ж» наблюдалась в случае образования устойчивых эмульсий типа «м/в» (масло-вода). Согласно литературным данным [115-116] эмульгирующая способность поверхностно-активных веществ (ПАВ) может быть сопоставлена с системой числовых коэффициентов, называемых числами гидрофильно-липофильного баланса (ГЛБ): оптимальные значения ГЛБ для эмульгаторов типа «в/м» (вода-масло) составляют 2¸6, для эмульгаторов типа «м/в» — 16¸18.
В данной работе сделана относительная оценка чисел ГЛБ для использованных солей тетраалкиламмония (без учета строения катиона) на основе принципа аддитивности для групповых чисел ГЛБ: В(R4N+Br–) = +18,6; В(‑СН2-, СН3-) = − 0,475.
На рис. 3.2 представлены зависимости выхода a-бромстирола от рассчитанных чисел ГЛБ солей тетраалкиламмония в системах «ж/ж» и «ж/т». Как видно из рис. 3.2 в системах «ж/ж» активность катализаторов при уменьшении чисел ГЛБ проходит через максимум, которому соответствуют числа 16,4¸18,2, т. е. максимальная устойчивость эмульсий типа «м/в».
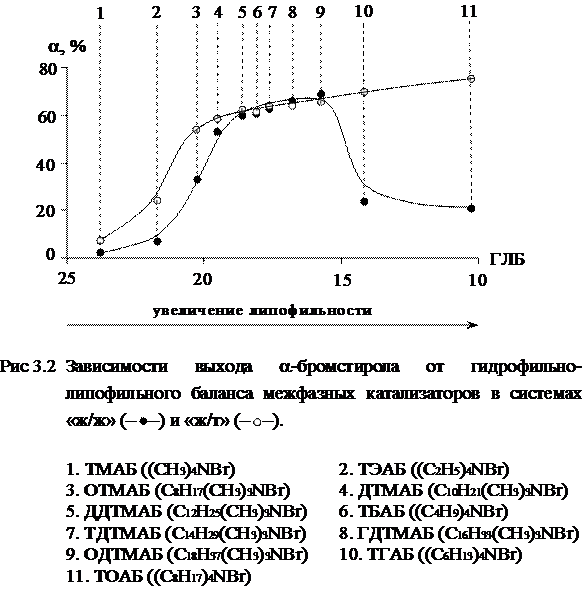
В соответствии с известной моделью эмульсий [115], поверхность раздела между фазами и соответственно межфазное натяжение можно условно разделить на две части (s1 + s2 = s): первую (s1), связанную с областью контакта полярных групп с водой, и вторую (s2), соответствующую области контакта углеводородных цепей молекул ПАВ с органической фазой. Тип образуемой эмульсии («в/м» или «м/в») должен быть таким, чтобы внутренняя поверхность характеризовалась более высоким межфазным натяжением. Это правило иногда формулируется таким образом: внешней должна быть та фаза, в которой лучше растворяется дифильное вещество, образующее эмульсию.
Таким образом, в ряду гидрофильных по своей природе солей тетраалкиламмония (s1 < s2), образующих эмульсии прямого типа «м/в», с увеличением липофильности уменьшается величина s2 и, соответственно, межфазное натяжение s, что облегчает процесс диспергирования в процессе перемешивания и приводит к образованию эмульсий с более высокоразвитой поверхностью раздела фаз: ТМАБ < ТЭАБ < ОТМАБ < ДТМАБ < ДДТМАБ < ТБАБ< ТДТМАБ < ГДТМАБ < ОДТМАБ. Липофильные по своей природе соли тетраалкиламмония (s1 ≥ s2), такие как ТГАБ и ТОАБ, уже не являются эмульгаторами типа «м/в», но существенную устойчивость обратных эмульсий «в/м» не обеспечивают.
Таким образом, можно считать, что в системах «ж/ж» каталитическая активность солей тетраалкиламмония коррелирует с их поверхностной активностью на границе раздела жидких фаз, причем наиболее высокая активность соответствует катализаторам, имеющим оптимальную сбалансированность ГЛБ и обеспечивающим максимальное снижение межфазного натяжения, что приводит к образованию эмульсий типа «м/в» с высокоразвитой поверхностью раздела фаз. Этот фактор является определяющим для реакций, протекающих по механизму МФК с участием ПРФ в системах «ж/ж».
В системах «ж/т» (рис. 3.2) каталитическая активность межфазных катализаторов возрастает с увеличением липофильности. В области чисел ГЛБ от 24 до 20 активность возрастает достаточно резко, что, по-видимому, связано с обеспечением агрегативной устойчивости суспензии мелкодисперсного КОН. Повышение липофильности поверхностного слоя межфазного катализатора на частицах предотвращает их коагуляцию и, соответственно, уменьшение эффективной площади ПРФ. После достижения агрегативной устойчивости суспензии дальнейшее повышение липофильности межфазных катализаторов, которым соответствует снижение чисел ГЛБ от 18 до 10, приводит к более медленному росту каталитической активности солей тетраалкиламмония. Возможно, это связано с дальнейшим снижением величины s2, соответствующей области контакта углеводородных цепей с органической фазой, что создает более благоприятные условия для взаимодействия молекул органического субстрата с ионными парами Q+OH– на ПРФ (ур. 3.8).
На рис. 3.3 приведены графики зависимости выхода a-бромстирола (за 8 минут реакции) от концентрации ГДТМАБ, ТОАБ и ПЭГ в системах «ж/ж» и «ж/т».

Как видно из рисунка, в системах «ж/ж» (рис 3.3-а) активность межфазных катализаторов увеличивается в ряду: ПЭГ < ТОАБ < ГДТМАБ, а в системах «ж/т» (рис 3.3-б) — в ряду ГДТМАБ < ТОАБ < ПЭГ, что согласуется с данными рис. 3.2.
Вид кривых зависимости выхода a-бромстирола от концентрации межфазных катализаторов аналогичен виду изотерм адсорбции, что согласуется с принятой в данной работе моделью механизма МФК с участием ПРФ для реакции дегидробромирования 1,2-дибром-1-фенилэтана. Как видно из рис. 3.3, насыщение ПРФ межфазным катализатором как в системах «ж/ж» (а), так и в системах «ж/т» (б), достигается при концентрации межфазного катализатора в органической фазе равной 1∙10–3 моль/л. На ПРФ катион межфазного переносчика Q+ находится преимущественно в виде ионных пар Q+OH–:
![]()
Вследствие того, что ионная пара Q+Br– является более липофильной, чем пара Q+OH– (из-за высокой гидрофильности иона ОН–), на ПРФ будет превалировать Q+OH–, а в объеме органической фазы — Q+Br–. Это согласуется с известными литературными данными [2, 8, 32] о том, что для большинства классических межфазных переносчиков растворимость ионных пар Q+OH– в органической фазе крайне незначительна.
После насыщения поверхности (Скат > 1∙10–3 моль/л) избыток межфазного катализатора будет находиться в органической фазе преимущественно в форме Q+Br–, что не приводит к увеличению каталитической активности систем.
Таким образом, на основании полученных экспериментальных данных можно считать, что реакция дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т» протекает по механизму МФК с участием ПРФ и оптимальной концентрацией межфазного катализатора является концентрация, соответствующая насыщению ПРФ. В системах «ж/т» активность солей тетраалкиламмония как для катионов симметричного, так и несимметричного строения возрастает с увеличением их липофильности, что обусловлено повышением устойчивости суспензии и обеспечением максимального сродства органического субстрата к ПРФ, на которой концентрируется основание в форме ионных пар Q+OH–.
В системах «ж/ж» активность солей тетраалкиламмония коррелирует с изменением поверхностной активности на границе раздела фаз и является максимальной для межфазных катализаторов, обеспечивающих образование устойчивой эмульсии «м/в» с высокоразвитой ПРФ. Следует подчеркнуть факт высокой активности ПЭГ в системах «ж/т», что может быть обусловлено синергизмом двух механизмов действия: извлечение ионов ОН– из твердой фазы в «омега»-фазу на ПРФ и дегидробромирование субстрата в объеме органической фазы за счет осно́вных свойств негидратированных молекул ПЭГ. Аналогичные особенности характерны для краун-эфира, но в меньшей степени, чем для ПЭГ.
В связи с этим существенный интерес представляет изучение возможностей повышения эффективности межфазных каталитических систем за счет использования композиций межфазных катализаторов, включающих краун-эфир или ПЭГ с одной стороны, и соль тетраалкиламмония с другой стороны.
1.2 Синергизм действия смесей различных по природе межфазных катализаторов.
Согласно литературным данным для реакций элиминирования и алкилирования явление сокатализа, а в некоторых случаях и синергетический эффект, были обнаружено для смесей "краун-эфир – четвертичная ониевая соль" [66-72] и "ПЭГ – четвертичная ониевая соль" [73-75]. Было установлено, что предпочтительным является использование каталитических пар типа "четвертичная аммониевая соль (аликват) – краун-эфир (бензо-15-краун-5)" и "аликват-полиэтиленгликоль (ПЭГ-300)". [117]. Авторами показано, что при использовании смеси "аликват – краун-эфир" наблюдается увеличение скорости реакции алкилирования на 20 % относительно аддитивной величины.
Однако однозначное представление о природе синергетического эффекта в литературе отсутствует. В работе [117] предполагается, что в системах «ж/т» роль краун-эфира сводится к разрыхлению кристаллической решетки твердого NaOH за счет образования комплекса [краун-эфир • Na+ • OH−], а роль катиона аммониевой соли состоит в образовании ассоциата с гидроксид-ионом и координации его с субстратом.
К количественной характеристике синергетического эффекта также нужно относиться с осторожностью. Большинство авторов для оценки эффекта синергизма используют предложенную в работе [67] величину k, числено равную отношению выхода продукта реакции в присутствии смеси катализаторов (h3) к сумме выходов продукта в присутствии индивидуальных катализаторов (h1 + h2):
 Если kS > 1, имеет место синергизм, если kS < 1 ¾ антагонизм и если kS = 1 — сокатализ.
Если kS > 1, имеет место синергизм, если kS < 1 ¾ антагонизм и если kS = 1 — сокатализ.
Следует, однако, обратить внимание на то, что авторы работы [67] оперируют фактом повышения выхода продукта при катализе смесью катализаторов, не соблюдая требования постоянства суммы их концентраций, что важно для корректного выявления синергетического эффекта.
В связи с этим для выявления эффектов положительного отклонения от аддитивности каталитического действия смеси мы использовали подход, при котором соотношение индивидуальных компонентов варьируется при условии сохранения постоянной суммарной концентрации межфазных катализаторов (Скат1 + Скат2 = 2∙10–3 моль/л). Данные по активности смесей ГДТМАБ и ПЭГ представлены на рис. 3.4, по активности смесей ТОАБ и ПЭГ — на рис. 3.5. Как видно из рис. 3.4 и 3.5, для смесей ГДТМАБ и ПЭГ и ТОАБ и ПЭГ как в системах «ж/ж» (кр. 1), так и в системах «ж/т» (кр. 2) для всех соотношений компонентов наблюдается положительное отклонение от аддитивности действия.

Согласно данным рис. 3.4, в системе «ж/ж» (кр. 1) ГДТМАБ в виде индивидуального компонента является более активным, чем ПЭГ, что, по-видимому, обусловлено его более выраженной эмульгирующей способностью. Смесь ГДТМАБ и ПЭГ является более активной, чем наиболее активный компонент — ГДТМАБ, если его концентрация составляет не менее 0,5∙10–3 моль/л, т. е. содержание в смеси не менее 25 %. Максимальная активность соответствует концентрации (1,00 ¸ 1,25)∙10–3 моль/л при его процентном содержании в смеси 50 ¸ 63 %.
По-видимому, в условиях конкурентной адсорбции на ПРФ синергизм действия ГДТМАБ и ПЭГ обусловлен тем, что более поверхностно-активный компонент (ГДТМАБ) адсорбируется на ПРФ в форме ионной пары Q+OH– и обеспечивает максимальную эффективность эмульгирования (максимальная площадь ПРФ) и концентрирование OH–, тогда как компонент с меньшей поверхностной активностью (ПЭГ) распределяется между водной-щелочной и органической фазами. ПЭГ, растворенный в органической фазе, выполняет функцию межфазного переносчика галогеноводорода от молекулы субстрата к ПРФ.
Из рис. 3.4 видно, что при дальнейшем увеличении содержания ГДТМАБ в смеси (> 63 %) уменьшается содержание ПЭГ и его концентрация как органического основания в углеводородной фазе, что приводит к относительному снижению величины синергетического эффекта.
С другой стороны, если содержание ГДТМАБ в смеси будет менее 25 %, то ПЭГ будет частично вытеснять его с ПРФ, что приведет к снижению эмульгирующей способности смеси и, соответственно, уменьшению эффекта синергизма действия двух межфазных катализаторов.
Согласно данным рис. 3.5, в системе «ж/ж» (кр. 1) для смеси ТОАБ и ПЭГ эффект синергизма действия выражен в меньшей степени, чем для смеси ГДТМАБ и ПЭГ (рис. 3.4, кр. 1). Это обусловлено тем, что ТОАБ является плохим эмульгатором, и его активность несущественно превышает активность ПЭГ. В остальном здесь сохраняются те же закономерности, что и для смеси ГДТМАБ и ПЭГ. Максимальная активность смеси наблюдается при содержании ТОАБ в смеси 50 ¸ 63 %.
Согласно данным рис. 3.4 и 3.5, в системах «ж/т» (кр. 2) ПЭГ является более активным компонентом, чем ГДТМАБ и ТОАБ. В системах «ж/т» активность смеси ГДТМАБ и ПЭГ (рис. 3.4, кр. 2) выше активности ПЭГ, если содержание ГДТМАБ не превышает 75 % и, соответственно, содержание ПЭГ составляет не менее 25 %. Активность смеси ТОАБ и ПЭГ в системах «ж/т» (рис. 3.5, кр. 2) выше активности ПЭГ, если содержание ТОАБ не превышает 87,5 % и, соответственно, содержание ПЭГ составляет не менее 12,5 %. Максимальная активность смеси в обоих случаях наблюдается при равном содержании компонентов: 50 % ПЭГ и 50 % соли тетраалкиламмония.

Таким образом, механизм действия смеси межфазных катализаторов в системах «ж/т», по-видимому, обусловлен тем, что соли тетраалкиламмония формируют на поверхности частиц твердой щелочи липофильный слой межфазного катализатора в форме ионных пар Q+OH–, обеспечивая эффективность взаимодействия OH– с субстратом на ПРФ, а небольшие добавки ПЭГ обеспечивают его действие в качестве органического основания в объеме органической фазы. При более высоких содержаниях ПЭГ может конкурентно вытеснять соль тетраалкиламмония с ПРФ, снижая липофильность межфазного слоя, что приводит к уменьшению эффекта синергизма действия двух катализаторов.
Общую схему механизма действия двух межфазных катализаторов в системах «ж/ж» и «ж/т» можно представить следующим образом:
Схема 3.4
![]()

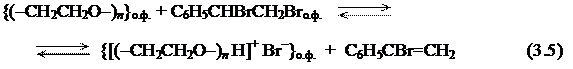
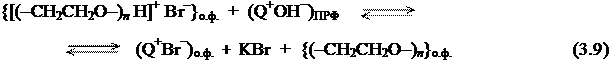
Синергизм действия двух катализаторов, по-видимому, обусловлен тем, что соль тетраалкиламмония, выполняющая роль катализатора межфазного переноса иона ОН− из щелочной водной фазы на ПРФ, обеспечивает не только повышение скорости взаимодействия ОН− с субстратом (ур. 3.8), но и необходимую скорость регенерации основной формы ПЭГ (ур. 3.9).
Согласно данным рис. 3.4 и 3.5, наибольший эффект синергизма можно ожидать в смесях, содержащих равные количества межфазных катализаторов. Далее в работе для оценки синергетического эффекта смесей катализаторов при постоянстве суммы их концентраций использовалась величина kS, определяемая с помощью следующего соотношения:
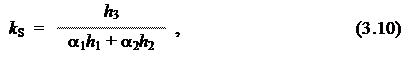 где h3 — выход продукта при суммарной концентрации смеси катализаторов, равной С; h1 — выход продукта в присутствии первого катализатора с концентрацией С1 = С; h2 — выход продукта в присутствии второго катализатора с концентрацией С2 = С; a1 и a2 — мольные доли компонентов в смеси.
где h3 — выход продукта при суммарной концентрации смеси катализаторов, равной С; h1 — выход продукта в присутствии первого катализатора с концентрацией С1 = С; h2 — выход продукта в присутствии второго катализатора с концентрацией С2 = С; a1 и a2 — мольные доли компонентов в смеси.
Индивидуальная активность использованных катализаторов (h1 и h2) при Скат = 2∙10–3 моль/л, представлена в таблице 3.1.
Таблица 3.1
Активность межфазных катализаторов в системах «ж/ж» и «ж/т»
(Скат )о. ф. = 2·10–3моль/л, (СSub)о. ф. = 0,8 моль/л, t = 8 мин;
система «ж/т»: nKOH = 0,025 моль; dКОН ≤ 0,4 мм; Т = 70 °С.
система «ж/ж»: (СКОН)в. ф. = 13,45 моль/л (50 %-ный раствор);
Vо. ф. : Vв. ф.= 1 : 1; Vо. ф. = 4 мл; Vв. ф.= 4 мл; Т = 80 °С.
1 — a-бромстирол, 2 — b-бромстирол, 3 — фенилацетилен.
Катализатор | Система «ж/ж» | Система «ж/т» | ||||
a1, % | a2, % | a3, % | a1, % | a2, % | a3, % | |
--- | 2,8 | 0,0 | следы | 6,8 | 0,0 | следы |
ДДТМАБ | 59,5 | 2,1 | - // - | 58,4 | 2,0 | - // - |
ГДТМАБ | 65,8 | 2,2 | - // - | 65,5 | 2,1 | - // - |
ТОАБ | 20,6 | 2,1 | - // - | 76,5 | 2,9 | - // - |
ПЭГ | 18,0 | 1,5 | - // - | 83,3 | 3,2 | - // - |
Бензо-15-краун-5 | 3,5 | 0,0 | - // - | 33,1 | 2,2 | - // - |
В таблице 3.2 представлены данные по активности смесей солей тетраалкиламмония (ДДТМАБ, ГДТМАБ и ТОАБ) с такими катализаторами, как ПЭГ и бензо-15-краун-5, взятыми в равных количествах (для каждого катализатора (Скат)о. ф. = 1∙10–3 моль/л), а также рассчитанные коэффициенты kS.
Таблица 3.2
Активность смесей межфазных катализаторов в системах «ж/ж» и «ж/т»
(Скат1)о. ф. = (Скат2)о. ф. = 1·10–3 моль/л; (СSub)о. ф. = 0,8 моль/л; t = 8мин;
система «ж/т»: nKOH = 0,025 моль; dКОН ≤ 0,4 мм; Т = 70 °С.
система «ж/ж»: (СКОН)в. ф. = 13,45 моль/л (50 %-ный раствор);
Vо. ф. : Vв. ф.= 1 : 1; Vо. ф. = 4 мл; Vв. ф.= 4 мл; Т = 80 °С.
1 — a-бромстирол, 2 — b-бромстирол, 3 — фенилацетилен.
Катали-затор 1 | Катализатор 2 | Система «ж/ж» | Система «ж/т» | ||||||
a1,% | a2,% | a3,% | kS | a1,% | a2,% | a3,% | kS | ||
ДДТМАБ | ПЭГ | 61,1 | 2,1 | следы | 1,6 | 90,6 | 3,5 | следы | 1,3 |
Бензо-15-краун-5 | 62,6 | 2,2 | - // - | 2,0 | 91,7 | 3,5 | - // - | 2,0 | |
ГДТМАБ | ПЭГ | 68,1 | 2,2 | следы | 1,6 | 92,2 | 3,9 | следы | 1,2 |
Бензо-15-краун-5 | 69,5 | 2,3 | - // - | 2,0 | 93,5 | 4,6 | - // - | 1,9 | |
ТОАБ | ПЭГ | 23,3 | 2,1 | следы | 1,3 | 97,0 | 3,0 | следы | 1,2 |
Бензо-15-краун-5 | 23,5 | 2,1 | - // - | 2,1 | 92,3 | 4,8 | 2,9 | 1,8 |
Согласно данным табл. 3.2, все смеси имеют более высокую активность, чем индивидуальные компоненты, и для всех смесей наблюдается эффект синергизма действия: kS > 1.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |



