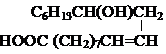С5Н5N > (С2Н5)3N > С2Н5(СН3)2N
По-видимому, это обусловлено тем, что в этом ряду уменьшение равновесной концентрации основания доминирует над увеличением его основности, также как это наблюдалось в случае карбоновых кислот и наиболее кислых фенолов.
2.3 Определение оптимального соотношения межфазного катализатора и спирта для получения синергетических композиций.
Как показано ранее (рис. 3.3), оптимальной для межфазных катализаторов, в частности солей тетраалкиламмония, в системах «ж/ж» и «ж/т» является концентрация (Скат)о. ф. = 1∙10–3 моль/л, соответствующая насыщению ПРФ. При получении смесей, обладающих синергетическим эффектом, целесообразно использовать два катализатора в равных количествах при суммарной концентрации 2∙10–3 моль/л (рис. 3.4 и 3.5).
Чтобы определить оптимальное соотношение количеств межфазного катализатора (соли тетраалкиламмония) и спирта при содержании основного катализатора 1∙10–3 моль/л, было проведено исследование влияния добавок 2‑метилбутанола-2 на эффективность реакции дегидробромирования 1,2‑дибром-1-фенилэтана в двухфазных системах «ж/ж» и «ж/т» в присутствии ГДТМАБ (рис. 3.6) и ТОАБ (рис. 3.7).
Как уже было отмечено ранее, все исследованные нами межфазные катализаторы, а также их смеси катализируют только первую стадию реакции дегидробромирования 1,2-дибром-1-фенилэтана с образованием основного продукта a‑бромстирола и практически неэффективны на второй стадии дегидробромирования, приводящей к образованию фенилацетилена.
Как видно из рис. 3.6, для смеси ГДТМАБ и спирта в системах «ж/т» характерна активность не только на первой стадии дегидробромирования 1,2‑дибром-1-фенилэтана, молекула которого имеет активированный протон в бензильном положении, но и на второй стадии дегидробромирования, включающей отщепление галогеноводорода от a - и b-бромстиролов, молекулы которых не содержат активированных протонов.
В присутствии смеси ГДТМАБ и 2-метилбутанола-2 (рис. 3.6) в системах «ж/ж» основным продуктом является a-бромстирол (кр. 1-а), также образуется небольшое количество фенилацетилена (кр. 2-а). В системах «ж/т» выход a-бромстирола снижается (кр. 1-б), а выход фенилацетилена увеличивается (2-б), что свидетельствует о более высокой активности систем «ж/т». Максимальный эффект синергетического действия наблюдается при концентрации спирта равной 1∙10–3 моль/л при (СГДТМАБ)о. ф. = 1∙10–3 моль/л.

В присутствии смеси ТОАБ и 2-метилбутанола-2 (рис. 3.7) активность систем «ж/т» также выше активности систем «ж/ж». В системах «ж/ж» оптимальной является добавка спирта в концентрации 1∙10–3 моль/л при условии (СТОАБ)о. ф. = 1∙10–3 моль/л (кр. 1а и 2а).
В системах «ж/т» эффективность превращения a-бромстирола в фенилацетилен возрастает с повышением концентрации спирта до 2∙10–3 моль/л (кр. 1б и 2б).

В дальнейшей работе по исследованию влияния соединений кислотно-основной природы на эффективность их смесей с классическими межфазными катализаторами — солями тетраалкиаммония, использовали смеси с суммарной концентрацией 2∙10–3 моль/л, при концентрации межфазного катализатора (Скат)о. ф. = 1∙10–3 моль/л и концентрации добавки (Ссокат.)о. ф. = 1∙10–3 моль/л.
2.4 Синергизм действия солей тетраалкиламмония и соединений кислотно-основной природы.
Данные по влиянию смеси солей тетраалкиламмония и соединений кислотно-основной природы на эффективность реакции дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т» представлены в таблицах 3.7 – 3.13.
Таблица 3.7
Выходы α-бромстирола (1), b-бромстирола (2) и фенилацетилена (3) в системах «ж/ж» в присутствии катализаторов межфазного переноса и карбоновых кислот: (Скат)о. ф. = 1×10–3 моль/л; (Скислоты)о. ф. = 1·10–3 моль/л, (СSub)о. ф. = 0,8 моль/л, t = 8мин; (СКОН)в. ф. = 13,45 моль/л (50 %-ный раствор); Vо. ф. = 4 мл;
Vо. ф. : Vв. ф. = 1 : 1; Vв. ф. = 4 мл; Т = 80 °С.
Катали-затор | № | Сокатализатор | 1 | 2 | 3 | kS | Dk∙102, мин–1 |
ДДТМАБ | 1 | — | 59,5 | 2,1 | следы | ||
2 | (CH3)2CHCH2COOH | 63,7 | 2,2 | - // - | 1,3 | 0,5 | |
3 | СН3(СН2)3СООН | 60,9 | 2,0 | - // - | 1,4 | 0,2 | |
4 | СН3(СН2)7СООН | 67,3 | 2,3 | - // - | 2,2 | 1,0 | |
5 | СН3(СН2)10СООН | 68,6 | 2,6 | - // - | 2,2 | 1,1 | |
6 | СН3(СН2)14СООН | 70,1 | 3,3 | - // - | 2,3 | 1,3 | |
7 |
| 72,4 | 3,4 | - // - | 2,4 | 1,6 | |
ГДТМАБ | 1 | — | 65,8 | 2,2 | следы | ||
2 | (CH3)2CHCH2COOH | 69,4 | 2,2 | - // - | 1,3 | 0,4 | |
3 | СН3(СН2)3СООН | 67,1 | 2,2 | - // - | 1,4 | 0,2 | |
4 | СН3(СН2)7СООН | 68,5 | 2,3 | - // - | 2,0 | 0,3 | |
5 | СН3(СН2)10СООН | 70,1 | 3,3 | - // - | 2,1 | 0,5 | |
6 | СН3(СН2)14СООН | 73,6 | 3,4 | - // - | 2,2 | 1,0 | |
7 |
| 74,4 | 3,4 | - // - | 2,2 | 1,1 |
Таблица 3.8
Выходы α-бромстирола (1), b-бромстирола (2) и фенилацетилена (3) в системах «ж/т» в присутствии катализаторов межфазного переноса и карбоновых кислот: (Скат)о. ф. = 1×10–3 моль/л; (Скислоты)о. ф. = 1·10-3 моль/л, (СSub)о. ф. = 0,8 моль/л; t = 8 мин; Vо. ф. = 4 мл; nKOH = 0,025 моль; dКОН ≤ 0,4 мм; Т = 70 °С.
Катали-затор | № | Сокатализатор | 1 | 2 | 3 | kS | Dk∙102, мин–1 |
ДДТМАБ | 1 | — | 58,4 | 2,0 | следы | ||
2 | (CH3)2CHCH2COOH | 78,5 | 3,2 | - // - | 1,8 | 2,5 | |
3 | СН3(СН2)3СООН | 73,1 | 3,0 | - // - | 1,9 | 1,8 | |
4 | СН3(СН2)7СООН | 80,2 | 3,5 | - // - | 2,2 | 2,7 | |
5 | СН3(СН2)10СООН | 81,4 | 3,6 | - // - | 2,2 | 2,9 | |
6 | СН3(СН2)14СООН | 82,3 | 3,9 | - // - | 2,2 | 3,0 | |
7 |
| 84,7 | 4,5 | - // - | 2,5 | 3,3 | |
ГДТМАБ | 1 | — | 65,5 | 2,1 | следы | ||
2 | (CH3)2CHCH2COOH | 70,4 | 2,7 | - // - | 1,5 | 0,6 | |
3 | СН3(СН2)3СООН | 66,4 | 2,3 | - // - | 1,6 | 0,1 | |
4 | СН3(СН2)7СООН | 90,2 | 3,5 | - // - | 2,2 | 3,1 | |
5 | СН3(СН2)10СООН | 91,4 | 3,5 | - // - | 2,3 | 3,2 | |
6 | СН3(СН2)14СООН | 92,3 | 3,9 | - // - | 2,3 | 3,4 | |
7 |
| 94,7 | 4,5 | - // - | 2,5 | 3,6 | |
ТОАБ | 1 | — | 76,5 | 2,9 | следы | ||
2 | (CH3)2CHCH2COOH | 84,9 | 3,9 | - // - | 1,6 | 1,1 | |
3 | СН3(СН2)3СООН | 78,7 | 3,6 | - // - | 1,7 | 0,3 | |
4 | СН3(СН2)7СООН | 93,1 | 4,0 | - // - | 2,0 | 2,1 | |
5 | СН3(СН2)10СООН | 95,1 | 4,3 | - // - | 2,1 | 2,3 | |
6 | СН3(СН2)14СООН | 95,3 | 4,5 | - // - | 2,1 | 2,3 | |
7 |
| 95,4 | 4,6 | - // - | 2,2 | 2,4 |
Таблица 3.9

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |