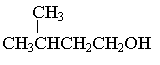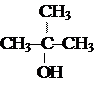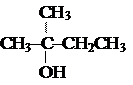п-NO2-C6H4OH > C6H5OH > м-CH3-C6H4OH < п-CH3-C6H4OH <
< о-CH3-C6H4OH
Таким образом, в системах «ж/т» в случае о- и п-крезолов, анионы которых являются более сильными основаниями, доминирующим фактором, влияющим на скорость дегидробромирования, становится увеличение величины константы скорости k, и, соответственно, каталитический эффект обусловлен фактором активности.
Данные по влиянию спиртов на эффективность реакции дегидробромирования в системах «ж/ж» и «ж/т» без межфазного катализатора представлены в таблице 3.5.
Таблица 3.5
Влияние спиртов на выход α-бромстирола (1), b-бромстирола (2) и фенилацетилена (3) в системах «ж/ж» и «ж/т» без катализатора межфазного переноса: (СSub)о. ф. = 0,8 моль/л, (Сспирта)о. ф. = 2·10–3моль/л, t = 8 мин.
система «ж/т»: nKOH = 0,025 моль; dКОН ≤ 0,4мм; Т = 70 °С.
система «ж/ж»: (СКОН)в. ф. = 13,45 моль/л (50 %-ный раствор);
Vо. ф. : Vв. ф.= 1 : 1; Vо. ф.= 4 мл; Vв. ф. = 4 мл; Т = 80 °С.
№ | Спирты | Kа для водного раствора | рKа | Система «ж/т» | Система «ж/т» | ||||
1 | 2 | 3 | 1 | 2 | 3 | ||||
1 | --- | – | – | 2,8 | 0,0 | следы | 6,8 | 0,0 | следы |
2 | CH3CH2OH | 1,26∙10–16 | 15,90 | 2,8 | - // - | - // - | 6,8 | - // - | - // - |
3 | CH3(CH2)2CH2OH | 8,64∙10–17 | 16,06 | 2,9 | - // - | - // - | 7,5 | - // - | - // - |
4 | CH3(CH2)3CH2OH | 8,23∙10–17 | 16,08 | 2,8 | - // - | - // - | 7,8 | - // - | - // - |
5 | CH3(CH2)4CH2OH | – | – | 2,8 | - // - | - // - | 8,0 | - // - | - // - |
6 | CH3(CH2)5CH2OH | – | – | 2,8 | - // - | - // - | 8,0 | - // - | - // - |
7 |
| 8,37∙10–17 | 16,08 | 2,8 | - // - | - // - | 10,1 | - // - | - // - |
8 | CH3CH(OH)CH3 | – | ~ 16 | 2,8 | - // - | - // - | 10,0 | - // - | - // - |
9 |
| – | – | 2,8 | - // - | - // - | 12,0 | - // - | - // - |
10 |
| – | – | 3,2 | - // - | - // - | 12,5 | - // - | - // - |
Согласно табл. 3.5, в системах «ж/ж» спирты не проявляют активности, поскольку доминирующим фактором, снижающим скорость реакции дегидробромирования, является, по-видимому, крайне низкая концентрация алкоголят-ионов, обусловленная малыми значениями Kа.
В системе «ж/т» этиловый спирт неактивен, но по мере уменьшения Kа, увеличения длины углеводородного радикала, перехода от первичных к вторичным и третичным спиртам каталитическая активность возрастает в ряду:
CH3CH2OH < CH3(CH2)2CH2OH < CH3(CH2)3CH2OH < CH3(CH2)4CH2OH
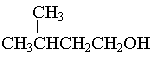 |
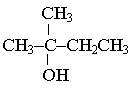
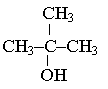 ≈ CH3(CH2)5CH2OH < ≈ CH3CH(OH)CH3 <
≈ CH3(CH2)5CH2OH < ≈ CH3CH(OH)CH3 <
< <
Следовательно, в этом ряду увеличение скорости реакции дегидробромирования вызвано тем, что снижение концентрации алкоголят-ионов на ПРФ компенсируется возрастанием константы скорости реакции, обусловленным увеличением основности этих ионов. Каталитическая активность спиртов в системах «ж/т» обусловлена фактором активности.
Таким образом, в отсутствие межфазного катализатора в обоих типах систем («ж/ж» и «ж/т») активность органических кислот уменьшается в ряду:
карбоновые кислоты > фенолы > спирты
Для всех кислот активность систем «ж/т» выше активности систем «ж/ж». Внутри каждого класса по мере уменьшения кислотности наблюдается следующие изменения каталитической активности: для карбоновых кислот — уменьшение активности; для фенолов — сначала уменьшение, а потом увеличение активности; для спиртов — увеличение активности.
2.2 Влияние аминов на эффективность дегидробромирования в системах «ж/ж» и «ж/т» в отсутствие межфазного катализатора.
Общую схему механизма действия органических оснований ( :В ) можно представить следующей схемой:
Схема 3.6
![]()
![]()
Соответственно, для скорости реакции дегидробромирования (ур. 3.14) можно записать следующее выражение:
W = k [:B]о. ф. [Sub]о. ф. (3.16)
При этом равновесная концентрация органического основания [:В] зависит от степени протекания межфазной реакции нейтрализации соответствующей ему кислоты ВН+Br− (ур. 3.16). С увеличением основности органического основания :В будет увеличиваться константа скорости реакции депротонирования k и уменьшаться равновесная концентрация [:В]о. ф.. Один из этих факторов может быть доминирующим.
В настоящей работе исследовано влияние аминов на эффективность реакции дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т» (табл. 3.7).
Согласно данным табл. 3.7, в системах «ж/ж» амины не влияют на скорость реакции дегидробромирования, что может быть обусловлено тем, что они растворимы в щелочной водной фазе, что, в свою очередь, приводит к снижению их эффективной концентрации в органической фазе.
В системах «ж/т» амины проявляют заметную активность. Поскольку их основность ниже, чем основность гидроксида калия, каталитическая активность обусловлена тем, что эффективность дегидробромирования субстрата в органической фазе под действием более слабого основания (ур. 3.14) выше, чем эффективность межфазной реакции дегидробромирования субстрата под действием более сильного основания КОН (ур. 3.14).
Таблица 3.6
Влияние аминов на выход α-бромстирола (1), b-бромстирола (2) и фенилацетилена (3) в системах «ж/ж» и «ж/т» без катализатора межфазного переноса:
(СSub)о. ф. = 0,8 моль/л; (Самина)о. ф. = 2·10–3моль/л; t = 8 мин.
система «ж/т»: nKOH = 0,025 моль; dКОН ≤ 0,4 мм; Т = 70 °С.
система «ж/ж»: (СКОН)в. ф. = 13,45 моль/л (50 %-ный раствор);
Vо. ф. : Vв. ф.= 1 : 1; Vо. ф.= 4 мл; Vв. ф. = 4 мл; Т = 80 °С.
№ | Амины | Kа для водного раствора | рKа | Система «ж/т» | Система «ж/т» | ||||
1 | 2 | 3 | 1 | 2 | 3 | ||||
1 | --- | – | – | 2,8 | 0,0 | следы | 6,8 | 0,0 | следы |
2 | С5Н5N | 6,17∙10–6 | 5,21 | 2,8 | - // - | - // - | 35,5 | 1,3 | - // - |
3 | (С2Н5)3N | 9,77∙10–12 | 11,01 | 2,8 | - // - | - // - | 30,4 | 1,3 | - // - |
4 | С2Н5(СН3)2N | – | – | 2,8 | - // - | - // - | 25,6 | 1,2 | - // - |
В системах «ж/т» активность аминов уменьшается с уменьшением величины Kа в ряду:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |