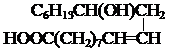При подборе оптимальных композиций необходимо учитывать индивидуальную активность межфазных катализаторов и коэффициент синергизма их действия. Для реакции дегидробромирования 1,2-дибром-1-фенилэтана в системе «ж/ж» наиболее эффективной является композиция из равных количеств ГДТМАБ и эфира бензо-15-краун-5, а в системе «ж/т» — композиция из равных количеств ТОАБ и ПЭГ.
Полученные результаты позволяют предположить, что аналогичные эффекты сокатализа и синергизма действия могут наблюдаться при использовании классических межфазных катализаторов — солей тетраалкиламмония с добавками органических оснований, таких как амины, соли алкилкарбоновых кислот, феноляты и алкоголяты щелочных металлов вместо дорогостоящих и менее доступных краун-эфиров и полиэтиленгликолей.
III.2 Каталитическая активность соединений кислотно-основной природы и синергизм действия их смесей с катализаторами межфазного переноса в реакции дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т».
В данном разделе рассмотрено влияние добавок карбоновых кислот, фенолов, спиртов и аминов на эффективность действия межфазных катализаторов, таких как ДДТМАБ, ГДТМАБ и ТОАБ на примере реакции дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т».
Согласно литературным данным [Никольский, Т. 3. С. 108], интервалы значений рKа для органических соединений различных классов в водных растворах составляют:
для одноосновных жирных кислот — 4,4 ¸ 5,0;
для алкилзамещенных фенолов — 9,2 ¸ 11,0;
для предельных аминов (•HX) — 9,8 ¸ 11,2;
для ароматических аминов (•HX) — 3,2 ¸ 7,2;
для спиртов — 15,9 ¸ 16,4.
Таким образом, активность органических оснований различных классов должна увеличиваться в ряду:
карбоксилат-ионы < фенолят-ионы < амины < алкоголят-ионы,
что позволяет изучить влияние органических оснований различной основности на эффективность межфазного катализа в присутствии солей тетраалкиламмония.
Для выявления эффекта синергизма действия смесей межфазного катализатора — солей тетраалкиламмония и соединений кислотно-основной природы — необходимо установить наличие каталитической активности в реакции дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т» для карбоновых кислот, фенолов, аминов и спиртов в отсутствие межфазного катализатора.
2.1 Влияние карбоновых кислот, фенолов и спиртов на эффективность дегидробромирования в системах «ж/ж» и «ж/т» в отсутствие межфазного катализатора.
Данные по влиянию карбоновых кислот, фенолов и спиртов на выход продуктов реакции дегидробромирования 1,2-дибром-1-фенилэтана за 8 минут в системах «ж/ж» и «ж/т» представлены в таблицах 3.3 – 3.5.
В отсутствие добавок кислот межфазная реакция дегидробромирования протекает неэффективно и в системах «ж/ж» (выход a‑бромстирола 2,8 %), и в системах «ж/т» (выход a-бромстирола 6,8 %):
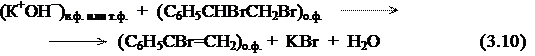
Согласно данным табл. 3.3 – 3.5, карбоновые кислоты, фенолы и спирты в большинстве случаев проявляют каталитическую активность как в системах «ж/ж», так и в системах «ж/т».
Общую схему механизма действия протонодонорных органических кислот можно представить следующим образом:
Схема 3.5
![]()
![]()
При добавлении кислот, фенолов и спиртов в системы, содержащие водный раствор щелочи или твердую щелочь, образование органических оснований происходит in situ в соответствии с уравнением нейтрализации соответствующих кислот (НА) (ур. 3.11). Поскольку из щелочной водной фазы органические соединения практически полностью высаливаются, органические кислоты будут локализованы в органической фазе, а их более гидрофильные соли — на ПРФ. Следовательно, следующая стадия взаимодействия основания с субстратом должна происходить на ПРФ (ур. 3.12).
Для скорости реакции дегидробромирования в расчете на единицу объема органической фазы можно записать следующее выражение:
![]()
В первом приближении можно считать, что константа межфазного равновесия Kр (ур. 3.11) пропорциональна силе кислоты, в водных растворах, характеризуемой величиной константы диссоциации (Kа). Следовательно, при использовании органических кислот, фенолов и спиртов в равных количествах концентрация основания [К+А−] будет тем меньше, а его активность при взаимодействии с субстратом (ур. 3.12) тем больше, чем меньше константа диссоциации соответствующей кислоты Kа. Следовательно, в соответствии с уравнением 3.13, при уменьшении силы кислоты изменение скорости реакции дегидробромирования (W) будет определяться двумя противоположными факторами: увеличением константы скорости реакции k и уменьшением концентрации основания [К+А−]ПРФ.
Соответственно, каталитический эффект, а именно, выгодность маршрута дегидробромирования субстрата по схеме 3.5, по сравнению с межфазной реакцией дегидробромирования субстрата щелочью (ур. 3.10), может быть обусловлена двумя причинами. Для кислот, у которых Kа > KW, а основность сопряженного основания А− меньше основности ОН−, каталитический эффект обусловлен концентрационным фактором, т. е. эффектом концентрирования основания на ПРФ за счет поверхностной активности соответствующей соли К+А−.
Для кислот, у которых Kа < KW, а основность сопряженного основания А− больше основности ОН−, каталитический эффект обусловлен фактором активности, т. е. повышением константы скорости реакции дегидробромирования k.
В таблице 3.4 представлены данные по влиянию карбоновых кислот на выход продуктов дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т» без межфазного катализатора в зависимости от значений Kа и рKа для водных растворов, рассчитанных по корреляционным уравнениям Гаммета [118] для соединений с известными значениями индукционными постоянных Тафта.
Таблица 3.3
Влияние карбоновых кислот на выход α-бромстирола (1), b-бромстирола (2) и фенилацетилена (3) в системах «ж/ж» и «ж/т» без катализатора межфазного переноса: (СSub)о. ф. = 0,8 моль/л, (Скислоты)о. ф. = 2·10–3моль/л, t = 8 мин.
система «ж/т»: nKOH = 0,025 моль; dКОН ≤ 0,4мм; Т = 70 °С.
система «ж/ж»: (СКОН)в. ф. = 13,45 моль/л (50 %-ный раствор);
Vо. ф. : Vв. ф.= 1 : 1; Vо. ф.= 4 мл; Vв. ф.= 4 мл; Т = 80 °С.
№ | Карбоновые кислоты | Kа для водного раствора | рKа | Система «ж/т» | Система «ж/т» | ||||
1 | 2 | 3 | 1 | 2 | 3 | ||||
1 | - - - | – | – | 2,8 | 0,0 | следы | 6,8 | 0,0 | следы |
2 | (CH3)2CHCH2COOH | 1,67·10–5 | 4,78 | 36,5 | 1,3 | - // - | 30,2 | 0,5 | - // - |
3 | СН3(СН2)3СООН | 1,40·10–5 | 4,86 | 30,4 | 0,3 | - // - | 20,2 | 0,2 | - // - |
4 | СН3(СН2)7СООН | 1,11·10–5 | 4,96 | 2,8 | 0,0 | - // - | 16,6 | 0,0 | - // - |
5 | СН3(СН2)10СООН | 1,10·10–5 | 4,95 | 2,8 | 0,0 | - // - | 16,2 | 0,0 | - // - |
6 | СН3(СН2)14СООН | – | – | 2,8 | 0,0 | - // - | 16,4 | 0,0 | - // - |
7 |
| – | – | 2,8 | 0,0 | - // - | 11,0 | 0,0 | - // - |
Как видно из данных табл. 3.3 активность исследованных карбоновых кислот зависит от эффективности стадии их нейтрализации (ур. 3.11). Активность систем «ж/т» выше активности систем «ж/ж», так как низкое содержание воды в системе «ж/т» приводит к смещению равновесия стадии нейтрализации вправо. Уменьшение каталитической активности кислот как в системах «ж/т», так и в системах «ж/ж» коррелирует с уменьшением константы равновесия Kр, которое обусловлено уменьшением констант диссоциации кислот Kа и увеличением их липофильности, которая в свою очередь уменьшает их сродство к полярной фазе и затрудняет межфазную реакцию нейтрализации, в ряду:
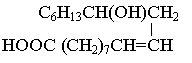 (CH3)2CHCH2COOH > СН3(СН2)3СООН > СН3(СН2)7СООН >
(CH3)2CHCH2COOH > СН3(СН2)3СООН > СН3(СН2)7СООН >
> СН3(СН2)10СООН > СН3(СН2)14СООН >
Таким образом, в ряду карбоновых кислот, которые из всех классов органических соединений, изученных в работе, генерируют самые слабые основания — карбоксилат-ионы, уменьшение скорости реакции дегидробромирования субстрата коррелирует с уменьшением концентрации основания [К+А−]ПРФ, а не с увеличением константы скорости реакции k. Каталитический эффект карбоновых кислот обусловлен концентрационным фактором.
В таблице 3.4 представлены данные по влиянию фенолов на эффективность реакции дегидробромирования 1,2-дибром-1-фенилэтана в системах «ж/ж» и «ж/т» без межфазного катализатора в зависимости от значений Kа и рKа [118].
Согласно данным табл. 3.4 в присутствии фенолов активность систем «ж/т» выше активности систем «ж/ж». В системах «ж/ж» снижение активности фенолов коррелирует с уменьшением величины константы диссоциации Kа в ряду:
п-NO2-C6H4OH > C6H5OH >
> м-CH3-C6H4OH ≈ п-CH3-C6H4OH ≈ о-CH3-C6H4OH
В этом случае, также как и в случае карбоновых кислот, доминирующим фактором, влияющим на скорость реакции дегидробромирования, является уменьшение концентрации основания [К+А−]ПРФ, а не увеличение основности фенолят-ионов и, соответственно, константы скорости реакции k, т. е. каталитический эффект обусловлен концентрационным фактором.
Таблица 3.4
Влияние фенолов на выход α-бромстирола (1), b-бромстирола (2) и фенилацетилена (3) в системах «ж/ж» и «ж/т» без катализатора межфазного переноса: (СSub)о. ф. = 0,8 моль/л; (Сфенола)о. ф. = 2·10-3 моль/л; t = 8 мин.
система «ж/т»: nKOH = 0,025 моль; dКОН ≤ 0,4мм; Т = 70 °С.
система «ж/ж»: (СКОН)в. ф. = 13,45 моль/л (50 %-ный раствор);
Vо. ф. : Vв. ф.= 1 : 1; Vо. ф.= 4 мл; Vв. ф.= 4 мл; Т = 80 °С.
№ | Фенолы | Kа для водного раствора | рKа | Система «ж/т» | Система «ж/т» | ||||
1 | 2 | 3 | 1 | 2 | 3 | ||||
1 | - - - | – | – | 2,8 | 0,0 | следы | 6,8 | 0,0 | следы |
2 | п-NO2-C6H4OH | 7,1·10–8 | 7,15 | 24,4 | - // - | - // - | 27,6 | - // - | - // - |
3 | C6H5OH | 1,0·10–10 | 10,0 | 14,5 | - // - | - // - | 15,4 | - // - | - // - |
4 | м-CH3-C6H4OH | 8,1·10–11 | 10,09 | 2,8 | - // - | - // - | 7,9 | - // - | - // - |
5 | п-CH3-C6H4OH | 5,5·10–11 | 10,26 | 2,8 | - // - | - // - | 11,2 | - // - | - // - |
6 | о-CH3-C6H4OH | 5,2·10–11 | 10,29 | 2,8 | - // - | - // - | 12,0 | - // - | - // - |
В системах «ж/т» (табл. 3.4) наблюдается экстремальная зависимость активность от Kа, активность фенолов уменьшается в ряду:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |