Реактивы:
1) биуретовый реактив 3,5 г растворить в 250 мл дистиллированной воды;
2) стандартный раствор с содержанием белка 2,5; 5,0 и 7,5 мг в 1 мл;
Ход работы.
1. В 4 пробирки вносят по 1 мл раствора белка. В первый три пробирки помещают стандартные растворы белка с известной концентрацией. В четвертую пробирку наливают раствор с неизвестной концентрацией белка, которую нужно определить.
2. В каждую пробирку добавляют по 4 мл биуретового реактива. Содержимое пробирок хорошо перемешивают и оставляют на 20 минут при комнатной температуре для развития окраски. Окрашенные растворы колориметрируют на ФЭКе в кюветах с толщиной 1 см, при длине волны 540 нм (зеленый светофильтр). В качестве контрольного раствора используют биуретовый реактив.
3. Стоят калибровочную кривую, откладывая по оси абсцисс концентрации стандартных растворов белка, а на оси ординат – соответствующие значения оптической плотности. Пользуясь этой кривой и зная оптическую плотность раствора белка с неизвестной концентрацией, определяют в нем содержание белка.
Вывод:____________________________________________________________________________________________________________________________________________________
Лабораторная работа № 4
Реакции осаждения белков
Реакции осаждения белков могут быть обратимыми и необратимыми. В первом случае белки не подвергаются глубоким изменениям, поэтому получаемые осадки могут быть вновь растворены в первоначальном растворителе с сохранением своих нативных свойств. При необратимых реакциях осажденные белки подвергаются глубоким изменениям — денатурации.
Реакции осаждения дают возможность:
1) изучить свойства белков;
2) освободить жидкость от присутствия белка;
3) установить наличие белка в биологических жидкостях, например в моче;
4) высаливанием с помощью различных концентраций нейтральных солей или спиртом выделить отдельные белковые фракции.
Осаждение белков при кипячении
Принцип метода. Для осаждения белка необходимо разрушить его гидратную оболочку и нейтрализовать его заряд. При кипячении происходит денатурация, поэтому разрушается гидратная оболочка. Белок теряет заряд, если рН раствора близок к изоэлектрической точке этого белка.
Реактивы:
1) 1 % раствор яичного белка;
2) 1 % раствор уксусной кислоты;
3) 10 % раствор NaOH;
4) насыщенный раствор NaCI;
Ход работы.
В 5 пробирок вносят по 5 капель 1 % раствора яичного белка.
Затем добавляют:
во вторую пробирку - 1 каплю уксусной кислоты;
в третью - 10 капель уксусной кислоты;
в четвертую - 5 капель уксусной кислоты и 2 капли насыщенного раствора NaCI;
в пятую - 2 капли NaОН.
Все пробирки кипятят 5 минут в водяной бане. Результаты оформляют в виде таблицы
Результат:
№ пробирки | Ход анализа, реакция среды | Наличие осадка (есть или нет) | Произошла ли денатурация (да или нет) | Наличие факторов стабилизации | |
Гидратная оболочка (есть или нет) | Заряд (если есть заряд, указать его знак) | ||||
1 | Нагреть до кипения, нейтральная | ||||
2 | Нагреть до кипения + слабокислая | ||||
3 | Сильнокислая + нагреть до кипения, | ||||
4 | Кислая +электролит + нагреть до кипения | ||||
5 | Щелочная + нагреть до кипения, |
Вывод:______________________________________________________________________
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Осаждение белков концентрированными минеральными кислотами
Принцип метода. Минеральные кислоты вызывают дегидратацию белковых частиц и образуют комплексные соли с белками. Осадок белка растворяется в избытке кислоты, за исключением азотной кислоты. Это позволяет использовать азотную кислоту при клинических исследованиях для количественного определения белков.
Реактивы:
1) концентрированная HNO3;
2) концентрированная H2SO4;
3) 1 % раствор яичного белка.
Ход работы. В пробирку вносят 10 капель концентрированной азотной кислоты, затем осторожно из пипетки наслаивают по стенке пробирки примерно 10 капель раствора белка так, чтобы жидкости не смешивались. Наблюдают, как на границе двух жидкостей образуется белое мутное кольцо. Пробирку встряхивают и добавляют избыток азотной кислоты. Осадок не растворяется. Проделывают то же самое с серной кислотой. Осадок при этом растворяется.
Результат: ___________________________________________________________________
__________________________________________________________________________________________________________________________________________________________
Вывод: ______________________________________________________________________
__________________________________________________________________________________________________________________________________________________________
Осаждение белков органическими кислотами
Принцип метода. Как и неорганические кислоты, трихлоруксусная, сульфосалициловая и другие органические кислоты, вызывая дегидратацию и образуя комплексные соли, денатурируют белки.
Реактивы:
1) 1 % раствор яичного белка;
2) 10 % раствор ССI3СООН;
3) 20 % раствор сульфосалициловой кислота С6Н3(ОН)(СООН)SО3Н.
Ход работы. В пробирку наливают 5 капель раствора белка, затем добавляют 2 капли трихлоруксусной кислоты 10 % раствора ССI3СООН (ТХУ) (агрессивная жидкость!) или 2 капли 20 % раствора сульфосалициловой кислота С6Н3(ОН)(СООН)SО3Н и наблюдают появление осадка белка.
Результат: ___________________________________________________________________
__________________________________________________________________________________________________________________________________________________________
Вывод: ______________________________________________________________________
__________________________________________________________________________________________________________________________________________________________
Растворимость белков
Принцип метода. Многие белки хорошо растворяются в воде, что обусловлено наличием па поверхности белковой молекулы свободных гидрофильных групп (-ОН, - NН2, - СООН и др.). Различные белки растворяются по-разному; белки опорных тканей (кератин, проколлаген, коллаген, эластин и др.) нерастворимы в воде.
Растворимость белка в воде зависит от характера белка, реакции среды и присутствия электролитов. В кислой среде лучше растворяются белки, обладающие кислыми свойствами (альбумины, глобулины, проламины, глютелины), щелочные белки (протамины и гистоны) лучше растворяются в щелочной среде.
Различия в растворимости отмечаются как среди кисло-, так и среди щелочно-реагирующих белков. Например, альбумины растворяются в дистиллированной воде, а глобулины растворяются в воде только в присутствии электролитов.
Реактивы:
1) разведенный яичный белок;
2) 5 % раствор NaCI;
3) кератин.
Ход работы. В одну пробирку вносят 2 капли не разведенного яичного белка, 20 капель воды, содержимое перемешивают. При этом яичный альбумин растворяется, а яичный глобулин выпадает в виде небольшого осадка. В другую пробирку вносят 2 капли яичного белка и 20 капель 5% раствора хлорида натрия. В слабом солевом растворе растворяются и альбумины, и глобулины.
В две другие пробирки помещают небольшое количество кератина (волосы). В одну пробирку вносят 20 капель воды, в другую — 20 капель 5% раствора хлорида натрия. Кератин не растворяется ни в воде, ни в солевом растворе.
Результат:
Название белка | Н2О | 5 % NaCI |
Яичный альбумин | ||
Яичный глобулин | ||
Кератин |
Вывод:______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
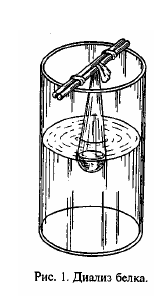
Очистка белков методом диализа
Принцип метода Диализ — освобождение коллоидов от низкомолекулярных органических и минеральных примесей с помощью диффузии последних через мембраны. Белки в растворе благодаря значительной величине молекул не диффундируют сквозь полупроницаемую мембрану.
Реактивы:
1) 1 % раствор яичного белка с примесью NaCI;
2) 10 % раствор NaOH;
3) 1 % раствор CuSO4.
Ход работы: Наливают 15—20 мл исследуемого солевого раствора белка в целлофановый мешочек (диализатор) и погружают его в стакан с дистиллированной водой таким образом, чтобы открытый край мешочка выступал над поверхностью воды. Через 1 час с водой из стакана (диализата – наружная жидкость) и раствора белка (диализируемая жидкость), проделывают биуретовую реакцию (на белок) и реакцию на хлориды, чтобы убедиться в отсутствии белка и наличии минеральных солей в воде из стакана.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |



