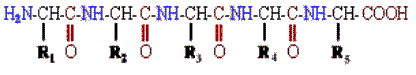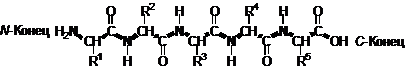ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ РОССИЙСКОЙ ФЕДЕРАЦИИ
КАРАЧАЕВО-ЧЕРКЕССКАЯ ГОСУДАРСТВЕННАЯ
ТЕХНОЛОГИЧЕСКАЯ АКАДЕМИЯ
Кафедра химии и биологии
ПРАКТИКУМ ПО БИОХИМИИ
для студентов II курса
лечебного факультета
Черкесск
2007
ВВЕДЕНИЕ
В данном практикуме изложены методики учебных лабораторных работ и некоторых современных биохимических методов исследования, выполняемых студентами на занятиях по биохимии. Проведение лабораторных работ позволит осмыслить теоретический материал, рассмотреть особенности строения и свойства вещества.
Методические указания могут быть использованы студентами лечебного факультета для самостоятельной, учебно - и научно-исследовательской работы.
I.ТЕМА: Вводное занятие
Лабораторная работа № 1.
Особенности работы в биохимической лаборатории и инструктаж по технике безопасности:
1. Работать разрешается только в халате с длинными рукавами.
2. Длинные волосы должны быть аккуратно убраны.
3. Выполнять лабораторную работу разрешается только на химическом столе. На химический стол нельзя класть одежду, учебники и другие ценные вещи.
4. Работа с биологическим материалом должна выполняться в медицинских перчатках.
5. Работать с агрессивными жидкостями (концентрированные кислоты, щелочи и др.) допускается только строго отвеченном для этого месте (вытяжной шкаф).
6. Использовать реагенты, маркировка которых указана на этикетке.
7. Отмеривать такие жидкости необходимо с большой осторожностью следующими способами:
а) с помощью мерного цилиндра;
б) с помощью пипетки с грушей;
в) с помощью стеклянной пипетки. Опустить пипетку в жидкость, после заполнения пипетки жидкостью плотно закрыть верхний конец указательным пальцем, перенести пипетку с жидкостью в пробирку. Осторожно приоткрыть конец пипетки и отмерить жидкость.
Внимание! Запрещается при отмеривании агрессивных жидкостей заполнять ими пипетку путем засасывания ртом. Так можно вызвать повреждение зубной эмали, ожог слизистой оболочки ротовой полости и пищевода.
8. Если на кожу, слизистые оболочки или в глаза попала агрессивная жидкость, немедленно смыть ее большим количеством воды и обратиться и лаборантскую службу кафедры.
9. Не нагревать посуду из простого химического стекла на открытом пламени.
10. Следить за тем, чтобы вода и другие жидкости не попадали в электрические приборы.
11. В лабораторные центрифуги помещать парное (четное) количество тщательно уравновешенных пробирок. Роторная камера может быть открыта только после полной остановки ротора.
12. Работу на измерительной аппаратуре следует проводить в присутствии преподавателя или ответственного лаборанта кафедры.
13. Необходимо аккуратно обращаться с лабораторной посудой, чтобы в случае ее повреждения не получить травму.
14. После завершения работы убрать рабочее место, отключить электричество, а также убедиться, что краны холодной и горячей воды закрыты.
II.ТЕМА: СТРОЕНИЕ И СВОЙСТВА БЕЛКОВ
Белки представляют собой высокомолекулярные полимерные органические соединения, построенные из α-аминокислот. Аминокислоты соединены меду собой пептидными связями (-СО-NН-), образуя полипептидные цепи. Пептидная связь формируется только за счет α–NH2 группы одной и COOH-группы другой аминокислоты у α -углеродного атома.
|
|
В белках различают первичную структуру (последовательность аминокислотных остатков, соединенных между собой при помощи пептидных связей), вторичную структуру (возникает за счет образования водородных связей между группами =N-H и O=C= данной полипептидной цепи, что приводит к расположению полипептидной цепи в виде спиральной или складчатой структуры), третичную структуру (возникает в результате взаимодействия между боковыми цепями аминокислотных остатков полипептидных цепей), четвертичную структуру (межмолекулярные взаимодействия между отдельными полипептидными цепями).
Лабораторная работа № 2.
КАЧЕСТВЕННЫЕ РЕАКЦИИ
Для проведения качественной реакции к исследуемому веществу прибавляют реагент, способный взаимодействовать с определенной химической группой. Если исследуемое вещество содержит такую группу, происходит реакция, в результате которой наблюдается, либо изменение цвета, либо выпадение осадка, либо появление характерного запаха. В этом случае реакцию можно считать положительной и сделать вывод о наличии данной группы в составе исследуемого вещества. Если изменений не происходит (отрицательная реакция), то вещество не содержит искомой группы.
Качественные реакции на белки и аминокислоты
Присутствие белка в биологических жидкостях можно обнаружить с помощью качественных (цветных) реакций. Можно выделить универсальные цветные реакции (биуретовая, нингидриновая), которые дают вещества, содержащие не менее двух пептидных связей, и специфические реакции, которые обусловлены наличием только определенных аминокислот в молекуле белка (ксантопротеиновая, Миллона, Фоля и др.)
Биуретовая реакция на пептидные связи
Принцип метода: Группировки - СО-NН-, входящие в пептидную связь, в щелочной среде образуют комплексные соединения с ионами меди (Сu+2). Полученные соединения окрашены в фиолетовый цвет с красным или синим оттенком в зависимости от длины полипептидной цепи. Раствор белка дает сине-фиолетовое окрашивание, а продукты неполного его гидролиза – розовое или красное.
Реактивы:
1) 1 % раствор яичного белка (белок куриного яйца фильтруют через марлю и разводят водой 1:10);
2) 1 % раствор желатина;
3) 10 % раствор NaOH;
4) 1 % раствор CuSO4.
Ход работы. Берут 3 пробирки: в первую внося 5 капель 1 % раствора яичного белка, во вторую – 5 капель 1 % раствора желатина, в третью - 5 капель воды. Затем в каждую пробирку добавляют по 5 капель 10 % NaOH и по 2 капли 1 % CuSO4. Пробирки встряхивают. Наблюдают за изменением окраски.
Результат:
Первая пробирка: _____________________________________________________________
_____________________________________________________________________________Вторая пробирка: ______________________________________________________________
_____________________________________________________________________________
Третья пробирка: ______________________________________________________________
_____________________________________________________________________________
Вывод: ______________________________________________________________________
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Нингидриновая реакция на a-аминокислоты
Принцип метода. Раствор белка при нагревании с разбавленным раствором нингидрина окрашивается в синий или фиолетовый цвет. Реакция обусловлена наличием в белке остатков а-аминокислот. При взаимодействии с нингидрином а-аминокислоты и пептиды окисляются и распадаются с образованием NH3, R-COH и CO2. Нингидрин восстанавливается и взаимодействует со второй молекулой нингидрина и аммиаком. В результате образуется сложное соединение мурексидного строения, окрашенное в синий или фиолетовый цвет (комплекс Руэмана). Нингидриновая реакция может быть использована для количественного определения а-аминокислот в аминокислотных анализаторах.
Реактивы:
1) 1 % раствор яичного белка;
2) 1 % раствор желатина;
3) 0,5 % раствор нингидрина.
Ход работы. Берут 3 пробирки; в первую вносят 5 капель 1 % раствора яичного белка, во вторую - 5 капель 1 % желатина, в третью - 5 капель воды. В каждую пробирку добавляют по 5 капель 0,5 % раствора нингидрина. Кипятят 2 минуты в водяной бане. Следят за изменением окраски.
Результат:
Первая пробирка: _____________________________________________________________
_____________________________________________________________________________Вторая пробирка: ______________________________________________________________
_____________________________________________________________________________
Третья пробирка: ______________________________________________________________
_____________________________________________________________________________
Вывод: ______________________________________________________________________
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Ксантопротеиновая реакция на циклические аминокислоты
Принцип метода. При смешивании раствора белка с концентрированной азотной кислоты белок сначала выпадает в осадок, при последующем нагревании растворяется и жидкость окрашивается в желтый цвет. Аминокислоты, имеющие в своем составе бензольное кольцо (фен, тир, три), вступают с азотной кислотой в реакцию нитрования с образованием нитросоединений желтого цвета.
Реактивы:
1) 1 % раствор яичного белка;
2) 1 % раствор желатина;
3) азотная кислота концентрированная (HNO3).
Ход работы. Берут 3 пробирки: в первую вносят 5 капель 1 % раствора яичного белка, во вторую – 5 капель 1 % желатина, в теретью - 5 капель воды. Затем в каждую пробирку добавляют по 5 капель концентрированной азотной кислоты (HNO3 - агрессивная жидкость!). Кипятят 2 минуты в водяной бане. Регистрируют изменение цвета.
Результат:
Первая пробирка: _____________________________________________________________
_____________________________________________________________________________Вторая пробирка: ______________________________________________________________

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |