а) п. 1. Дано:
CnH2n–2,
M(CnH2n–2Cl4) = 21,0 г,
M(CnH2n–2Br4) = 38,8 г. Найти: химическая формула – ?
б) п. 2. CnH2n–2 + 2Сl2 = CnH2n–2Сl4,
CnH2n–2 + 2Br2 = CnH2n–2Br4.
в) п. 3. 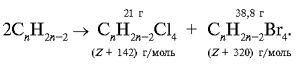
Обозначим M(CnH2n–2) = Z.
Решаем полученную пропорцию: 21/(Z + 142) = 38,8/(Z + 320), Z = 68.
Найдем индекс n: M(CnH2n–2) = 12n + 2n – 2,
12n + 2n – 2 = 68, n = 5. Ответ. С5Н8.
Алгоритм 2. Насыщенные растворы
1. Записать, что дано и что необходимо найти.2. Составить первую пропорцию, используя определение коэффициента растворимости Краств3. Составить вторую пропорцию, исходя из первой и данных задачи:

Решить пропорцию относительно х. Записать ответ (при решении обратных задач составляется такая же схема)Для газов растворимость понижается при нагревании. Растворимость (коэффициент растворимости Kраств) – количество вещества (в г), которое может раствориться в 100 г растворителя при определенной температуре, образуя насыщенный раствор.
Пример 1. Коэффициент растворимости соли при температуре 50 °С равен 40 г, при температуре 10 °С составляет 15 г. Определите массу осадка, полученного при охлаждении насыщенного при температуре 50 °С раствора массой 70 г до температуры 10 °С.
а) п. 1. Дано:
Kраств(соли) при t = 50 °С – 40 г,
Kраств(соли) при t = 10 °С – 15 г,
m(насыщ. р-ра) при t = 50 °С – 70 г. Найти: m (осадка) при 10 °С – ?
б) п. 2.
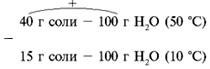
в) п. 3.
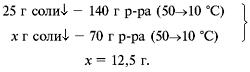
Ответ. m(осадка) при охлаждении равна 12,5 г.
Пример 2. При н. у. в воде массой 100 г растворяется хлороводород объемом 50,5 л. При температуре 50 °С и нормальном давлении коэффициент растворимости хлороводорода равен 59,6 г. Насыщенный при температуре 0 °С раствор HCl массой 40 г нагрели до температуры 50 °С. Определите массу полученного раствора.
а) п. 1. Дано:
V(HCl) = 50,5 л (н. у.),
Kраств(HCl) = 59,6 г (50 °С, 1 атм),
m(насыщ. р-ра) = 40 г (0 °С). Найти: m(р-ра HCl) – ?
б) п. 2.
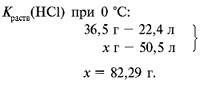
в) п. 3.

5 г HCl улетучится при нагревании. Ответ. m(полученного р-ра HCl) = 40 – 5 = 35 г.
Пример 3. В воде массой 100 г растворяется при температуре 30 °С бромид аммония массой 81,8 г. При охлаждении насыщенного при температуре 30 °С раствора NH4Br массой 300 г до температуры 0 °С выпадает в осадок соль массой 36,8 г. Определите, какая масса бромида аммония может быть растворена в воде массой 100 г при t = 0 °С.
а) п. 1. Дано:
Kраств = 81,8 г (30 °С),
m(насыщ. р-ра) = 300 г (30 °С),
m(осадка) = 36,8 г (0 °С). Найти: K'раств(0 °С) – ?
б) п. 2.

Ответ. K'раств(0 °С) = 59,5 г.
Алгоритм 3.
Расстановка коэффициентов методом полуреакций
(электронно-ионный баланс)
1. В уравнении окислительно-восстановительной реакции определить элементы, которые меняют степень окисления.
2. Составить электронно-ионный баланс с учетом среды:
– малодиссоциирующие вещества, недиссоциирующие вещества на ионы не расписывают;
– в кислой среде в реакции могут участвовать Н+ и Н2О;
– в щелочной среде – ОН– и Н2О;
– в нейтральной среде – Н2О, Н+ и ОН–.
3. Записать сокращенное ионное уравнение согласно электронно-ионному балансу:
– суммировать процессы окисления и восстановления с учетом равенства электронов в этих процессах;
– сократить справа и слева в химическом уравнении одинаковые ионы, молекулы.
4. Записать уравнение в молекулярной форме по ионному уравнению, дописать формулы веществ, которые в электронно-ионном балансе не были задействованы.
5. Проверить коэффициенты в молекулярном уравнении.
Пример 4. Расставить коэффициенты методом электронно-ионного баланса: H2S + K2Cr2O7 + H2SO4 = S Cr2(SO4)3 + H2O + K2SO4.
а) п. 1.
![]()
б) п. 2.
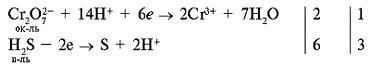
в) п. 3.
![]()
г) п. 4, п. 5. Ответ. 3H2S + K2Cr2O7 + 4H2SO4 = 3S + Cr2(SO4)3 + 7H2O + K2SO4.
http://him.1september. ru/
Тексты задач и практических ситуаций
для самостоятельного решения при подготовке к итоговой аттестации
Расчетные задачи.
А. Задачи на определение молекулярных масс веществ в газовом состоянии, на молярный объем, закон Авогадро:
1. Плотность газа по воздуху 3,5. Найти массу молекулы газа.
2. Определить массу атома и молекулы гелия.
3. Масса 1 л газа (н. у.) равна 1,43г. Чему равна молярная масса этого газа?
Б. Задачи на газовые законы:
4. Давление воздуха в автомобильной шине 0,3 МПа при 15оС. Как изменится давление, если шина нагреется до 50оС?
5. Под каким давлением в сосуд вместимостью 5•10-3 м3 можно при температуре 27оС собрать СО2 массой 0,022 кг?
В. Задачи на вывод химических формул:
6. Вывести простейшую формулу фторида алюминия – калия, если в нем содержится 27,46%К, 19,02%Аl, 53,52F.
7. Из 0,462г пирита получено 1,77г сульфата бария. Определите содержание серы в пирите и его формулу.
Г. Расчеты по химическим формулами уравнениям с использованием понятий: моль, переход от количества вещества к массе и обратно, объемная и мольная доли, выход продукта реакции от теоретически возможного:
8. Вычислить процентное содержание фторапатита Са3(РО4)2•Са2F2 и примесей в хибинской руде, если в ней 30% оксида фосфора (V)
9. При пропускании сернистого газа через раствор едкого калия образовалось по 0,1 молю средней и кислой соли. Какой объем газа был пропущен через раствор?
10. Вычислите массовую долю углерода в карбонате натрия и гидрокарбонате натрия. 11) Сколько г серы прореагирует с газом, выделившимся при взаимодействии 6.5 г цинка с избытком разбавленной серной кислоты, если используется только 80% газа?
11. Какой объем SO2 выделится при сжигании серы в 5 л кислорода при выходе 80%?
Д. Растворы:
12. Чему равна молярность 10%-ой серной кислоты (ρ = 1.11 г/мл)?
13. Чему равна нормальность 10%-го раствора сульфата алюминия (ρ = 1.12 г/л)?
14. Смешали 200 г 20%-ного и 300 г 10%-ного растворов глюкозы. Чему равна массовая доля вещества в полученном растворе.
15. Какова молярность серной кислоты, если к 100 мл воды добавили 20 мл Н2SО4 (ρ = 1,835 г/мл)?
16. Какой рН имеет раствор, в 500 мл которого растворено 1,825 г HCl.
17. К 30 мл воды прибавили 5 мл 3М раствора КNO2. Вычислить рН раствора.
18. Определить концентрацию раствора уксусной кислоты, если α = 2%. Ка=1,75 × 10-5.
19. Сколько мл 96%-ой H2SO4 (ρ = 1,835 г/мл) нужно взять, чтобы приготовить 1 л 0,5М раствора кислоты?
20. В 500 мл раствора содержится 2,52 г Na2СО3. Определить рН раствора.
Задания.
1. Составьте уравнения реакций в молекулярном и ионном виде:
а) Р2О5+ Са(ОН)2 → з) FeCI3 + NaOH→
б) ZnO + H3PO4 → н) СаО + СО2 →
в) Sn(OH)2 + NaOH → к) SО3 + Са(ОН)2 →
г) Sn(OH)2 + НС1 → л) Pb(NO3)2 + KCI →
д) NaHCO3 + HC1 → м) SO2 + Н2О →
е) NaHCO3 + NaOH → н) MnO + Н2О→
ж) Са(НСО3)2+ NaOH → о) Mg(OH)2 + СО2 →
2. Составьте уравнения реакций гидролиза солей с указанием среды: Са (СN)2 RbNO3 CuCl2 Ca(ClO)2 Cs2SO4 Na2HPO4.
3. Уравнять методом электронного или электронно-ионного баланса:
NaOH +S Na2S+Na2SO3
BaCrO4 =BaO +Cr2O3 +O2
Na2SO3 + KMnO4 +KOH = Na2SO4 + K2MnO4 +H2O
4. Напишите уравнения реакций, назовите вещества в схемах превращений
1) Сu → CuO → Cu(NO3) → Cu(OH)2→CuSO4→ (CuOH)2SO4
2) S → SO2 → SO3 → H2SO4 → NaHSO4 → Na2SO4
3) Fe→ FeCl3 → Fe(OH)2 → Fe2O3 → Fe → Fe(OH)2→ Fe(OH)3
4) Zn → ZnCl2→ ( Zn(NH3)4) Cl2 → ZnCO3 → Zn (OH)2→Na2[Zn(ОH)4)]
5. Как сместится равновесие в системе а) при повышении давления, б) при понижении температуры:
N2 + 3Н2 → 2NH3 ΔН = -92кДж.
6. Как изменится скорость прямой реакции в системе: 2 SO2 + О2 → 2SO3,
ΔН = -192 кДж, если при T = const увеличить давление в три раза?
Сколько кДж тепла выделится при сгорании 0.1 кг метана?
7. Вычислить ΔН (кДж) реакции:
CH3OH + CH3COOH → CH3COOCH3 + H2O, если энтальпии сгорания спирта, кислоты и эфира соответственно равны:- 1366,91, - 873,79, и – 2254.21 кДж/моль.
РАЗДЕЛ 6. Изменения в рабочей программе, которые произошли после
утверждения программы.
Характер изменений в программе | Номер и дата протокола заседания кафедры, на котором было принято данное решение | Подпись заведующего кафедрой, утверждающего внесенное изменение | Подпись декана факультета (проректора по учебной работе), утверждающего данное изменение |
РАЗДЕЛ 7. Учебные занятия по дисциплине ведут:
Ф. И.О., ученое звание и степень преподавателя | Учебный год | Факультет | Специальность |
, к. п.н. доцент кафедры биологии и химии ЕГФ | 2009/2010 | ЕГФ | 050103.00 География с доп. специальностью Биология |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 |




