9. Как вычислить степень диссоциации бинарного электролита, если известны константа диссоциации и молярная концентрация раствора?
10. Концентрация каких ионов в растворах солей KHSO3 и КН2РО4 больше и каких меньше?
11. Какой из растворов при одинаковой молярной концентрации содержит больше ионов СН3СОО-: СН3СООН или CH3COONa?
12. Какие гидроксиды называются амфотерными?
13. Составьте ионно-молекулярные уравнения следующих реакций:
a) AI2(SO4)3 + Pb(NO3)2 → г) HCN + NaOH →
6) ZnS + HCl → д) Сu (ОН)2 +Na2S→
в) Fe(OH)3+ HNO3 → e) Cu(OH)2 + H2S →
14. Составьте молекулярные уравнения к следующим ионно-молекулярным уравнениям:
а) Рb2+ + 2I-→ г) HCN + ОН-→
б) Са2+ + СО3 2-→ д) Сu2+ + 2ОН-→
в) NH4OH + Н+ → е) CN - + Н+ →
Модуль «Неорганическая химия»
ЛАБОРАТОРНАЯ РАБОТА № 4(2 ч.)
Тема: Водород, кислород и их соединения.
Цель работы - изучить способы получения и химические свойства водорода кислорода и их соединений.
Получение водорода. Получение кислорода. Восстановительные свойства водорода. Образование аквакомплексов. Окислительно-восстановительные свойства пероксида водорода.Контрольные вопросы
Приведите все способы получения кислорода и водорода в лаборатории. Как изменяются свойства бинарных соединений водорода и кислорода в периоде (на примере III периода) и как эту закономерность можно объяснить? На основании опыта № 2 определите составы растворов после окончания всех реакций, считая, что весь полученный кислород полностью прореагировал, а плотности растворов равны 1 г/моль. Объясните, почему лед легче воды? Вычислите значение ΔG˚298 реакций разложения, какое из указанных веществ предпочтительнее использовать для получения кислорода?2 КСlO3 → 2 КСl + 3 О2 (ΔН = 2 ΔН˚KCl - 2 ΔН˚KClO3)
Na2SO4 → 2 Na2SO3 + O2 (ΔН = 2 ΔН˚Na2SO3 - 2 ΔН˚Na2SO4)
Термодинамические параметры для веществ:
ВЕЩЕСТВО | ΔН˚f | S˚298 |
KClO3 | - 391.20 | 142.97 |
KCl | - 435.85 | 82.68 |
Na2SO4 | - 1384.00 | 149.40 |
Na2SO3 | - 1090.00 | 146.00 |
O2 | --- | 205.03 |
ЛАБОРАТОРНАЯ РАБОТА № 5(2 ч.)
Тема: Углерод и его соединения.
Цель работы - изучить химические свойства углерода и его соединений.
1. а) Свойства активированного угля.
б) Свойства диоксида углерода.
2. Растворимость карбонатов.
3. Гидролиз карбонатов.
4. Термическая устойчивость карбонатов.
5. Растворимость карбонатов.
6. Гидролиз силикатов.
7. Сравнение силы угольной и кремниевой кислот.
Контрольные вопросы
1. Объясните сущность гидролиза силиката натрия. Составьте уравнение реакциигидролиза силиката натрия в молекулярной и ионных формах.
2. Сравнить гидролиз силикатов с гидролизом карбонатов, если обнаружится сходство, объяснить его.
3. Почему карбонаты и силикаты легко гидролизуются?
4. Какой объем оксида углерода (IV) израсходуется на реакцию с 20 мл 10% раствора едкого натра при условии образования кислой соли.
5. Какая соль и в каком количестве образуется при пропускании 5,6 л СО2 через 200 г 5% раствора едкого натра?
ЛАБОРАТОРНАЯ РАБОТА № 6 (4 ч.)
Тема: МЕТАЛЛЫ
Цель работы - изучить химические свойства металлов и их соединений.
Опыт 1. Амфотерные свойства алюминия.
Опыт 2. Амфотерные свойства гидроксида алюминия.
Опыт 3. Отношение меди к кислотам.
Опыт 4. Восстановление оксида меди (II) углем.
Опыт 5. Гидролиз солей меди.
Опыт 6. Отношение цинка к кислотам и щелочам.
Опыт 7. Получение гидроксида цинка и изучение его свойств.
Опыт 8. Гидролиз солей цинка.
Контрольные вопросы
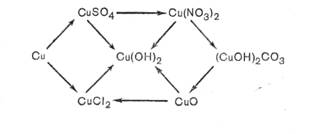
Как экспериментально доказать, что оксид меди (II) —основной оксид? Предложите способ получения из оксида меди (II) гидроксида меди (II). Сделайте вывод об отношении меди к концентрированным и разбавленным кислотам в связи с ее положением в электрохимическом ряду напряжений. Как осуществить следующие превращения: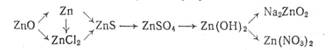
1.7.3 Перечень примерных контрольных вопросов и заданий
для самостоятельной работы.
Модуль1-2 «Общая и неорганическая химия»
Задание 1.
1. Атомы каких из приведенных элементов являются изобарами:
40 42 40 40 112 112 136 138
а. 20 Ca и 20Ca; b. 18 Ar и 19K; c. 48Cd и 50Sn; d. 54Xe и 56Ba?
2. Укажите математическое выражение принципа неопределенности :
а. l = ![]() b. DE = hn; c.
b. DE = hn; c.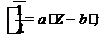 d. D x D v ³
d. D x D v ³ ![]()
3. Какие частицы являются изоэлектронными :
a. Ca2+ ; b. Si4+; c. Ar ; d. Cl - ?
4. Какой подуровень в атомах - 3d или 3p и 6s или 5d - заполняется раньше:
a. 3d и 6; b. 3p и 6s; c. 3d и 5d; d. 3p и 5d?
5. Какова конфигурация валентных электронов в атоме технеция:
a. ...5s2 p5; b. ...4d6 5s1; c. ...4d5 5s2; d....4d25s2 p3?
6. Сколько свободных 3d-орбиталей в атоме хрома:
7. Какие из электронных конфигураций соответствуют возбужденным состояниям:
a. ...2s2; b. ...3s2 3d1; c. ... 4s2 3d2; d. ... 1s2 2s2 p6 3p1?
8. Сколько электронов находится на 4d - подуровне атома гафния
9. Атомы каких элементов - актиноидов имеют наибольшее число неспаренных f-электронов:
a. Pu; b. Am; c. Cm; d. Bk?
10. Какой из переходов электрона в атоме водорода требует поглощения фотона с минимальной энергией:
a. 1s → 2p; b. 1s → 4d; c. 2s → 4s; d. 2p →3s?
2. Какое уравнение характеризует корпускулярно-волновую природу электрона:
a. DE = h n; b. HY = E Y; c. l = h /mv; d. E = -13.6/ n2?
3. Укажите, какие из указанных частиц являются изоэлектронными:
a. Al3+; b. P3-; c. S; d. Cl-?
4. Какие значения всех квантовых чисел (n, ml, m, ms) возможны для валентного электрона атома калия:
a. 4, 1, -1 , - 1/2; b. 4, 1 , +1 , +1/2; c. 4, 0, 0, + 1/2; d. 5, 0, +1, +1/2?
5. Вычислите энергию (Дж), необходимую для перехода электрона атома водорода из состояния, характеризующегося n= 1, в состояние с n3 :
a. 1.5; b. 0.2.10-18; c. 1.9.10 -18; d. 12 .
Задание 2.
а) Определить степени окисления хрома, фосфора, марганца, иода в следующих солях кальция: CrO4 , CaCr2 O7 , Ca 2P2 O7 , Ca (MnO4)2 , Ca MnO3 , CaMnO4 , CaH3 JO6.
CrO4 , CaCr2 O7 , Ca 2P2 O7 , Ca (MnO4)2 , Ca MnO3 , CaMnO4 , CaH3 JO6.
б) Определить степени окисления мышьяка в следующих соединениях:
Ca3 As2, KAs(OH)6 ,KH2 AsO3 ,KAsO2, Mg3 (AsO4)2 , AsCl3 , AsH3 ,HAsCl4, AsOCl .
в) Определить степени окисления серы в следующих соединениях:
SF6 , SO2 Cl2 , K2 S2 O7 , KHSO4 , H2 S, KHS, K2 S2 O3 , SOCl2 .
г) поставить цифровые индексы вместо “х”:
ангидрон MgCl2 Ox ортоклаз KAlSi xO8
антихлор Na2 H10 Sx O4 боракс Na2 BO5(OH)4
свинцовые пандермит Ca2 BxO6(OH)7
белила Pbx CO5 H2 криолит Na3AlFx
берилл Be3 Al2 Ox Si6 натролит Na2 AlxSi3O10
гремучая ртуть Hg(Cx Nx O)2 нефелин KNa3Al4SixO16
кордиерит Mg2 Al4 Si5 Ox улексит BaCaBxO6(OH)6
Задание 3.
Расставить коэффициенты в следующих уравнениях реакций:
1. Cr(OH)3 + H2 SO4 → Cr2(SO4)3 + H2O
2. MnCO3 + HNO3 → Mn(NO3)2 + H2O + CO2
3. Al2 (SO4)3 + Ba Cl2 → AlCl3 + BaSO4
4. NaNO3 + H2 SO4 → HNO3 + Na2SO4
5. KMgCl3 .6 H2 O + H2 SO4 → K2SO4 + MgSO4 + HCl + H2O
6. FeO(OH) + HCl → FeCl3 + H2 O
7. Cu2 (OH )3 Cl + H2 SO4 → CuSO4 + HCl + H2 O
8. NaCaB5 O6 (OH)6 + HCl → NaCl + CaCl2 + H3 BO3 + H2O
9. Co3 (AsO4)2 + H2 SO4 → CoSO4 + H3AsO4
10. Cu3 (OH)2(CO3) + H Cl → CuCl2 + CO2 + H2O
11. (NH4)2 SO4 + KOH → K2 SO4 + NH3 + H2 O
12. AlCl3 + (NH4)2S + H2 O → Al(OH)3 + NH4Cl + H2 O
13. (NH4)SnS3 + HCl → NH4 Cl + SnS2 + H2O
14. Na2 Sn(OH)4 + HCl → NaCl + H2SnCl4 + H2O
15. Na2 O • CaO • 6SiO2 + HF → NaF + CaF2 + SiF4 + H2O
16. Fe3 (PO4)2 + H2 SO4 → FeSO4 + H3PO4
17. KMgSO4Cl + H2SO4 → K2 SO4 + MgSO4 + HCl
18. Mg2 B2 O5 + H2 O + H Cl → MgCl2 + H3BO3
19. CaFe(CO3)2 + HCl → CaCl2 + FeCl2 + CO2 + H2 O
20 KAl3 (OH)6 •(SO4 )2 + H2SO4 → K2 SO4 + Al2(SO4)3 + H2 O
21. CaB(OH) SiO4 + H2 SO4 → CaSO4 + H3BO3 + SiO2

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 |




