10.Какие соединения называются амфотерными? Как доказать их амфотерность?
11. Напишите уравнения реакций, с помощью которых можно осуществить следующие
превращения:
Na → NaOH → NaCl → NaOH → Na.
12. Почему для получения карбоната цинка реакцией обмена используют не карбонат натрия, а гидрокарбонат?
Расчетные задачи:
13. Серебро, массой 5,4 г, растворили в концентрированной азотной кислоте. К
полученному раствору прилили избыток раствора бромида натрия. Рассчитайте
массу образовавшегося осадка.
14. Вычислите объем соляной кислоты (массовая доля HCl 20%, плотность 1,1 г/мл),
которая потребуется для растворения смеси цинка и никеля, массой 9,8 г (массовая
доля никеля в смеси 60,2%).
Задания для самостоятельной работы:
1. Напишите уравнения реакций, протекающих при электролизе водного раствора и расплава бромида калия. Какие вещества можно получить при этом?
2. Допишите схемы тех реакций, которые протекают практически до конца:
а) Li + H2O →
б) NaOH (изб.) + H3PO4 →
в) Na2O + SO2 →
г) NaOH + BaCl2 →
д) LiOH + CuSO4 →
3. С помощью каких реакций можно осуществить следующие превращения:
KCl → KOH → KHS → K2S → KNO3.
Напишите уравнения реакций в молекулярной и ионной формах.
4. Натрий получают электролизом расплава хлорида натрия, а для получения чистого
железа используют электролиз водного раствора сульфата железа (II). Напишите
уравнения реакций, протекающих при этих процессах.
5. При взаимодействии щелочного металла, массой 4,6 г, с йодом образуется иодид,
массой 30 г. Какой щелочной металл был взят для реакции?
6. Сколько технического цинка, содержащего 4% примесей, и сколько 30% соляной кислоты потребуется для приготовления 50 кг 45% раствора хлорида цинка?
7. Сколько цинка и серной кислоты можно получить из 1 т цинковой обманки, содержащей 85% сульфида цинка?
8. Какой должна быть реакция среды в растворе нитрата меди (II)?
9. Как осуществить следующие превращения, напишите уравнения реакций:
А)
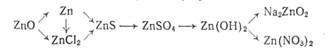
В)
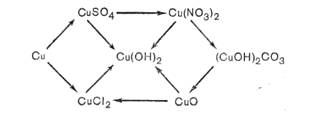
10. Осуществите превращения:
![]()
![]()
Литература
, и др. Лабораторные и семинарские занятия по общей и неорганической химии.- М.: Академия,1999.-360с. Ахметов и неорганическая химия: учебник для химико-технол. Спец. Вузов.- 4-е изд., - М.: Высшая школа, 2001.-743с. Глинка и упражнения по общей химии.- Ленинград: Химия, 1988. Глинка химия.- Л.: Химия, 1973. Мень к контрольным и лабораторным работам по общей и неорганической химии.- М.: МГПУ, 2004.1.7.2 Тематика и планы лабораторных работ по изученному материалу.
Модуль «Общая химия»
Лабораторная работа № 1(2 ч.)
ТЕМА: ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Цель работы — изучить некоторые химические свойства оксидов, гидроксидов, кислот, солей и условия необратимости реакции между растворами двух веществ.
ТБ в химической лаборатории.
Приемы работы с химическим оборудованием и реактивами.
Опыт 1. Взаимодействие основных оксидов с водой.
Опыт 2. Взаимодействие кислотных оксидов с водой.
Опыт 3. Взаимодействие солей с основаниями. Получение нерастворимых в воде гидроксидов металлов и определение их характера.
Опыт 4. Взаимодействие кислот с солями.
Опыт 5. Получение средних и кислых солей.
Опыт 6. Получение гидроксида меди (II) и основной соли меди.
Опыт 7. Взаимодействие солей друг с другом.
Контрольные вопросы
1. Какие вещества называются оксидами? Приведите примеры основных, кислотных и амфотерных оксидов.
2. Как образуются гидроксиды? Какие вещества называются основаниями? кислотами?
3. На примере оксидов и гидроксидов элементов третьего периода объясните изменения их характера при увеличении порядкового номера элемента.
4. Как определяют кислотность основания? Как определяют основность кислоты?
5. Какие вещества называются солями? Назовите различные способы получения солей и составьте соответствующие уравнения.
6. В чем сходство диссоциации оснований? кислот? Докажите, что оно имеется.
7. Как образуются нерастворимые в воде основания? Составьте соответствующие уравнения.
8. Какие гидроксиды называются амфотерными? Как доказать их амфотерность?
9. Назовите условие необратимости реакции между растворами двух солей.
10. Составьте уравнения реакций:
а) Р2О5+ Са(ОН)2 → з) FeCI3 + NaOH→
б) ZnO + H3PO4 → н)СаО + СО2 →
в) Sn(OH)2 + NaOH → к) SО3 + Са(ОН)2 →
г) Sn(OH)2 + НС1 → л) Pb(NO3)2 + KCI →
д) NaHCO3 + HC1 → м) SO2 + Н2О →
е) NaHCO3 + NaOH → н) MnO + Н2О→
ж) Са(НСО3)2+ NaOH → о) Mg(OH)2 + СО2 →
11. При помощи каких реакций можно осуществить следующие переходы от одного вещества к другому?
а) Zn → ZnS → ZnO → (ZnOH)2SO4 → ZnO
б) Cu(OH)2 → CuCl2 → ZnCl2→ ZnOHCl→ ZnSO4
в) CO2 → MgCO3 → Mg(HCO3)2 → MgCO3 → MgO
г) С →CО2 → H2CO3 → BaCO3 → BaCl2
д) MgO → MgCl2→ Mg(OH)2 → MgOHNО3 → Mg(NO3)2
Лабораторная работа № 2 (2ч.)
ТЕМА: ПРИГОТОВЛЕНИЕ РАСТВОРОВ
Цели работы — приготовление растворов кислот и солей различной концентрации.
Опыт 1. Приготовление растворов процентной концентрации.
Задание. Приготовить 200г 5-%- ного раствора карбоната натрия из кристаллической соды Na2CO3 . 10 Н2О и воды.
Вычислить, какое количество Na2СОз . 10 Н2О требуется для приготовления 200г 5-%-ного раствора в расчете на безводную соль Nа2СОз.
Отвесить это количество измельченной соды в предварительно взвешенном стаканчике на технохимических весах с точностью до 0,01г.
Рассчитать, какой объем воды необходим для растворения взятой навески. Отмерить мерным цилиндром этот объем воды.
Вылить воду в стакан и растворить в ней отвешенную соль.
* Вылить раствор в сухой высокий узкий цилиндр и опустить в него ареометр так, чтобы он не касался стенок сосуда. Отметить то деление шкалы, которое совпадает с уровнем жидкости в цилиндре, произведя расчет по шкале сверху вниз. ( Ареометр промыть водой, осторожно вытереть досуха и сдать лаборанту).
Раствор вылить в приготовленную склянку.
Задание. Рассчитать молярность приготовленного раствора, используя найденную плотность.
Опыт 2. Приготовление молярных растворов.
Задание. Приготовить 250мл 1М раствора соляной (серной) кислоты из раствора, имеющегося в лаборатории.
Определить ареометром плотность раствора кислоты.
По найденной плотности, определить процентную концентрацию данного раствора, вычислить навеску, а затем объем этого раствора, необходимый для приготовления заданного раствора.
Налить в мерную колбу 250мл около половины её объема воды и влить в неё ( в случае серной кислоты - тонкой струей, осторожно!) через воронку вычисленный объём раствора кислоты, отмеренный цилиндром. Осторожно перемешать полученный раствор и охладить его до комнатной температуры. Долить колбу водой до метки, закрыть пробкой и хорошо перемешать.
* Вылить полученный раствор в сухой высокий цилиндр, определить ареометром его плотность и затем вылить в приготовленную склянку.
Задание. Вычислить процентную и молярную концентрации, сравнить вычисленную молярность с заданной, установить точность выполнения опыта.
Лабораторная работа №3 (2ч.)
Тема: Свойства растворов сильных и слабых электролитов.
Цели работы — сравнить химическую активность кислот; изучить влияние одноименных ионов на направление диссоциации слабых электролитов; изучить свойства амфотерных электролитов; осуществить ионообменные реакции образования труднорастворимых и малодиссоциирующих веществ.
Опыт 1. Сравнение химической активности кислот.
а) Взаимодействие соляной и уксусной кислот с мрамором.
б) Взаимодействие соляной и уксусной кислоты с цинком.
Опыт 2. Смещение равновесия диссоциации слабого электролита.
а) Влияние соли слабой кислоты на степень диссоциации кислоты.
б) Влияние соли слабого основания на степень диссоциации этого основания.
Опыт 3. Влияние соли слабой кислоты на степень диссоциации сильных кислот.
Опыт 4. Амфотерные электролиты.
Контрольные вопросы
1. Какие вещества называют электролитами? Чем отличаются их водные растворы от растворов неэлектролитов?
2. Какими условиями определяется возможность электролитической диссоциации вещества? Какая величина характеризует ионизирующую способность растворителя? Покажите механизм распада частиц растворенного вещества на ионы.
3. Какие величины являются количественной характеристикой процесса электролитической диссоциации? Дайте их определения. Какую из них называют постоянной величиной и почему?
4. На какие группы условно разделяются электролиты по степени диссоциации? Приведите примеры представителей этих групп.
5. Как и почему на степень диссоциации слабого электролита влияют введение в его раствор одноименного иона и разбавление раствора?
6. Как способность электролитов к диссоциации зависит от вида химической связи?
7. По какому признаку согласно теории электролитической диссоциации вещества классифицируются на кислоты, основания и соли? Почему гидросоли и гидроксосоли можно назвать промежуточными соединениями?
8. Что называется ступенчатой диссоциацией? Чем определяется число ступеней для многоосновных кислот и многокислотных оснований? Как и почему изменяются значения α и Кд, от первой ступени к последней? Напишите уравнение ступенчатой диссоциации мышьяковой кислоты H3AsО4.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 |




