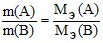ЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ ЭЛЕКТРОЛИТОВ
4.1 Теоретическая часть
Электролиз – совокупность окислительно-восстановительных процессов, протекающих на электродах при пропускании постоянного электрического тока через расплав или раствор электролита. При электролизе происходит превращение электрической энергии в химическую. Устройство для электролиза, называемое электролизером, состоит из двух электродов и электролита. Электрод, соединенный с отрицательным полюсом источника тока, называют катодом, а электрод, подключенный к положительному полюсу – анодом. На аноде протекают реакции окисления, на катоде – восстановления. При этом ионы электролита перемещаются к электроду противоположной полярности, а именно:
катионы – к катоду К (–)
анионы – к аноду А (+)
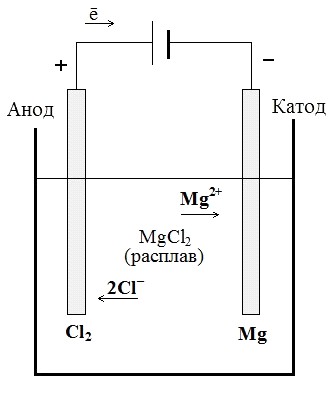
Например, при электролизе расплава хлорида магния MgCl2 на катоде образуется металлический магний, а на аноде молекулярный хлор (см. рисунок 4.1):
Рисунок 4.1 Электролиз расплава хлорида магния | К (–) Mg2+ + 2з = Mg0 A (+) 2Cl– – 2з = Cl20↑ Суммарное уравнение процесса: MgCl2 = Mg0 + Cl20↑ Следовательно, при электролизе расплавов участниками этих процессов являются только ионы электролита (при условии использования инертных электродов). |
При электролизе водных растворов электролитов катодные процессы будут определяться электродным потенциалом катиона, который необходимо сравнить с потенциалом восстановления ионов водорода из воды (-0,41 В) (см. приложение Е):
2H2O + 2з = H2↑ + 2OH– (в нейтральной и щелочной средах)
2H+ + 2з = H2↑ (в кислой среде)
К таким металлам относятся металлы начала ряда напряжений – приблизительно до марганца (см. приложение В).
При значениях потенциала металла, близких к -0,41 В (металлы средней части ряда от марганца до олова), на катоде происходит восстановление как ионов водорода (в зависимости от среды), так и ионов металла:Men+ + nз = Me0
Ионы металлов, потенциал которых значительно выше этого значения (начиная от олова и до конца ряда напряжений), будут восстанавливаться на катоде.Характер анодного процесса при электролизе зависит не только от природы аниона, входящего в состав электролита, но и от материала анода. Платиновый или графитовый электроды являются инертными анодами и не подвергаются окислению. Если же анод изготовлен, например, из железа, никеля, кадмия, меди, то происходит окисление материала анода. Такой электрод называют активным анодом.
Анодные процессы на инертных анодах будут определяться соотношением потенциалов разрядки анионов: прежде всего окисляются бескислородные анионы (I–, Br –, Cl–, S2–, CN–); если же раствор содержит кислородсодержащие анионы (PO43–, SO42–, NO3–), а также ионы F–, то на аноде будет выделяться кислород (см. приложение Е):
2H2O – 4з = O2 + 4H+ (в кислой и нейтральной средах)
4OH– – 4з = O2 + 2H2O (в щелочной среде)
В случае активного анода окисляется и сам анод. Например, процессы электролиза водного раствора сульфата меди с угольным (а) и медным (б) анодами включают следующие электродные процессы:
а) K(–): Cu2+ + 2з = Cu0 A(+): 2H2O – 4з = O2 + 4H+ | б) K(–): Cu2+ + 2з = Cu0 A(+): Cu0 – 2з = Cu2+ |
В последнем случае происходит перенос массы металла с одного электрода (анода) на другой (катод). При этом масса анода уменьшается («анод растворяется»), а масса катода в процессе электролиза увеличивается. Поэтому электролиз с активным анодом часто называют электролизом с растворимым анодом.
Рассмотрим электролиз сульфата натрия с графитовыми электродами:
Na2SO4 ⇄ 2Na+ + SO42–
H2O ⇄ H+ + OH–
K(–): Na+; H+(H2O) A(+): SO42–; OH–(H2O)
Стандартный электродный потенциал системы Na+ + з = Na0 (E°= -2,71 В) значительно отрицательнее потенциала водородного электрода в нейтральной среде (-0,41 В), поэтому на катоде будет происходить электрохимическое восстановление воды по уравнению (см. приложение Е):
2H2O + 2з = H2 + 2OH–
Ионы Na+ будут накапливаться в катодном пространстве.
На аноде будет происходить электрохимическое окисление воды по уравнению:
2H2O – 4з = O2 + 4H+
Сульфат-ионы будут накапливаться в анодном пространстве.
Суммарное уравнение процесса:
эл.-з
2H2O = 2H2 + O2
Побочными продуктами электролиза являются гидроксид натрия (NaOH) и серная кислота (H2SO4).
Электролиз бромида хрома с графитовыми электродами:
CrBr3 ⇄ Cr3+ + 3Br –
H2O ⇄ H+ + OH–
K(–): Cr3+; H+ (H2O) A(+): Br –; OH– (H2O)
Стандартный электродный потенциал системы Cr3+ + 3з = Cr0 (E° = -0,71В), поэтому на катоде будет происходить совместное восстановление хрома и восстановление воды с образованием водорода (см. приложение Е):
Cr3+ + 3з = Cr0
2H2O + 2з = H20 + 2OH–
На аноде разрядка бромид-ионов энергетически предпочтительнее окисления молекул воды, поэтому будет выделяться молекулярный бром:
2Br – – 2з = Br20
Электролиз раствора гидроксида натрия с графитовыми электродами
Процессы, происходящие при электролизе раствора гидроксида натрия, представим в виде схемы:
NaOH ⇄ Na+ + OH-
H2O ⇄ H+ + OH–
K(–): Na+; H+ (H2O) A(+): OH– (H2O)
2Н2О + 2з → Н2 + 2ОН– 2ОН–-2з →ЅО2 + Н2О
Суммарное уравнение электролиза:
2Н2О + 2з → Н2 + 2ОН–
2ОН– -2з →ЅО2 + Н2О
Н2О = Н2 + ЅО2
Процесс электролиза количественно описывается законами Фарадея.
1 закон Фарадея: массы (для твердых и жидких) или объемы (для газообразных) веществ, выделившихся на электродах при электролизе, прямо пропорциональны количеству электричества, прошедшего через электролит:
| (4.1) |
| (4.2) |
где m – масса вещества, образующегося на электроде, г;
Q – количество электричества, Кл;
F – постоянная Фарадея, 96500Кл = 26,8А∙час;
I – сила тока, А;
ф – продолжительность электролиза, с;
Mэ – молярная масса эквивалента, г/моль;
V – объем газа, образующегося на электроде, л;
Vm – молярный объем, л/моль (молярный объем при нормальных условиях равен 22,4 л).
2 закон Фарадея (закон эквивалентов для электрохимических реакций): массы прореагировавших на электродах веществ, при постоянном количестве электричества, относятся друг к другу как их молярные массы эквивалентов:
| (4.3) |
где m(A) – масса вещества А, г;
m(B) – масса вещества B, г;
Mэ(А) – молярная масса эквивалента вещества А, г/моль;
Mэ(B) – молярная масса эквивалента вещества B, г/моль.
Количество электричества, которое затрачивается на выделение нужных продуктов, характеризуется величиной, называемой выходом по току (з):
| (4.4) |
Выход по току – это отношение массы практически выделившегося вещества (mПР) к массе рассчитанной по закону Фарадея (mТЕОР).
Электрохимические процессы широко применяются в различных областях современной техники, в аналитической химии, биохимии и т. д. В химической промышленности электролизом получают хлор и фтор, щелочи, хлораты и перхлораты, надсерную кислоту и персульфаты, химически чистые водород и кислород и т. д.
Электролиз в гидрометаллургии является одной из стадий переработки металлсодержащего сырья, обеспечивающей получение товарных металлов. Электролиз может осуществляться с растворимыми анодами – процесс электрорафинирования или с нерастворимыми анодами – процесс электроэкстракции.
В цветной металлургии электролиз используется для извлечения металлов из руд и их очистки. Электролизом расплавленных сред получают натрий, алюминий, магний, титан, цирконий, уран, бериллий и др. (см. рисунок 4.2, 4.3).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |