ОПЫТ 1. Восстановление перманганата калия в различных средах
Перманганат калия (KMnO4) – один из самых распространенных окислителей. Он превращается в различные вещества в зависимости от рН раствора (см. приложение Б).
В 3 пробирки внести по 1-2 мл раствора перманганата калия KMnO4.
Затем в первую добавить 1 мл раствора серной кислоты H2SO4, во вторую – 1 мл воды, в третью – 1 мл раствора гидроксида натрия NaOH. В каждую пробирку внести сухую соль сульфита натрия Na2SO3 до изменения цвета раствора.
Отметить в лабораторном журнале наблюдаемые изменения.
Составить уравнения реакций между KMnO4 и Na2SO3 в кислой, нейтральной и щелочной средах по методу электронно-ионного баланса. Сделать заключение об окислительно-восстановительной способности перманганата калия в различных средах.
ОПЫТ 2. Окислительные свойства дихромата калия
В пробирку внести 2-3 мл раствора K2Cr2O7 и 1-2 мл раствора H2SO4. Затем добавить небольшое количество раствора KI.
Отметить изменение окраски полученного раствора. Чем оно обусловлено?
Записать и составить уравнение окислительно-восстановительной реакции, при помощи метода электронно-ионного баланса, используя схему (см. приложение Б):
Cr2O72– + H+ → 2Cr3+ + H2O
ОПЫТ 3. Окислительно-восстановительная двойственность соединений элементов, находящихся в промежуточной степени окисления на примере нитрита натрия
Чтобы убедиться в окислительно-восстановительной двойственности нитрита натрия, для этого в одну пробирку поместить 1-2 мл раствора перманганата калия, подкислить раствором серной кислоты и добавить раствор нитрита натрия до обесцвечивания раствора.
В другую пробирку внести 1-2 мл раствора иодида калия KI, подкислить раствором H2SO4 и добавить раствор NaNO2 до изменения окраски.
Как объяснить наблюдаемые явления?
Написать соответствующие уравнения реакций, принимая во внимание, что при восстановлении нитрит-ионов выделяется азот, а при их окислении образуются нитрат-ионы. Расставить коэффициенты, используя метод электронно-ионного баланса, указав протекающие процессы.
В каком случае нитрит-ионы проявляют восстановительные свойства, а в каком – окислительные?
1.3 КЕЙС-Задания
При изготовлении печатных плат производят избирательное травление (окисление) пленки меди, нанесенной на полимер. Определите, можно ли использовать в качестве окислителя трихлорид железа, т. е. пойдет ли реакция: Cu + Fe3+ → Cu+ + Fe2+ при активностях ионов Fe3+ и Cu+, равных 1 моль/л и 298 К. Предложите другой окислитель для растворения меди (приложение Г). Известно получение некоторых металлов путем восстановления с помощью CO или H2. Подтвердите расчетом возможность реакции восстановления меди: CuO(т) + H2(г) ⇄ Cu(т) + H2O(г) при стандартных состояниях веществ и 298 К (приложение Д). Рассчитайте массу восстановления меди, если объем затраченного водорода составляет 22,4 л (измерен при нормальных условиях). Окислительно-восстановительная способность систем зависит от активности окисленной и восстановленной форм вещества, а также от рН раствора. Можно ли окислить ион Fe2+ до иона Fe3+ перманганат-ионом MnO4–, который при восстановлении в кислом растворе превращается в ион Mn2+ (состояния веществ – стандартные)? Составьте уравнение окислительно-восстановительной реакции и рассчитайте константу равновесия реакции при 298 К (приложение Г). При помощи ОВР получают металлические покрытия на поверхностях изделий химическим способом (химическое никелирование, серебрение, меднение). Химическое меднение можно провести восстановлением соли меди, например CuCl2 гидразином (N2H4), который окисляется до воды и азота. Напишите уравнение реакции, определите с помощью расчета для стандартных состояний веществ направление реакции при 298К (приложение Д). Укажите пути ускорения реакции. Какие экологические последствия возможны при протекании процесса? Можно ли предложить другой восстановитель для этой цели? Приведите уравнения реакции и рассчитайте стандартную энергию Гиббса этой реакции при 298К.
1.4 КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Какие реакции называют окислительно-восстановительными?
2. Что называется степенью окисления элемента?
3. Определить степень окисления элементов в соединениях: HNO3, K2SO4, FeO, SO2, Na2CrO4, HMnO4, Br2, Ca(OH)2.
4. Какие вещества называются окислителями и восстановителями? Привести примеры типичных окислителей и восстановителей.
5. На каком принципе основаны методы электронного и электронно-ионного баланса составления уравнений окислительно-восстановительных реакций?
6. Каков порядок составления уравнений окислительно-восстановительных реакций?
7. В какой степени окисления (-2, +4 или +6) должна находиться сера в своем соединении, чтобы она могла диспропорционировать?
8. Какие окислительно-восстановительные реакции называются внутримолекулярными?
2 Лабораторная работа
ЭЛЕКТРОХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ. ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ
2.1 Теоретическая часть
Механизм возникновения электродного потенциала
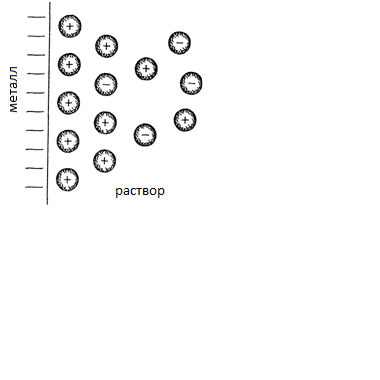
Если погрузить металлическую пластинку в раствор электролита, содержащий ионы этого же металла, то положительные ионы, находящиеся на поверхности металла, гидратируются и некоторое их количество переходит в раствор. В результате этого перехода на пластинке образуется избыток электронов, и она заряжается отрицательно. Катионы, перешедшие в раствор, вследствие притяжения отрицательно заряженным металлом, располагаются вблизи его поверхности. Что приводит к образованию двух слоев с противоположными зарядами – двойного электрического слоя (см. рисунок 2.1).
Рисунок 2.1 Образование двойного электрического слоя | Таким образом, на границе раздела «металл – раствор» устанавливается подвижное равновесие: Ме + mН2О ⇄ Ме n+ ∙ mН2О + n з (в растворе) (на металле) или можно записать, не включая гидратационную воду: Ме ⇄ Ме n + + n з |
От положения приведенного равновесия находится знак и величина заряда поверхности.
Если поверхность металла заряжена положительно, наблюдается картина, обратная представленной на рисунке 2.1. Таким образом,
- при погружении металла в раствор, содержащий ионы этого же металла, на поверхности раздела фаз образуется двойной электрический слой и возникает определенный скачок потенциала, который принято называть электродным потенциалом.
Факторы, от которых зависит
величина электродного потенциала
Как отмечалось выше, знак и величина потенциала зависят от положения равновесия между металлом и раствором. Электродный потенциал зависит от следующих основных факторов:
- От природы металла. Чем большей химической активностью обладает данный металл, т. е. чем легче он растворяется, тем в большей степени равновесие смещено вправо – тем отрицательнее потенциал. От концентрации ионов металла в растворе. Переход ионов металла в раствор происходит тем интенсивнее, чем меньше концентрация катионов в растворе. Наоборот, с увеличением концентрации раствора равновесие смещается влево, и потенциал становится более положительным. От температуры. С повышением температуры потенциал становится более положительным, т. е. равновесие смещается влево. Чтобы понять причины этого эффекта, необходимо учесть, что переход ионов в раствор связан с гидратацией, а гидратация – процесс экзотермический (действие принципа Ле Шателье).
Зависимость величины потенциала от указанных факторов выражается уравнением Нернста:
Е Me n+/ Me = Е°Me n+/ Me + ![]() ln a Me n+ (2.1)
ln a Me n+ (2.1)
Для разбавленных растворов a Me n+ = [Ме n+], тогда:
Е Me n+/ Me = Е°Me n+/ Me + ![]() ln [Ме n+] (2.2)
ln [Ме n+] (2.2)
где a Me n+ – активность ионов металла в растворе, моль/л;
[Ме n+] – концентрация ионов металла, моль/л;
E Me / Me n+ – электродный потенциал металла в растворе, содержащем катионы Ме n+, В;
E° Me / Me n+ – стандартный электродный потенциал, В;
R – универсальная газовая постоянная, равная 8,314 Дж/моль∙К;
Т – температура по шкале Кельвина;
F – постоянная Фарадея, равная 96500 Кл/моль;
n – число электронов, участвующих в электродном процессе для одного атома металла (или заряд иона металла).
Если в уравнение (2.2) подставить численные значения постоянных R и F, принять температуру равной 298 К (25°С) и перейти от натурального логарифма к десятичному (коэффициент перехода равен 2,3), то получим:
Е Me n+/ Me = Е°Me n+/ Me + ![]() lg [Ме n+] (2.3)
lg [Ме n+] (2.3)
Из уравнения (2.3) следует:
стандартный электродный потенциал E° – это потенциал электрода при стандартных условиях: [Ме n+] = 1 моль/л, Т =298 К, Р = 101кПа.
Величина E° характеризует химическую активность металла: чем активнее металл, тем отрицательнее его стандартный потенциал.
Измерение электродных потенциалов
Ряд напряжений металлов

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |