Измерить абсолютную величину электродного потенциала невозможно, а можно измерить только разность потенциалов между двумя электродами. Для определения электродного потенциала нужно составить гальванический элемент из исследуемого и стандартного водородного электродов и измерить его напряжение. Поскольку стандартный водородный электрод является эталоном, потенциал которого условно равен нулю:
E°2H+/ H2 = 0 В
то, измеренное напряжение будет представлять собою потенциал данного электродного процесса.
Тогда потенциал водородного электрода:
E2H+/ H2 = 0,059 1g а H+ = -0,059 рН (2.4)
- Стандартный потенциал водородного электрода - это потенциал при температуре 298 К, давлении водорода 1,01·105Па и активности ионов водорода в растворе 1 моль/л. По отношению к стандартному водородному электроду выражают потенциалы всех других электродов.
Если измерить стандартные электродные потенциалы различных металлов по отношению к потенциалу стандартного водородного электрода и расположить их в порядке увеличения, получим электрохимический ряд стандартных электродных потенциалов (ряд напряжений) металлов (см. приложение В):
Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H, Sb, Bi, Cu, Hg, Ag, Pt, Au
В этом ряду слева направо происходит уменьшение химической активности металлов. Положение металлов в ряду напряжений позволяет предсказать возможность самопроизвольного протекания реакции.
- Самопроизвольно могут протекать те реакции, в которых восстановитель имеет более электроотрицательный потенциал, чем окислитель.
Чем меньше стандартный электродный потенциал металла, тем более сильным восстановителем он является, и тем слабее выражены окислительные свойства его ионов. И наоборот.
Таким образом, в ряду напряжений:
- все металлы, имеющие отрицательный стандартный электродный потенциал (т. е. стоящие в ряду напряжений до водорода), могут вытеснять (восстанавливать) водород из растворов кислот; металлы, имеющие низкий стандартный электродный потенциал (от начала ряда по магний включительно), вытесняют водород из воды; каждый металл может вытеснять (восстанавливать) из растворов солей те металлы, которые имеют больший стандартный электродный потенциал (стоят в ряду напряжений после него).
Кроме того, ряд напряжений используют:
- для выбора материала электродов при разработке гальванических элементов и аккумуляторов; для выбора материала металлопокрытия (катодного или анодного), наносимого на металл, с целью защиты от коррозии; при конструировании машин, механизмов, металлоконструкций для исключения контакта металлов с большой разницей электродных потенциалов; для определения последовательности разряда ионов металлов при электролизе.
Типы электродов
В зависимости от свойств веществ, участвующих в электродных процессах, все электроды можно разделить на несколько типов.
Электроды первого рода. К этому типу электродов относятся все металлические электроды и водородный электрод. Условные обозначения таких электродов:
Металлические электроды: Ме / Ме n+, например, Cu / Сu2+
Водородный электрод: (Рt) Н2 / Н+
Вертикальная черта символизирует поверхность раздела фаз. Общим для этих электродов является то, что в равновесии на электроде участвуют нейтральные атомы (или молекулы) и один вид катионов. Такие электроды
являются обратимыми относительно катионов.
Электроды второго рода. Такие электроды состоят из трех фаз:
- металл покрыт слоем труднорастворимой соли этого металла, а в растворе, куда он опущен, находятся те же анионы, которые входят в состав труднорастворимой соли.
Например:
Хлорсеребряный электрод: Аg, АgСl / КС1
Каломельный электрод: Нg, Нg2С12 / КС1
В отличие от электродов первого рода в равновесиях участвуют анионы, т. е. электроды второго рода обратимы относительно анионов. Величина потенциала этих электродов зависит от концентрации анионов:
EAg, AgС1, КС1 = Е° Ag, АgС1, КС1 + 0,059 1g СCl - (2.5)
Эти электроды в лабораторной практике обычно используют в качестве электродов сравнения. Водородный электрод довольно сложен в изготовлении и им трудно пользоваться при стандартных условиях. Поэтому практически удобнее измерять потенциалы различных электродов по отношению к хлорсеребряному или каломельному электроду. Их потенциалы по отношению к водородному электроду известны. Так, если применять насыщенные растворы хлорида калия, потенциал хлорсеребряного электрода при 25°С равен 0,22 В, а каломельного 0,24 В.
Окислительно-восстановительные электроды.
- Эти электроды представляют собой пластинку или проволоку из благородного металла (чаще всего платины), погруженную
в раствор, содержащий ионы одного элемента в разной степени окисления. Например: Pt / Fe3+, Fе2+.
Платина в процессах не участвует и играет роль переносчика электронов. Величина потенциала может быть рассчитана по уравнению Нернста:
Е Fe+3/ Fe+2 = Е° Fe+3/ Fe+2 + ![]() lg
lg ![]() (2.6)
(2.6)
где E Fe+3/ Fe+2 – окислительно-восстановительный потенциал, В;
E° Fe+3/ Fe+2 – стандартный окислительно-восстановительный потенциал, В;
n – число электронов, участвующих в электродной реакции (для данной системы n = 1);
Сок и Свосст – концентрация ионов в высшей и низшей степени окисления, моль/л.
Из уравнения (2.6) следует,
- что стандартный окислительно-восстановительный потенциал - это потенциал электрода при Сок = Свосст = 1 моль/л.
Величина стандартного окислительно-восстановительного потенциала характеризует свойства окислителей и восстановителей, а именно:
- чем выше E°, тем более сильным окислителем являются ионы в высшей степени окисления; чем ниже E°, тем более сильным восстановителем являются ионы в низшей степени окисления.
Стандартные окислительно-восстановительные потенциалы некоторых систем приводятся в справочниках (см. приложение Г). Располагая величинами E°, можно предсказать, какие окислительно-восстановительные реакции могут протекать самопроизвольно.
Гальванические элементы
Гальванический элемент – это химический источник электрической энергии, которая вырабатывается за счет протекания окислительно-восстановительного процесса. При этом реакция окисления происходит на отрицательном электроде (аноде), а реакция восстановления – на положительном электроде (катоде). В роли анода выступает металл с более низким значением электродного потенциала (ЕА < ЕК).
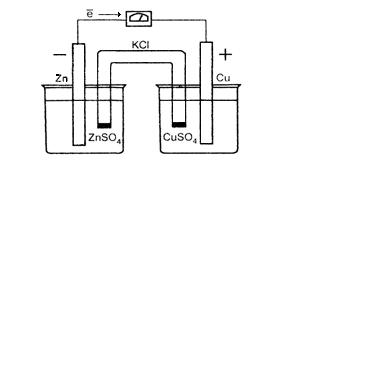
Одним из наиболее простых гальванических элементов является медно-цинковый, или элемент Якоби - Даниеля. В нем проводником (внешняя цепь) соединены пластинки из меди и цинка, при этом каждый металл опущен в раствор соответствующей соли. Растворы CuSO4 и ZnSO4 соединены между собой солевым мостиком – стеклянной трубкой, заполненной раствором КCl (внутренняя цепь). Солевой мостик препятствует смешиванию растворов, проводит электрический ток (см. рисунок 2.2).
Рисунок 2. 2 Схема гальванического элемента Якоби - Даниеля | На электроде из цинка (аноде) происходит окисление атомов цинка в ионы (разрушение металла и получение электронов): Zn0 – 2з = Zn2+. Поскольку электродный потенциал цинка (Е°Zn2+ / Zn = - 0,76 В) меньше, чем меди (Е° Cu2+ / Cu = 0,34 В), электроны по внешней цепи переходят на медную пластину. |
На медном электроде (катоде) происходит восстановление ионов меди в атомы, которые осаждаются на электроде:
Cu2+ + 2з = Cu0.
Одновременно часть ионов SO42- переходит по внутренней цепи из сосуда с CuSO4 в сосуд с ZnSO4.
Гальванический элемент обычно изображают электрохимической схемой, в которой слева направо записывают:
- анод (электрод, имеющий меньший потенциал);
- вертикальная линия (граница металла с раствором соли); ион соли; две вертикальные линии (граница между растворами); ион другой соли; вертикальная линия (граница раствора соли с металлом); катод (электрод, имеющий больший потенциал); в скобках указывают знаки полюсов.
Например, электрохимическая схема медно-цинкового гальванического элемента:
А (–) Zn | ZnSО4 || СuSО4 | Cu (+) К
Подобным образом обозначают любые гальванические элементы. При этом следует помнить, что слева принято указывать электрод с более электроотрицательным потенциалом.
Далее указываются процессы, протекающие на электродах:
А (–) Zn 0 – 2з = Zn 2+ окисление
К (+) Сu 2+ + 2з = Сu 0 восстановление
Суммарное уравнение процесса:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |