3) перемещение ионов в растворе электролита;
4) процесс катодного восстановления окислителей, присутствующих в растворе электролита.
Причинами возникновения гальванопар могут являться, например: контакт двух металлов, находящихся в растворе электролита, примеси в металлах, контакт металла с его оксидом, электрохимическая неоднородность поверхности металла и др.
Окислители снимают избыточный отрицательный заряд с поверхности катода, уменьшая его поляризацию, поэтому их называют в этом процессе деполяризаторами.
Наиболее распространенные в природе окислители – ионы водорода и растворенный в воде кислород, поэтому различают:
- водородную деполяризацию (происходит в кислых средах)
2Н+ +2з = Н2
- кислородную деполяризацию (влажный воздух, морская вода, почвенные воды нейтрального характера и т. п.)
О2 + 2Н2О + 4з = 4ОН-
Таким образом, в кислых средах продуктами коррозии являются соль металла-анода и газообразный водород, а в нейтральной среде – гидроксид металла-анода Ме(ОН)n или его оксогидроксид МеО(ОН)n-2.
Металлы, применяемые в технике, всегда содержат примеси других металлов, поэтому металл-основа и металл-примесь образуют множество микрогальванических элементов.
Сталь состоит в основном из мельчайших кристалликов железа (феррит), смешанных с зернами карбида железа (цементит – Fe3C) и углерода. В агрессивной среде возникает гальванический элемент, в котором отрицательным электродом (анодом) является феррит, а положительным электродом (катодом) является цементит и углерод.
По окислительной способности растворенный в воде кислород значительно активнее ионов водорода, поэтому вода, содержащая кислород более опасна в коррозийном отношении.
Схема образовавшегося гальванического элемента:
А (–) Fe | H2O, O2 | Fe3C (+) K
На аноде протекает процесс окисления железа (металл разрушается, ионы его переходят в раствор):
Fe0 – 2з = Fe2+
На катоде происходит кислородная деполяризация (восстанавливается агрессивная среда):
О2 + 2Н2О + 4з = 4ОН-
Процессы, протекающие в растворе:
Fe2+ + 2OH - = Fe(OH)2
Последующее окисление до гидроксида железа (III):
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
Продуктами коррозии железа является сложная смесь гидратированных и дегидратированных форм гидроксидов железа (например, FeO(OH)), в упрощенном виде выражается общей формулой: Fe2O3 · nH2O (ржавчина – бурый рыхлый порошок, который не защищает поверхность железа от дальнейшего разрушения).
Электрохимической коррозии подвержены стальная и алюминиевая арматура железобетона при образовании в теле бетона микротрещин, по которым в толщу бетона проникают морские, речные или сточные воды. В этом случае скорость электрохимической коррозии зависит от рН среды, влажности грунта, количества растворенного кислорода и других факторов.
Таким образом, при электрохимической коррозии поток электронов направляется от более активного металла к менее активному и более активный металл корродирует. Скорость коррозии будет тем больше, чем дальше стоят друг от друга металлы в ряду напряжений (см. приложениие В), т. е. чем больше величина ЭДС гальванического элемента.
МЕТОДЫ ЗАЩИТЫ МЕТАЛЛОВ ОТ КОРРОЗИИ
Потери железа вследствие ржавления достигают 20% от его ежегодного производства. Поэтому в технике широко используют различные меры защиты металлов, позволяющие свести коррозию к минимуму. Выбор метода защиты зависит от эффективности и экономической целесообразности.
Для защиты металлов от коррозии применяют следующие методы:
1. Легирование – введение добавок, повышающих коррозийную стойкость металлов. Например, при введении в состав стали до 12% хрома получают нержавеющую сталь, устойчивую к коррозии. Добавление цветных металлов – кобальта, никеля, меди усиливает антикоррозийные свойства стали, поскольку повышается склонность сплава к пассивации.
2. Обработка коррозийной среды – уменьшение содержания деполяризатора, нейтрализация кислых сред, удаление из воды кислорода (деаэрация), ее проводят на станциях водоочистки. Для этого воду пропускают через слой железной стружки, которая поглощает кислород из воды. В теплотехнике проводят обессоливание воды, так как соли – активаторы коррозии – значительно ускоряют коррозийный процесс. Для замедления коррозии металла в электролит вводят вещества, которые называются ингибиторами. К неорганическим ингибиторам относятся хроматы цинка и свинца, из органических ингибиторов используется уротропин, адипиновая кислота, бензонат натрия и др. Ингибиторы широко используются при химической очистке от накипи паровых котлов, а так же при хранении и перевозке кислот в стальной таре. Сравнительно недавно разработаны летучие (атмосферные) ингибиторы. Их применяют для пропитки бумаги, которой обертывают металлические изделия. Пары ингибитора адсорбируются на поверхности металла и образуют на ней защитную пленку.
3. Изоляция металлов от окружающей среды – различного рода покрытия. Покрытия бывают неметаллические, металлические, химические.
В качестве неметаллических покрытий используют самые разнообразные материалы: лаки, краски, эмали, битум, резину, синтетические смолы, полимерные материалы и т. п. Необходимым условием эффективности этого метода является чистота поверхности металла и отсутствие на ней влаги перед обработкой.
Химические покрытия получают путем химической или электрохимической обработки поверхности металла.
Например, оксидирование – обработка поверхности металла раствором кислот, щелочей, различных окислителей и восстановителей. Металл после такой обработки становится «пассивным», т. е. не подвергается коррозии и даже не растворяется в кислотах. Вещества, способствующие возникновению на поверхности металла защитной пленки обычно называют пассивирующими агентами (конц. HNO3, K2Cr2O7, NaNO2 и др.).
Фосфатирование – химическая обработка металлической поверхности, приводящая к образованию труднорастворимых фосфатов, которые характеризуются высокой степенью сцепления (адгезии) с основным металлом и хорошо защищает его от коррозии.
Из металлических покрытий широко распространены хромирование, никелирование, лужение, цинкование, серебрение, золочение. Металлические покрытия подразделяются на анодные и катодные.
Анодные покрытия изготавливают из металлов, имеющих меньшие значения электродных потенциалов, чем защищаемый металл.
Например, в случае оцинкованного железа (рисунок 3.1) поверхность железа (3) покрыта слоем цинка (2). До тех пор, пока целостность покрытия не нарушена, поверхность цинка изолирует основной металл (железо) от окружающей среды. Однако как только на цинковой поверхности образуется трещина, царапина или другое механическое повреждение, то кислота (1) входит в контакт с металлами, начинает работать микрогальванический элемент, в котором функцию анода выполняет цинк (Е° = - 0,763 В), а функцию катода – железо (Е° = - 0,440 В).
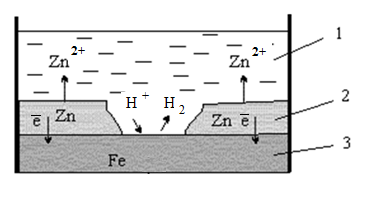
Рисунок 3.1. Схема разрушения оцинкованного железа в кислой среде
Составим схему и работу этого микрогальванического элемента в кислой
среде:
А (–) Zn | HСl | Fe (+) K A(–): Zn – 2з = Zn2+ – окисление K(+): 2Н+ + 2з = Н2 – восстановление Zn + 2Cl - = ZnCl2 |
В этом случае разрушается слой покрытия, а стальная деталь не корродирует.
Подбирая анодные покрытия, необходимо учитывать то обстоятельство, что наиболее эффективно «работают» в роли анодных покрытий те металлы, электродные потенциалы которых максимально отличаются от электродных потенциалов основного металла (другими словами, металл-покрытие и основной металл должны стоять в таблице стандартных электродных потенциалов (см. приложение В) как можно дальше друг от друга).
Разновидностью анодной защиты является протекторная защита (см. рисунок 3.2). В переводе с латинского protector – защитник, покровитель. В этом методе к защищаемой металлической детали (3) припаивают или присоединяют металлическим проводником (2) пластины из более активного металла (1). При этом создается гальванопара, анодом которой является более активный металл, т. е. протектор. В качестве протекторов используют магний, алюминий, магниево-алюминиевые сплавы, цинк (его активность не столь высока, но он имеет низкую стоимость).
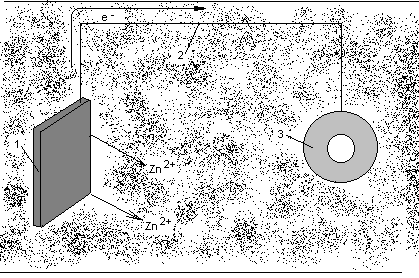
Рисунок 3.2 Схема протекторной защиты.
Металлы, применяемые для изготовления катодных покрытий, имеют больший электродный потенциал, чем защищаемый металл. Например: в случае луженого железа (белая жесть) железо (Е° = - 0,440 В), покрыто оловом (Е° = - 0,136 В).
Защитная роль катодного покрытия существенно отличается от действия анодных покрытий. На первой стадии (до нарушения целостности покрытия) особых различий нет, но как только возникают условия для работы гальванического элемента (оба металла вступают в контакт с агрессивной средой), функцию анода берет на себя основной металл, т. к. его потенциал имеет меньшее значение. В этих условиях коррозийному разрушению подвергается основной металл, а металл покрытия этому разрушению способствует, поляризуясь катодно.
Рассмотрим, как протекает процесс коррозии железа (3), находящегося в контакте с медью (2), во влажном воздухе (3) при нарушении покрытия (см. рисунок 3.3).
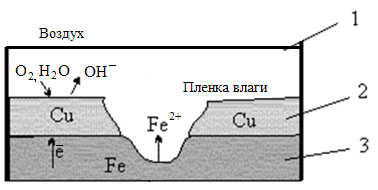
Рисунок 3.3 Схема атмосферной коррозии железа, находящегося в контакте с медью
А (–) Fe | H2O, O2 | Cu (+) K A(–): Fe0 – 2з = Fe2+ K(+): 2Н2О + О20 + 4з = 4ОН- 2Fe + O2 + 2H2O = 2Fe(OH)2 При дальнейшем окислении железа получим: 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 |
Катодное покрытие защищает основной металл от разрушения только при отсутствии повреждений на поверхности покрытия.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



