Для катодных покрытий целесообразно подбирать те металлы, электродные потенциалы которых в наименьшей степени отличаются от электродного потенциала основного металла (т. е. в таблице стандартных электродных потенциалов (см. приложение В) эти металлы должны находиться как можно ближе друг к другу).
4. Электрохимический метод защиты – катодная защита (метод внешнего потенциала). В этом методе (см. рисунок 3.4) защищаемое изделие (1) подключают к отрицательному полюсу внешнего источника постоянного тока (2), поэтому оно становится катодом, а анодом служит металлолом (3).
Например, защищаемая железная конструкция и вспомогательный (стальной) электрод образуют электрохимическую схему в воде:
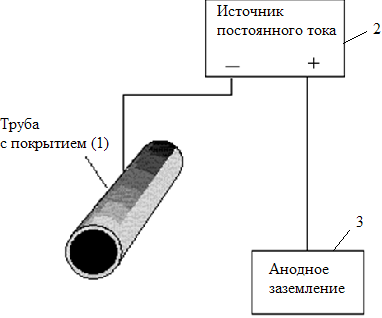
Рисунок 3.4. Схема катодной электрозащиты.
А (–) Fe | H2O | Fe (+) K
A(–): Fe0 – 2з = Fe2+
K(+): 2Н2О + 2з = H20 + 2ОН-
Fe + 2H2O = H2 + Fe(OH)2
При дальнейшем окислении железа:
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
Вспомогательный электрод разрушается и его периодически заменяют новым, а на защищаемой конструкции (катоде) восстанавливается среда (в данном случае – вода), получая электроны не от металла, а от источника тока.
С явлением «коррозия» мы встречаемся постоянно, поскольку изделия из металлов встречаются повсюду: автомобили, самолеты, мосты, станки, водопроводные трубы, железобетонные конструкции, предметы домашнего обихода и др. Борьба с коррозией в настоящее время приобрела особое значение, т. к. в промышленности и в технике применяют высокие температуры и давление, различные агрессивные среды – растворы кислот, солей, щелочей.
Коррозия наносит не только прямой ущерб – разрушение металла, но и косвенный – это связано с выходом из строя различных приборов, машин, металлоконструкций, которые являются более ценными, чем сам металл. Например, при коррозийном разрушении поршней автомобильного двигателя или шасси приводит к тому, что автомобиль теряет свое предназначение. Иногда коррозия приводит к авариям, например, в котельных установках могут происходить взрывы котлов.
Эффективность борьбы с коррозией основана на понимании механизма коррозийных процессов и должна решаться комплексным подходом – применением комбинированных методов защиты с учетом эффективности действия каждого из них в данных конкретных условиях.
3.2 ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Цель работы: смоделировать в лабораторных условиях процессы электрохимической коррозии металлических изделий и методы защиты металлов от коррозийных разрушений.
Оборудование и реактивы: пробирки; штатив для пробирок; наждачная бумага; фильтровальная бумага, пластинки: цинка, алюминия, оцинкованного железа, луженого железа; медный стержень; стальные гвозди; железные стружки; уротропин; 2%-ные растворы: сульфата меди (CuSO4), нитрата ртути (I) (Hg2(NO3)2), нитрата ртути (II) (Hg(NO3)2),гидроксида натрия (NaOH); растворы: серной кислоты (H2SO4), разб.; азотной кислоты (HNO3), конц.; красной кровяной соли (K3[Fe(CN)6]), 1M.
ОПЫТ 1. Коррозия при контакте двух различных металлов
В пробирку поместить цинковую пластинку. Прилить разбавленной серной кислоты. Отметить выделение водорода и объяснить возможность протекания реакции с помощью значения стандартного электродного потенциала (см. приложение В).
Ввести в раствор кислоты медный стержень, не доводя его до соприкосновения с цинковой пластинкой. Наблюдается ли выделение водорода на меди? Прикоснуться медным стержнем цинковой пластинки. На каком металле будет наблюдаться выделение водорода? Записать схему коррозийного медно-цинкового гальванического элемента с водородной деполяризацией на катоде. Как повлиял контакт с медью на коррозию цинка?
ОПЫТ 2. Влияние гальванопары, возникающей в результате химической реакции, на процесс растворения металла
В две пробирки налить по 2 мл разбавленной серной кислоты и внести по одной пластинке цинка. Наблюдать медленное выделение водорода в пробирках. В одну из пробирок добавить 1 мл раствора сульфата меди. Что наблюдается? Почему возросла скорость выделения водорода при добавлении раствора сульфата меди? Объяснить результаты опыта.
ОПЫТ 3. Коррозия алюминия на воздухе и в воде
Алюминий способен проявлять высокую химическую активность, если с его поверхности снять защитную оксидную пленку. Для удаления оксидной пленки, опустить две алюминиевые пластинки в раствор щелочи на 1-2 минуты, промыть водой и осушить фильтровальной бумагой. Опустить обе пластинки в раствор Hg2(NO3)2 на 1-2 минуты. Вынув алюминиевые пластинки из пробирки, осушить фильтровальной бумагой и одну пластинку оставить на воздухе, сделав 2-3 царапины на поверхности металла. Что происходит с алюминиевой пластинкой на воздухе? Каков состав белого порошка, которым обрастает пластинка?
Другую пластинку поместить в дистиллированную воду. Какой газ выделяется при опускании алюминиевой пластинки в воду? Если выделение газа незначительно, осторожно потереть поверхность пластинки стеклянной палочкой. Записать схемы гальванических элементов и уравнения анодного и катодного процессов, протекающих в первом и втором случаях.
ОПЫТ 4. Пассивация металлов и роль защитных пленок в процессе коррозии (опыт а – демонстрационный).
а) Очистить наждачной бумагой два стальных гвоздя. Один гвоздь пассивировать, опустив его в пробирку с концентрированным раствором азотной кислоты на 1-2 минуты. Обработка в кислоте проводится под тягой! Записать свои наблюдения. Ополоснуть гвоздь водой и опустить в пробирку с разбавленным раствором серной кислоты. Отметить скорость выделения водорода.
Для сравнения опустить в раствор серной кислоты необработанный гвоздь. Написать уравнения анодных и катодных процессов, протекающих при коррозии железа в серной кислоте. На каком образце скорее выделяется водород? Отметить роль оксидной пленки, образованной на металле при обработке концентрированной азотной кислотой, по отношению к коррозии.
б) Для удаления оксидной пленки опустить пластинку алюминия в раствор щелочи, промыть водой и осушить фильтровальной бумагой. Затем поместить на 1 минуту в раствор соли ртути (II) и вновь промыть пластинку водой. При этом идет реакция:
2Al + 3Hg2+ = 2Al3+ + 3Hg
и на поверхности алюминия образуется амальгама – его раствор в металлической ртути. На амальгамированном алюминии оксидная пленка не удерживается и поверхность металла на воздухе быстро покрывается хлопьями. Снять хлопья фильтровальной бумагой и поместить пластинку в пробирку с водой. Написать соответствующие уравнения реакций.
Ускоряющее влияние на коррозию алюминия оказывает возникающая гальванопара Al – Hg. Написать схему ее действия.
ОПЫТ 5. Катодные и анодные защитные покрытия
В две пробирки налить (1/2 объема) воды и добавить в каждую пробирку по 1-2 мл H2SO4 и по 2-4 капли раствора красной кровяной соли K3[Fe(CN)6]. В одну пробирку поместить оцинкованное железо, а в другую – луженое. Отметить изменение цвета раствора в пробирках. Учесть, что красная кровяная соль образует с ионами Fe2+ соединение синего цвета.
Объяснить наблюдения, записать уравнения анодных и катодных процессов и привести схемы работы коррозийных гальванопар. В каком случае корродирует железо? Указать, какое из изученных покрытий было анодным, а какое – катодным.
ОПЫТ 6. Влияние ингибитора на скорость коррозии
Налить в 3 пробирки (до 1/4 объема) раствор соляной кислоты. В одну из пробирок поместить пластинку цинка, во вторую – железные стружки и в третью – пластинку алюминия. Наблюдать выделение водорода. Затем добавить в каждую из пробирок немного уротропина. Какой наблюдается эффект?
3.3 КЕЙС-ЗАДАНИЯ
1. Газовая коррозия является примером химической коррозии. Она протекает на поверхности металла в условиях повышенных температур.
Определите термодинамическую возможность газовой коррозии изделия из углеродистой стали, протекающей по реакции:
Fe(т) + H2O(г) = FeO(т) + H2(г),
если это изделие эксплуатируется при 700°С под действием водяного пара с относительным давлением р H2O = 6 и р H2 = 1 (см. приложение Д).
2. Наиболее распространённый вид коррозии – это коррозия в электролитах. Такой вид коррозии называется электрохимический.
Возможна ли электрохимическая коррозия олова (Sn) в водном растворе (рН=6) при контакте с воздухом. Напишите уравнения реакций анодного и катодного процессов. При каких значениях рН возможна коррозия с выделением водорода? (см. приложение В).
3. Наиболее распространенным окислителем, выполняющий роль деполяризатора, является кислород.
При электрохимической коррозии стального (железного) изделия с поглощением кислорода и без выделения водорода за 2 минуты работы коррозийного элемента образовалось 0,225 г Fe(OH)2. Вычислите объем кислорода при нормальных условиях, израсходованного на коррозию железа, коррозийный ток и массу растворенного металла.
4. Один из методов защиты металла от коррозии является применение различного рода покрытий – неметаллические, металлические и химические.
Стальное изделие имеет цинковое покрытие. Какой из металлов будет окисляться при коррозии, если эта пара металлов попадает в нейтральную среду с рН=7? Рассчитайте ЭДС коррозийного элемента для стандартных состояний. При каких значениях рН прекратится процесс выделения водорода? (см. приложение В).
3.4 КОНТРОЛЬНЫЕ ВОПРОСЫ
Почему коррозийная стойкость металла увеличивается при уменьшении примесей в нем? Какой металл в паре Fe – Ni будет растворяться в разбавленном растворе уксусной кислоты? На каком металле выделяется водород? В контакте с цинком или с железом коррозия магния будет происходить сильнее? Привести схему процесса коррозии. Каковы причины возникновения коррозийных микрогальванических элементов? Подвергается ли коррозии во влажном воздухе стальная деталь, покрытая кадмием или хромом при нарушении целостности защитного покрытия?
4 Лабораторная работа

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



