Применение гальванических элементов в строительстве
Электроосмотическая сушка заключается в переносе жидкости в толще стены под действием электростатического поля. Разность потенциалов, необходимая для перемещения ионов жидкости, создается с помощью гальванических элементов, которые монтируются непосредственно в теле влажной стены. Этот метод применяется для сушки кирпичных и каменных стен зданий и сооружений.
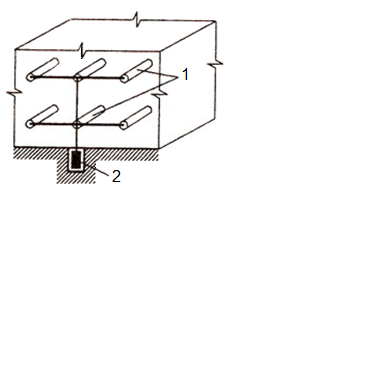
Схема электроосмотического осушения стен с помощью гальванических элементов (гальваноосмоса) приведена на рисунке 2.7.
Рисунок 2.7 Электроосмотическое осушение стен с помощью гальванических элементов | При гальваноосмосе электроды (1) размещают с внутренней стороны стены, причем более активный из них – протектор (2) – в наиболее влажной среде (в грунте под зданием или ниже зоны промерзания). Сущность способа гальва-нических элементов заключается в использовании тока, создаваемого в сырой стене и грунте вследствие химических реакций, протекающих вокруг специально устроенных короткозамкнутых гальванических элементов. |
Эти элементы подпитываются от протектора, заложенного в грунт и служащего причиной самопроизвольного возникновения тока, способствующего перемещению влаги в стене.
Так как два любых металла с разными нормальными электродными потенциалами дают некоторую их разность, гальванические элементы для электроосмотического осушения могут быть выполнены из самых разных металлов. Лучшими по максимальной и стабильной в течение года величине силы тока являются магниевые, магниево-литиевые, медно-цинковые и угольно-цинковые гальванические элементы.
Наибольшую разность потенциалов создают магниевые протекторы, причем длительность их службы при массе от 5 до 10 кг колеблется в пределах от 8 до 20 лет. Протекторы должны иметь цилиндрическую или шаровую форму, так как острые грани, углы и выступающие части быстрее разрушаются.
Электроосмотическое осушение стен гальваническими элементами пока не нашло широкого применения и находится в стадии дальнейшей разработки и совершенствования.
2.2 ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Цель работы: Ознакомление с устройством гальванических элементов и изучение окислительно-восстановительных процессов, протекающих при их работе.
Оборудование и реактивы: Милиамперметр; U – образный электро-литический мостик; химические стаканы; пробирки; наждачная бумага; пластинки меди, цинка, олова, алюминия, кадмия. Растворы: хлорида калия (KCl), насыщ.; сульфата меди (II) (CuSO4), 1М; сульфата цинка (ZnSO4), 1М, 0,0001М; сульфата железа (II) (FeSO4), 1М; хлорида олова (II) (SnCl2), 1М; ацетата свинца (II) ((CH3COO)2Pb), 1M; серной кислоты (H2SO4), 2н.
ОПЫТ 1. Исследование активности металлов
Налить в отдельные пробирки по 1 мл растворов солей цинка, железа (II), меди (II), олова (II), свинца (II) и H2SO4. Опустить в растворы (кроме раствора с одноименными ионами) пластинки металлического цинка. Отметить наблюдения. Повторить аналогичные опыты с пластинками меди, олова, кадмия, алюминия. Из каких растворов вытесняются металлы? Написать уравнения соответствующих окислительно-восстановительных реакций. Записать металлы по убыванию их восстановительной способности, определенной экспериментально. Выписать значения их стандартных электродных потенциалов (см. приложение В). Соответствует ли экспериментальный ряд металлов их положению в электрохимическом ряду напряжений?
ОПЫТ 2. Химический гальванический элемент
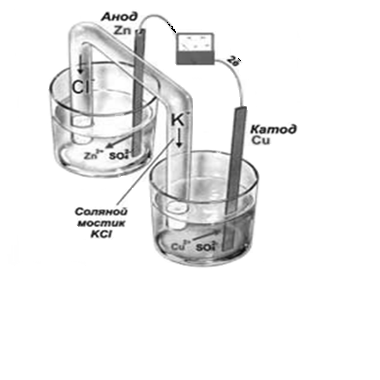
Собрать гальванический элемент, как показано на рисунке 2.8. Для этого цинковую и медную пластинки хорошо очистить наждачной бумагой и опустить в стаканы с растворами одноименных солей. Для замыкания внутренней цепи элемента, солевой мостик (гальванический ключ) заполненный раствором хлорида калия, опустить в растворы солей. Электроды с помощью проводов соединить с миллиамперметром. Что наблюдается?
Рисунок 2.8 Схема установки медно-цинкового гальванического элемента |
Составить схему гальванического элемента. Указать, какие процессы происходят на электродах. Рассчитать ЭДС. До каких пор может работать данный гальванический элемент?
ОПЫТ 3. Концентрационный гальванический элемент
Две цинковые пластинки хорошо очистить наждачной бумагой и опустить в стаканы с растворами сульфата цинка разных концентраций: 1М и 0,0001 М. Пластики соединить с клеммами миллиамперметра, а стаканы – гальваническим ключом. Следить за показаниями миллиамперметра. Составить электрохимическую схему гальванического элемента с указанием процессов протекающих на электродах.
Рассчитать ЭДС полученного концентрационного элемента.
Провести расчет ЭДС гальванических элементов, если концентрации растворов сульфата цинка: 1М и 0,1М; 1М и 0,001М. В каком случае вырабатывается большее количество электричества, почему?
2.3 КЕЙС-Задания
В два стакана налито по 25 мл 0,1 М раствора AgNO3. Растворы соединены солевым мостиком, содержащим КNO3, и в них введены одинаковые серебряные электроды. Разность потенциалов между электродами равна нулю. Почему? В один из стаканов налили 10 мл раствора Pb(NO3)2 , вследствие чего между электродами возникла ЭДС, равная 0,007 В. Чему равна массовая доля примеси серебра в свинце, если раствор Pb(NO3)2 приготовлен растворением 10 г свинца, загрязненного серебром, в азотной кислоте? Коэффициенты активности растворов принять равными 1, температуру 298К. В заряженном свинцовом аккумуляторе, состоящем из шести последовательно соединенных элементов, электролитом является 38%-ная серная кислота (с=1,286 г/см3). Чему равна ЭДС аккумулятора в заряженном состоянии и разряженном, когда концентрация кислоты равна 5%, а с=1,025 г/см3. Известно, что для питания различной аппаратуры используется сухой марганцево-цинковый элемент. Какова должна быть минимальная масса цинкового электрода, при ЭДС элемента, равной 1,5В? Составьте электрохимическую схему и приведите процессы на электродах. В настоящее время, как источники электрического тока, наибольший интерес вызывают низкотемпературные топливные элементы. Среди которых, наиболее простым является водородно-кислородный топливный элемент. Рассчитайте стандартную ЭДС такого элемента, при рабочей температуре 25°С (относительное парциальное давление
2.4 Контрольные вопросы
Вычислить электродный потенциал серебра, опущенного в раствор
его соли с концентрацией 0,001 моль/л. Составить электрохимическую схему свинцово-алюминиевого гальванического элемента. Записать процессы, протекающие на электродах и уравнение токообразующей реакции. Рассчитать ЭДС элемента. В каком направлении будут перемещаться электроны во внешней
цепи следующих гальванических элементов: а) Мg | Мg2+ || Рb2+ | Рb;
б) Сu | Сu2+ || Аg+ | Аg, если концентрации растворов электролитов 1М? Какой металл будет растворяться в каждом из этих случаев? Вычислить потенциал водородного электрода, погруженного:
а) в раствор с рН = 4; б) в раствор с рН = 11. Электродвижущая сила элемента, состоящего из медного и свинцового электродов, опущенных в 1М растворы соответствующих солей, равна 0,47В. Изменится ли ЭДС, если взять растворы с концентрацией 0,001М? Ответ подтвердить расчетом.
3 Лабораторная работа
КОРРОЗИЯ МЕТАЛЛОВ. МЕТОДЫ ЗАЩИТЫ ОТ КОРРОЗИИ
3.1 Теоретическая часть
Коррозия (от лат. сorrodere – разъедать, разрушать) – самопроизвольный процесс разрушения металла вследствие его окисления при воздействии с окружающей средой:
Ме0 – nз = Меn+
Коррозию металлов по характеру ее проявления различают:
- равномерная;
- неравномерная;
- межкристаллитная;
- нитевидная.
Классификация коррозийных процессов по механизму их протекания подразделяет коррозию на химическую, электрохимическую и электрокоррозию.
Химическая коррозия возникает при взаимодействии металлов с сухими газами или неэлектролитами. Этот процесс происходит в отсутствии электролитов. К химической коррозии относится:
- газовая коррозия, которая протекает в газовой среде (Cl2, H2S, SO2 и др.) без конденсации влаги на поверхности металлов при высокой температуре. Такая коррозия происходит при ковке или сварке металлов;
- коррозия в органических жидкостях. Например, коррозия нефтепроводов, коррозия двигателя внутреннего сгорания под действием жидкого топлива.
В результате химической коррозии металл покрывается оксидной пленкой. У некоторых металлов (Al, Zn, Cr и др.) на поверхности образуется плотная защитная пленка, которая замедляет, а иногда и прекращает дальнейшую коррозию металла. Рыхлая оксидная пленка не обладает защитным действием и не предохраняет металл (например, Fe) от дальнейшей коррозии.
Электрокоррозии подвержены металлы, находящиеся под действием блуждающих токов (например, вблизи линий электропередач, трамвайных и троллейбусных линий в городах).
Электрохимическая коррозия металлов – совокупность пространственно разделенных процессов окисления (анодный процесс) и восстановления (катодный процесс). Этот вид коррозии происходит в токопроводящих средах, содержащих электролиты, например, во влажном воздухе или в морской воде.
В основе процессов электрохимической коррозии лежит работа короткозамкнутых микро - или макрогальванических элементов (коррозийных гальванопар), основные моменты которой являются:
1) процесс анодного окисления (роль анода выполняет более активный металл);
2) переход электронов с анодного участка на катодный (в отличие от обычного гальванического элемента электроны движутся внутри металла из-за отсутствия внешней цепи);

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |