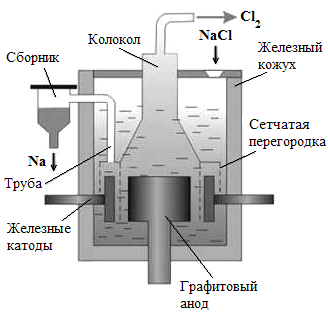

Рисунок 4.2. Схема установки для получения металлического натрия | Рисунок 4.3. Схема установки для электролиза хлорида натрия |
Гальванотехника – область прикладной электрохимии, занимающаяся процессами нанесения металлических покрытий на поверхность как металлических, так и неметаллических изделий при прохождении постоянного электрического тока через растворы их солей. Гальванотехника подразделяется на гальваностегию и гальванопластику.
Гальваностегия (от греч. покрывать) – это электроосаждение на поверхность металла другого металла, который прочно связывается (сцепляется) с покрываемым металлом (предметом), служащим катодом электролизера. Способом гальваностегии можно покрыть деталь тонким слоем золота или серебра, хрома или никеля.
Гальванопластика – получение путем электролиза точных, легко отделяемых металлических копий значительной толщины с различных как неметаллических, так и металлических предметов, называемых матрицами.
С помощью гальванопластики изготовляют бюсты, статуи и т. д. Гальванопластика используется для нанесения сравнительно толстых металлических покрытий на другие металлы (например, образование "накладного" слоя никеля, серебра, золота и т. д.).
Кроме указанных выше, электролиз нашел применение и в других областях:
- получение оксидных защитных пленок на металлах (анодирование); электрохимическая обработка поверхности металлического изделия (полировка); электрохимическое окрашивание металлов (например, меди, латуни, цинка, хрома и др.); электрохимическая заточка режущих инструментов (например, хирургических ножей, бритв и т. д.); получение металлических сплавов; получение гальванических покрытий; электрохимическая очистка производственных сточных вод (электродиализ и обессоливание) – удаление из воды различных примесей, а также извлечение меди и других цветных и драгоценных металлов.
Актуальность электролиза объясняется тем, что многие вещества получают именно этим способом. Преимущество электролиза в относительной дешевизне и простоте. Однако чтобы производство было наиболее выгодным, с наименьшими затратами электроэнергии и с наибольшим выходом продукции, необходимо учитывать различные факторы, влияющие на количество и качество продуктов электролиза (сила тока, плотность тока, температура электролита, материал электродов и др.).
Таким образом, исследование электрохимических процессов, определение факторов, влияющих на них, установление новых способов использования процессов электролиза в промышленных условиях сохранило свою актуальность в наши дни.
Примеры решения задач
Пример 1. Какая масса меди выделится на катоде при электролизе раствора хлорида меди в течение 2 ч при силе тока 5 А?
Решение: Согласно I закону Фарадея:
![]()
Молярная масса эквивалента меди в CuCl2 равна 63,54/2 = 31,77 г/моль.
Подставив в формулу (4.1) значения Mэ = 31,77 г/моль; I = 5 А; ф = 2 ч = 7200 с, получим
![]() г
г
Пример 2. Чему равна сила тока при электролизе раствора в течение 1 ч 40 мин 25 с, если на катоде выделилось 1,4 л водорода (н. у.)?
Решение: Из формулы (4.2) выразим силу тока:
![]() или
или ![]() , где Vэ – эквивалентный объем газа.
, где Vэ – эквивалентный объем газа.
Эквивалентный объем водорода при нормальных условиях равен половине молярного объема 22,4/2 = 11,2 л.
Подставив в приведенную формулу значения VH2 = 1,4 л; Vэ(H2) = 11,2 л;
ф = 1 ч 40 мин 25 с = 6025 с, получим:
![]() А
А
Пример 3. В течение какого времени необходимо пропускать ток силой 2 А через раствор сульфата цинка, чтобы на катоде выделилось 10 г металла, если выход по току составляет 70%?
Решение: Используя формулы (4.4) и (4.1), выразим mПР и ф:
![]() ;
; ![]() ;
; ![]()
Подставив в приведенную формулу значения з = 70%; F = 96500 Кл;
mПР = 10 г; Mэ(Zn) = 65,38/2 = 32,69 г/моль; I = 2 A, находим
![]()
4.2 ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Цель работы: рассмотреть последовательность протекания процессов на электродах при электролизе водных растворов электролитов с растворимым и нерастворимым анодом.
Оборудование и реактивы: электролизер; выпрямитель ВСП-12; графитовые электроды; медный электрод. Растворы: нитрата калия (KNO3), 2%; иодида калия (KI), 0,2М; хлорида (сульфата) цинка (ZnCl2 (ZnSO4)), 5%; сульфата меди (CuSO4), 2%; серной кислоты (H2SO4), 2н. Лакмус 1%; фенолфталеин; крахмал.
ОПЫТ 1. Электролиз раствора нитрата калия
Лабораторная установка для электролиза представлена на рисунке 4.4:
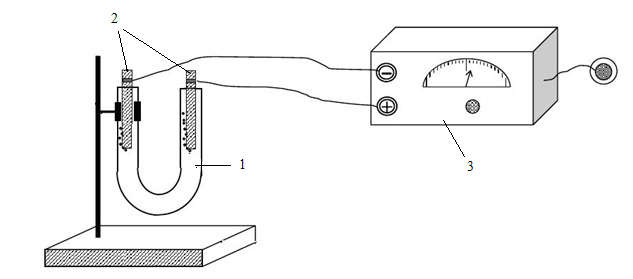
Рисунок 4.4 Лабораторная установка для электролиза
В электролизер (U-образный сосуд) (1) налить ѕ объема раствора нитрата калия и добавить в оба колена сосуда несколько капель раствора лакмуса, опустить в раствор графитовые (инертные) электроды (2) и с помощью проводов присоединить их к выпрямителю тока (3) (см. рисунок 4.4). Пропускать ток в течение 3-5 минут. Наблюдать изменение окраски раствора в катодном и анодном пространстве.
Написать уравнения реакций, происходящих на катоде и аноде. Какие побочные продукты электролиза образуются? Электролиз солей каких металлов подобен электролизу раствора KNO3?
ОПЫТ 2. Электролиз раствора иодида калия
В электролизер налить раствор иодида калия, прибавить в оба колена сосуда по 3-4 капли фенолфталеина и опустить графитовые электроды. Пропустить ток. Наблюдать выделение пузырьков газа и окрашивание раствора у катода. К раствору в анодной части прибавить несколько капель раствора крахмала. Отметить наблюдения. Составить схему электролиза раствора KI.
ОПЫТ 3. Электролиз хлорида (сульфата) цинка
В электролизер налить раствор соли, погрузить угольные электроды и пропустить ток. Отметить выделение соответствующего газа на аноде и образование светло-серого осадка на катоде. Составить схему электролиза раствора соли цинка.
ОПЫТ 4. Электролиз раствора сульфата меди
В электролизер с раствором сульфата меди (CuSO4) опустить графитовые электроды и проводить электролиз в течение нескольких минут. Что наблюдается? Какие вещества выделяются на катоде и аноде? Составить уравнения реакций, протекающих на электродах.
Катод, покрытый медью, оставить для следующего опыта.
ОПЫТ 5. Электролиз с растворимым анодом
а) В электролизер налить раствор серной кислоты, в качестве катода взять графитовый электрод, в качестве анода – графитовый электрод, покрытый медью из предыдущего опыта и проводить электролиз в течение 3-5 минут. Отметить выделение газов на катоде и аноде. Что происходит с медью на аноде?
б) В электролизер с раствором серной кислоты опустить графитовый катод и медный анод. Провести электролиз и отметить выделение соответствующих продуктов на катоде и аноде. Составить схему электролиза раствора серной кислоты с растворимым анодом.
4.3 КЕЙС-ЗАДАНИЯ
Наиболее технологичным и эффективным способом выделения металлов из растворов является электролиз. Определите время, необходимое для выделения всей меди электролизом при силе тока 19,8 А и выходе по току 100 %, если годовой объем очищаемой воды равен 1000 м3, а содержание в нем ионов Cu2+ составляет 28 мг/дм3. Гальваностегия (электроосаждение) – это нанесение на поверхность металлического изделия другого металла. Таким методом можно покрыть деталь слоем золота или серебра, хрома или никеля. Электрохимическое хромирование проводят из раствора смеси хромовой (H2CrO4) и серной (H2SO4) кислот с использованием нерастворимого анода. Рассчитайте время, необходимое для получения хромового покрытия, толщиной 20 мкм на стальной ленте при плотности тока 1 кА/м2 и выходе хрома по току, равном 0,3. Рассчитайте объемы других веществ (при нормальных условиях), выделившихся на электродах с поверхностью, равной 1 м2. Анодное оксидирование (анодирование) широко применяется для обработки металлов и прежде всего алюминия.
При анодировании алюминиевого изделия с поверхностью, равной 1 м2, использовали разбавленный раствор H2SO4 и нерастворимые PbO2 – катоды. Сколько граммов алюминия окислилось, если при нормальных условиях на катоде выделилось 33,6 л газа? Какова толщина слоя анодированного алюминия Al2O3, если плотность Al2O3 составляет 3,85 г/см3 принимая, что растворение беспористого осадка Al2O3 не происходит.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |



