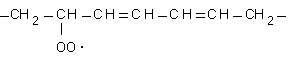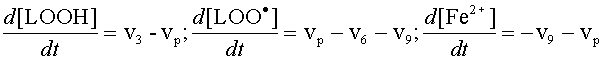В качестве реагента, способного отрывать атом водорода чаще всего служит свободный радикал, например, радикал гидроксила HO·:
HO· + - СH2-CH=CH-СH2-CH=CH-СH2- |
Реакция инициирования может быть записана в виде простого химического уравнения:
HO· + LH → H2O + L· (1)
Двойная связь, как известно, образуется одной парой - элетронов и двумя - электронами. В молекуле полиненасыщенных жирных кислот имеется не одна, а две или более двойнх связей, но они разделены группой - CH2- (метиленовым мостиком). Двойные связи и p-электроны локализованы. В радикале L· имеется не один, а пять одинаковых - электронов, расположенных у соседних углеродных атомов, как это изображено ниже:
![]()
Нельзя определить, какие же из этих электронов образуют двойные связи.
Все они находятся в равном положении, и присоединение какой-либо химической группы к любому из этих пяти углеродных атомов примерно равновероятно.
Можно сказать, что свободная валентность принадлежит не конкретному атому углерода, а делокализована.
Продолжение цепи
В кислород-содержащей среде происходит быстрое присоединение молекулы кислорода к одному из атомов углерода с неспаренным электроном, обычно к крайнему. Образуется радикал перекиси липида:
| или |
|
В дальнейшем мы будем обозначать такой радикал знаком LO2· и называть его липидным диоксиалкил-радикалом.
Реакция образования диоксил-радикала может быть теперь описана таким химическим уравнением:
L· + O2 → LO2· (2)
Радикал LO2·легко отнимает атом водорода от одной из соседних ненасыщенных жирных кислот (LH):
LO2·+ LH → LOOH + L· (3)
Образуется новый липидный алкил-радикал, а затем реакции 2 и 3 повторяются.
Перекисное окисление липидов - это цепная реакция, и её можно наглядно изобразить следующим образом.
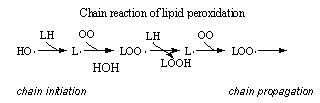
В реакцию продолжения цепи вовлекаются всё новые и новые молекулы субстратов, т. е. молекулярный кислород О2 и полиненасыщенные жирные кислоты LH, и в каждом звене этой цепной реакции образуется молекула продукта - гидроперекиси липида LOOH
В каждый данный момент протекает какая-то одна частная реакция цепного окисления, так что цепи разворачиваются во времени, а не в пространстве.
Обрыв цепей
В конце концов цепи обрываются, поскольку свободные радикалы L·;и LO2·;, "ведущие" цепи окисления, исчезают из-за одной из возможных реакций обрыва цепей
Это могут быть следующие реакции:
L· + L· → LL (4) |
Последняя реакция диспропорционирования радикалов LO2·; интересна тем, что она сопровождается hemilumм - хемилюминесценцией.
В липид-содержащих системах длина цепей может составлять десятки и сотни звеньев.
Для организма цепное окисление липидов - весьма нежелательное явление не только потому, что оно приводит к бесполезному сжиганию ценных компонентов клетки, но ещё и потому, что некоторые продукты цепного окисления липидов чрезвычайно токсичны.
В связи с этим имеется целая система защиты от перекисного окисления, в частности, имеются вещества, "перехватчики" свободных радикалов, которые тормозят цепное окисление за счёт ещё одной реакции обрыва цепей:
L· + InH → LH + In· (7)
где In·; - свободный радикал ингибитора цепного окисления.
К числу молекул - перехватчиков радикалов относятся токоферол (витамин Е), женские половые (стероидные) гормоны, коэнзим Q (убихинон), многие другие соединения.
Хотя в реакции 7 образуются радикалы этих соединений, эти радикалы недостаточно активны, чтобы оторвать атом водорода от молекул жирных кислот, и поэтому не инициируют новых цепей окисления.
Обычно они быстро исчезают, например, вследствие взаимодействия друг с другом:
In· + In· → In-In (8)
Все соединения, тормозящие процессы цепного окисления липидов, называются антиоксидантами.
К числу антиоксидантов относятся и перехватчики свободных радикалов. Антиоксидантными свойствями в определённых условиях обладают ионы металлов переменной валентности в восстановленной форме, в частности, ионы Fe2+. Они также способны перехватывать свободные радикалы в одной из следующих реакций:
Fe2+ + L· + H+ → Fe3+ + LH (9) |
Разветвление цепей
В большинстве случаев ионы Fe2+ обладают однако не анти-, а прооксидантным действием, т. е. они не подавляют, а наоборот, резко усиливают процессы перекисного окисления.
Это происходит потому, что ионы двухвалентного железа вступают в реакцию с продуктом перекисного окисления - гидроперекисями липидов:
Fe2+ + LOOH → Fe3++ LO· + OH - (10)
В результате появляется новый свободный радикал (алкоксильный радикал липида) LO·, который инициирует образование новой цепи окисления:
LO·+ LH → LOH + L· (11) |
и далее реакции 2-3, 2-3, 2-3 и т
Разветвление цепей более наглядно видно на схеме:
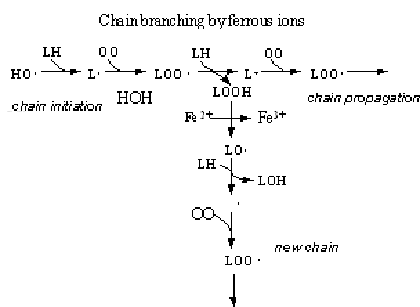
Упрощение схемы реакций
Совокупность химических уравнений кинетики цепного окисления липидов выглядит солидно:
HO· + LH → HOH + L· (1) |
Система дифференциальных уравнений, описывающих процесс, будет очень сложной, а константы скоростей большинства перечисленных реакций неизвестны.
Можно однако существенно упростить систему химических, а значит - и дифференциальных уравнений кинетики, если использовать два важных закона химической кинетики:
Правило 1: Скорость нескольких последовательных реакций равна скорости самой медленной из них.
Это правили позволяет заменить последовательные реакции одной обобщённой реакцией, приняв константу скорости этой реакции равной константе скорости самой медленной из последовательных реакций.
В нашем случае реакции 2 и 3 - это последовательные реакции. Для наших целей не очень важно, какую из них считать более медленной. В кислород - содержащей среде скорость реакции 3 во много раз ниже скорости реакции 2, поэтому уравнение реакции продолжения цепи можно записать так:
![]()
а константа скорости этой реакции будет равна константе скорости реакции 3, которую мы обозначим как k3; константы скоростей мы в дальнейшем будем писать над стрелкой в химическом уравнении реакции.
Правило 2: Из нескольких параллельных реакций наибольшую роль играет самая быстрая; для простоты, остальными реакциями иногда можно пренебречь
Это правило позволяет заметно упростить приведенную выше схему из одиннадцати реакций.
В присутствии кислорода воздуха радикалов LO· и L· гораздо меньше, чем радикалов LOO·; поэтому реакциями 4 и 5 можно пренебречь оставив только одну реакцию взаимодействия радикалов - реакцию 6. При наличии в среде ионов Fe2+ и при незначительной конццентрации других антиоксидантов часто можно пренебречь реакцией 7, оставив реакцию 9. Реакцию 9а мы тоже не будем пока принимать во внимание. В отсутствие иных источников свободных радикалов, образование новых радикалов происходит только в реакции 10 (реакция разветвления цепей). Обозначим константу скорости этой реакции как kp. Реакцией 1 можно пренебречь, если нет источника радикалов HO·.После всех этих упрощений получаем систему химических уравнений цепного окисления липидов, содержащую всего четыре реакции:
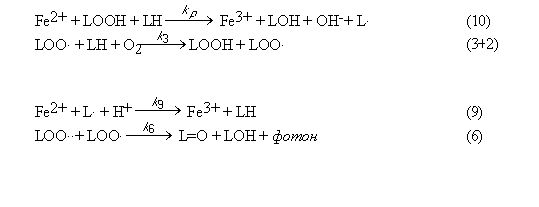
Дифференциальные уравнения кинетики
Реакции 9 и 10 выглядят, как тримолекулярные, или как реакции третьего порядка. В водной забуференной среде, однако, концентрация протонов постоянна, и эту величину можно включить в постоянную - константу скорости k9. Поэтому мы будем рассматривать реакцию 9 как бимолекулярную с константой скорости второго порядка k9.
Также и концентрация субстрата окисления LH внутри мембраны достаточно велика и мало изменяется во времени, поэтому и реакцию 10 можно рассматривать как бимолекулярную (второго порядка) с константой скорости.
После этого введения, запишем дифференциальные уравнения кинетики, описывающие скорости приведенных выше частных (или парциальных) реакций цепного окисления липидов:
v3-k3[LH][LOO·]; v6 - k6[LOO·]2; |
Дифференциальные уравнения, описывающие изменение концентраций основных участников реакции с учётом уравнений, приведенных выше, можно записать так:
| (15-17) |
Расчеты концентраций компонентов на ЭВМ
Как ни старались мы упростить систему химических и дифференциальныых уравнений кинетики, конечная система уравнений третьего порядка всё равно не может быть решена аналитически.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |