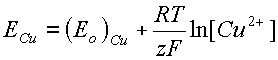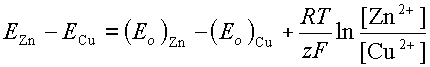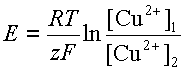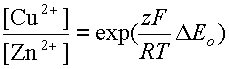|
| (3) |
Величина равновестного электродного потенциала, как видно из этого уравнения, зависит от концентрации ионов цинка:
|
| (4) |
При концентрации С = 1 моль/литр величина потенциала E приобретает совершенно определенное значение E0 = μ0/zF и называется стандартным электродным потенциалом пары Zn/Zn2+.
При концентрациях, отличающихся от одного моля, электродный потенциал равен
|
| (5) |
Все приведенные рассуждения могут быть повторены для реакции окисления меди до ионов меди на медном электроде. Для пары Cu/Cu2+ существует свой стандартный электродный (редокс) потенциал.
Если мы возьмем различные другие пары метал/катион, то для всех них величина стандартного электродного потенциала тем выше, чем больше энергии выделяется при восстановлении ионов металла, т. е. присоединении электронов к этим ионам.
Гальванический элемент как система из двух полуэлементов и двух проводников
Вернемся к рисунку 1 раздела "Гальванический элемент". Можно видеть, что в гальваническом элементе электроды соединены двумя проводниками: по внешней цепи электроны идут по металлическому проводнику (проводнику первого рода), а по внутренней цепи ионы идут по солевому мостику, в сущности, по раствору электролита (проводник второго рода). Превращение тока электронов в ток ионов и обратно происходит на границах разделов фаз за счет реакций окисления и восстановления. При этом ток будет в общем случае результатом этих химических реакций. Иными словами, гальванический элемент может быть источником электричества во внешней цепи, а между электродами может возникать определенная разность потенциалов, которая будет зависеть от свойств полуэлементов и электрического сопротивления во внешней и внутренней цепях.
Электродвижущая сила гальванической ячейки
При очень высоком входном сопротивлении измерительного прибора (вольтметра) на рисунке 1, сопротивление растворов электролитов в ячейках и солевом мостике будет относительно настолько мало, что его можно считать равным нулю. Это означает, что в уравнениях 1-3 потенциалы E отсчитываются от одного уровня и их можно сравнивать, т. е. складывать и вычитать. Запишем электродные потенциалы для меди и цинка, базируясь на уравнении 5 в разделе "Электродный потенциал":
|
| (6) |
Разность потенциалов между электродами будет равна:
|
| (7) |
Для случая, когда внутреннее сопротивление источника разности потенциалов пренебрежимо мало, разность потенциалов между электродами называется электродвижущей силой (ЭДС) и обозначается буквой E.
Концентрационный элемент
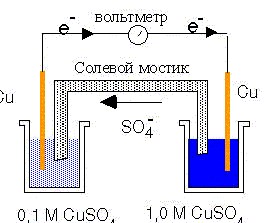
Уравнение 7 в разделе "ЭДС гальванического элемента" показывает, что в принципе "батарейка для карманного фонаря" может быть изготовлена из двух одинаковых электродов одного и того же металла, но опущенных в растворы соли разной концентрации, как это изображено на рис. 5
Рис. 5. Концентрационный элемент.
В этом случае электродвижущая сила ячейки будет равна:
| (8) |
В случае, приведенном на рис. 8, ЭДС гальванического элемента будет равна приблизительно 60 Мв.
Стандартный электрод. Восстановительный потенциал
Во всех предыдущих уравнениях фигурируют величины стандартных редокспотенциалов Eo, которые определены как разность потенциалов между электродом и одномолярным раствором иона, в который погружен электрод. К сожалению, не существует методов прямого определения этой разности потенциалов: всё, что мы можем, - это измерить разность потенциалов между двумя электродами, погруженными в растворы, соединенные электролитом. Тогда потенциалы водных фаз равны, и разность потенциалов между электродами описывается уравнением 7, которое при концентрациях электролитов в гальванической ячейке, равных одному молю, существенно упрощается:
|
| (9) |
Эта величина может быть названа стандартной" электродвижущей силой" ячейки. Физический смысл уравнения 9 заключается в том, что величина стандартной электродвижущей силы гальванического элемента, которую можно измерить экспериментально, равна разности электродных потенциалов, которые определены как теоретическая величина (см. уравнение 5).
Разумеется, для разных пар электродов разности потенциалов будут разными. Естественно принять потенциал какого-то одного электрода за нуль, чтобы от него отсчитывать потенциалы остальных электродов. В качестве такого стандартного электрода решено использовать водородный электрод, схематически изображенный на рис. 6.
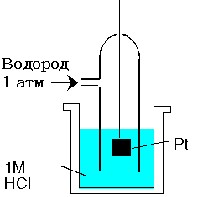
Рис. 6. Стандартный водородный электрод.
Платина адсорбирует водород в водородном электроде и на границе электрод/электролит протекает окислительно-восстановительная реакция:
H2 ![]() 2H+ + 2e-
2H+ + 2e-
Разность потенциалов между цинковым и водородным электродом при концентрациях иона цинка (и водорода) 1М
| (9) |
называется стандартным восстановительным потенциалом цинка, потому что характеризует способность цинка восстанавливать водород. Поскольку, по определению, потенциал стандартного водородного электрода равен нулю, стандартный восстановительный потенциал цинка может быть обозначен как
| (10) |
В литературе используются и другие термины, эквивалентные термину "стандартный восстановительный потенциал", а именно: стандартный потенциал, стандартный окислительно-восстановительный потенциал, восстановительный потенциал, окислительно-восстановительный потенциал. Во избежание путаницы лучше пользоваться первым из перечисленных терминов.
Равновесие при окислительно-восстановительной реакции
Если электроды в гальванической ячейке соединены проводником (солевым мостиком), то под действием разности потенциалов через эту цепь начнет протекать ток. Совокупность реакций, протекающих при этом в гальванической ячейке, может быть записана в виде двух уравнений:
Zn → Zn2+ + 2e -
Cu2+ + 2e - → Cu
В конечном счете количество электронов в системе остаётся неизменным, а происходит окисление цинка и восстановление ионов меди
Zn + Cu2+ → Zn2+ + Cu
В ходе реакции количество ионов меди в ячейке с медным электродом будет уменьшаться, а ионов цинка в ячейке с цинковым электродом - увеличиваться. При этом разность потенциалов между электродами будет снижаться до тех пор, пока не наступит равновесия, при котором разность потенциалов станет равной нулю. Из уравнения 7 следует, что при этом
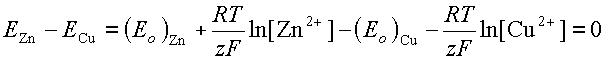 .
.
Отсюда находим разность стандартных электродных потенциалов:
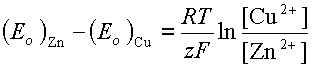
Это позволяет найти отношение концентраций ионов Cu2+ и Zn2+ при равновесии:
| , где |
| (11) |
Из таблицы можно найти разность стандартных восстановительных потенциалов для цинка и меди (ΔEo = - 0.91). Поскольку F/RT = 37,4353, отношение ионов меди к ионам цинка в равновесии составит всего 1,6•10-15. Иными словами, практически все ионы меди восстановятся, а цинк окислится. Ионы меди выступают здесь как окислитель, а металлический цинк - как восстановитель.
Восстановительные потенциалы
Из предыдущих разделов совершенно ясно, что в уравнениях для потенциалов гальванических элементов мы можем смело заменять стандартные электродные потенциалы на восстановительные потенциалы и наоборот. Поэтому во многих руководствах эти термины употребляются как эквивалентные, хотя это не вполне корректно. Дело в том, что восстановительный потенциал - величина, находимая в эксперименте и измеряемая относительно некоторого общепринятого стандарта, а величина электродного потенциала - величина чисто теоретическая и непосредственно измерена быть не может. Вместе с тем разность потенциалов (а именно ее только и приходится использовать) в обоих случаях будет одной и той же.
Ниже приведены стандартные восстановительные потенциалы для некоторых полуэлементов (в химии они называются также окислительно-восстановительными парами, или редокс парами).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |



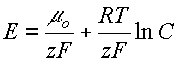
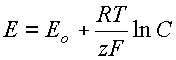
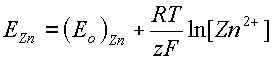 и
и