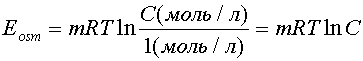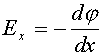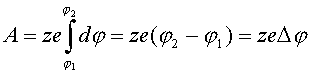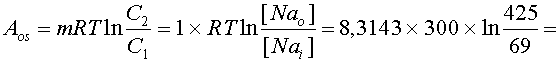| (7) |
В последнем уравнении C - это безразмерная концентрация, т. к. это число, равное отношению молярной концентрации вещества к его концентрации 1М.
Электрическая работа
Напомним некоторые сведения из электростатики. Перемещение заряда q = ze в электрическом поле c напряженностью E обусловлено действием на заряд силы F = zeE. Перемещение заряда на расстояниеdx в направлении, противоположном действующей на него силе, потребует совершения работы, равной:
| (8) |
Напряженность поля связана с градиентом потенциала в направлении поля (ось X) уравнением:
| (9) |
Из последних двух уравнений получаем уравнение работы, затрачиваемой на перемещение иона в электрическом поле:
| (10) |
Таким образом, работа, затрачиваемая на перенос иона с зарядом ze из точки с потенциалом j1 в точку с потенциалом j2 равна:
| (11) |
где e - элементарный заряд, т. е. заряд протона в Кулонах, а z - безразмерный заряд, иногда называемый валентностью иона. Величина z для ионов Na+ , K+, Cl-, Ca2+ и Fe3+ составляет соответственно 1, 1, -1, 2 и 3.
Работа при переносе зарядов через мембрану
Работа, необходимая для перемещения m киломолей ионов из облати с потенциалом j1 в область с потенциалом j2, равна:
| (12) |
где NA - число Авогадро, а F - число Фарадея (заряд в Кулонах одного киломоля одновалентных ионов).
Задача Расчитать работу, которую нужно затратить, для переноса одного моля ионов Na+ из клетки в окружающую среду. Условия даны в Таб.2.
Таблица 2: Концентрации натрия и потенциалы внутри и вне клетки (гигантский аксон кальмара в морской воде)
Концентрация натрия в клетке [Na+i], мМ | 69 |
Концентрация натрия в среде [Na+o], мМ | 425 |
Внутриклеточный потенциал ji, мВ | -60 |
Внеклеточный потенциал jo, мВ | 0 |
Температура | 27оС=300K |
Решение: Работа складывается из осмотической и электрической составляющих. Осмотическую работу расчитываем по уравнению 6:
| 4534,6 кДж |
Электрическую работу при переносе одного киломоля ионов находим по уравнению 12:
| 5789,22 кДж. |
Общая работа по переносу ионов равна 4534,6+5789,22 = 10323,82 кДж на каждый киломоль или 10,32 кДж на моль.
Единицы энергии и работы
Ниже даны соотношения различных единиц энергии, употребляемых в разных случаях.
Таблица 3. Соотношение единиц энергии в разных системах.
1 джоуль (Дж) = 107 эрг = 107 дин. см = 107 г. см2.с-2. |
Принятая в международной системе единиц СИ единица энергии - Джоуль - не очень-то наглядна. Немногим лучше килокалория. Гораздо понятнее во многих случаях другая единица энергии - электрон-вольт.
Например, в рассмотренной выше задаче электрическую энергию переноса иона сразу можно найти равной 0,060 эВ, и смысл этой величины вполне понятен: столько энергии требуется, чтобы перенести один ион натрия из области с потенциалом -60мВ в область с потенциалом 0 мВ, поскольку [0мВ-(-60мВ)] = 60 мВ
Электрохимический потенциал ионов
Энергия некоторого одного киломоля ионов отличается от энергии одного иона в NA раз (NA - число Авогадро). Общая энергия моля ионов в растворе называется электрохимическим потенциалом иона. Электрохимический потенциал равен работе, которую нужно затратить для того, чтобы:
| (13) |
Реакции окисления-восстановления
Электрохимические процессы
Гальваническая ячейка
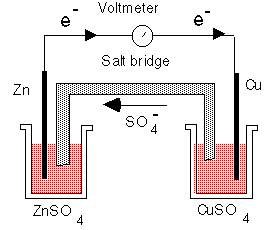
Схема гальванического элемента (гальваничесвой ячейки) приведена на рис. 1. Металлические электроды, в данном случае цинковая и медная пластинки, опущены в растворы электролита; в нашем случае это растворы ZnSO4 и CuSO4, в которых концентарции ионов металлов мы будем обозначать, как обычно, [Zn2+] и [Cu2+]. Одна пара (электрод + раствор соли того же металла) называется полуэлементом. Таким образом, гальванический элемент состоит из двух полуэлементов, соединенных проводником — солевым мостиком, по которому свободно перемещаются ионы и который выравнивает потенциалы в растворах электролитов.
| Рис. 1. Гальванический элемент (A galvanic cell). Солевой мости заполнен элетролитом, обычно KCl или NH4NO3, который проводит электрический ток ( в виде потока ионов). |
Электродные реакции
Рассмотрим, что происходит на границе между электродом, скажем, цинковым (слева) и омывающем его раствором соли. Атомы цинка могут переходить из металлической решетки в водный раствор в виде ионов цинка Zn2+; при этом освободившиеся электроны уходят по электрической цепи, т. е. происходит процесс:
Zn ![]() Zn2+ + 2e-
Zn2+ + 2e-
Отрыв электрона от цинка называется процессом его окисления, присоединение электронов к ионам цинка называют их восстановлением. Слева направо протекает окислительная реакция, а справа налево - восстановительная.
Какая же из этих реакций окажется преобладающей? - Это зависит от разности потенциалов между электродом и окружающим раствором, которую обозначим через E и назовем электродным потенциалом. Интуитивно мы понимаем, что увеличение потенциала будет способствовать восстановлению ионов цинка до металлического цинка, тогда как его уменьшение - наоборот, окислению цинка до ионов (см. рис. 2).
|
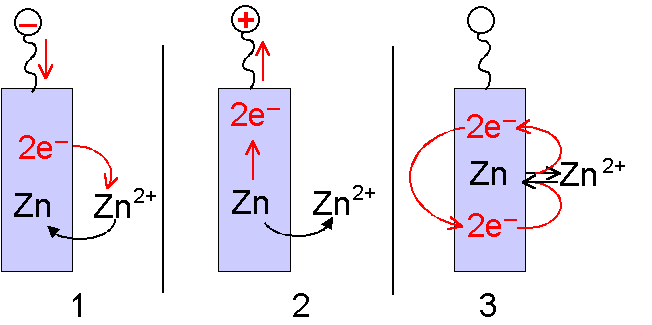
Рис. 2. Влияние электродного потенциала на направление окислительно-восстановительной реакции на электроде.
1 - при отрицательном потенциале доминирует перенос электронов с электрода (восстановление Zn2+).
2 - при положительном потенциале доминирует перенос электронов на электрод (окисление Zn и выход ионов Zn2+ в раствор).
3 - при определенном электродном потенциале Eo устанавливается равновесие.
Электродный потенциал
Рассмотрим количественно связь между концентрацией ионов в растворе и равновесным электродным потенциалом. Для этого рассчитаем количество энергии, которую надо затратить на восстановление одного моля ионов цинка до металлического цинка (т. е. для перехода цинка из раствора на электрод).
Как мы знаем, энергия моля ионов цинка называется электрохимическим потенциалом этого иона, который равен:
|
| (1) |
Заметим, что потенциал электрода по отношению к раствору равен E, и если принять потенциал электрода за начало отсчета (т. е. за нуль), то потенциал раствора будет равен j = - E. Итак:
|
| (2) |
Очевидно, что такое количество энергии надо затратить для того, чтобы образовался один моль ионов цинка за счет их окисления и выхода ионов в раствор. Эта величина (m.) зависит, как видно из уравнения 1, от потенциала E на электроде и от концентрации ионов цинка С. Чем выше концентрация цинка в растворе и чем меньше потенциал электрода, тем труднее растворятся этому положительно заряженному иону. При малом низком потенциале и высокой концентрации ионов цинк вообще перестанет растворяться, а наоборот, ионы цинка из раствора, соединяясь с электронами, будут оседать на электроде в виде слоя металлического цинка. Изменение энергии системы будет равно нулю при равновесии.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |