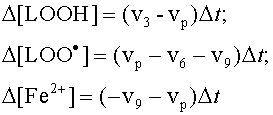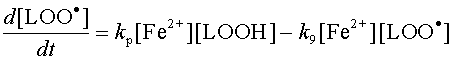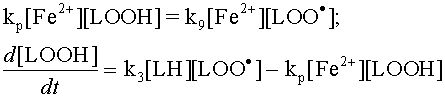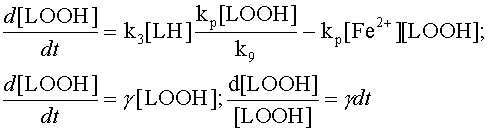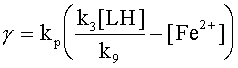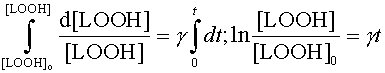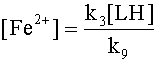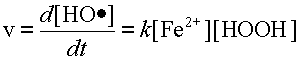Однако если мы знаем константы скоростей и начальные концентрации участников реакции, то можно расчитать численным методом с использованием ЭВМ концентрации всех участников реакции как функцию времени.
Самый простой метод - Эйлера и Коши, при котором бесконечно малые заменяются на достаточно малые приращения, а интегрирование заменяется суммированием. Процедура вычислений сводится к следующему.
Переписываем систему дифференциальных уравнений в виде обычных алгебраических уравнений с использованием очень малых приращений концентраций веществ и времени:
| (18-20) |
Задаём достаточно малую величину t и расчитываем величины D1[LOOH], D1[LOO·] и D1[Fe2+]. Находим для времени t1 = 0 + t величины:
[LOOH]1 = [LOOH]0 + D1[LOOH] (21) |
[LOOH]2 = [LOOH]1 + k2[LOOH] (24) |
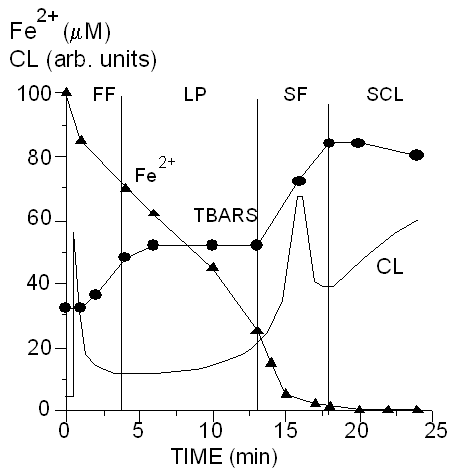
В качестве такого рода экспериментальных данных могут служить кривые тапа приведенных на рис.1 (суспензия митохондрий) или на рис.2 (суспензия фоосфолипидных везикул - липосом).
| Рис. 2. Кинетика окисления ионов двухвалентного железа (Fe(II), накопления продукта перекисного окисления липидов - малонового диальдегида (MDA) и хемилюминесценции (CL) в суспензии фосфолипидных везикул - липосом. |
Дальнейшие упрощения схемы реакций
При некоторых дополнительных упрощениях системы удаётся свести систему дифференциальных уравнений до уравнения первого порядка, которое можно решить аналитически.
Эти упрощения, правда лишают нас возможности построить всю кривую кинетики процесса, но позволяют расчитывать её небольшие участки, а главное - лучше понять некоторые особенности реакций.
Первое упрощение основано на допущении, что скорости частных реакций значительно превышают скорость цепного окисления в целом. Смысл этого допущения можно пояснить, анализируя уравнение, описывающее скорость изменения концентрации радикалов LOO· :
| (27) |
Видно, что скорость появления новых радикалов определяется разностью скоростей двух частных реакций: разветвления цепи и обрыва цепи. Если считать, что скорость образования радикалов гораздо меньше скорости каждой из частных реакций, то можно приравнять нулю правую часть уравнения. Тогда
| (28) |
Порядок системы уравнений понижается при этом на единицу. Такое упрощение, называемое стационарным приближением Боденштейна-Семёнова, предполагает большую длину цепей окисления.
Надо однако заметить, что основной вывод, к которому мы подводим читателя, сохраняется и без допущения Боденштейна-Семёнова, но требует более сложных математических выкладок.
Запишем в развёрнутом виде уравнения - С учётом приближения Боденштейна-Семёнова:
| (29-30) |
В этих уравнениях кроме концентраций гидроперекисей и радикалов фигурирует ещё одна переменная - концентрация ионов железа.
Чтобы решить систему уравнений, нам придётся использовать очень небольшие интервалы времени, в пределах которых величина [Fe2+] не успевает сильно измениться, и тогда мы можем рассматривать её как константу, величина которой в рассматриваемый момент времени нам известна.
С этим дополнительным допущением произведём подстановку значения [LOO·] из первого уравнения во второе и разделим переменные:
| (31) |
где |
|
Триггерная роль ионов двухвалентного железа
Проинтегрируем последнее уравнение *:
| (33) |
Из этого уравнения, а также из уравнения ** следует, что:
| (34) |
Последние уравнения показывают, что как концентрация гидроперекисей в системе, так и концентрация цепей окисления (которая равна концентрации радикалов, ведущих цепи) изменяется во времени по экспоненте.
Будет ли реакция самоускоряющейся или затухающей, зависит от знака индекса в показателе степени.
При "больше 0" процесс будет самоускоряющимся, при "меньше 0" - самозатухающим. Когда "равно 0", сорость процесса будет постоянной во времени.
От чего же зависит сам индекс?
Это можно увидеть, вернувшись к уравнению.
| (35) |
Эту концентрацию железа мы назвали "критической концентрацией" обозначили как [Fe2+]*.
Из уравнений следует, что g=0 при [Fe2+]=[Fe2+]*. Стационарная реакция.
g будет больше 0 при [Fe2+]меньше[Fe2+]*. Ускоряющаяся реакция.
g будет меньше 0 при [Fe2+]больше[Fe2+]*. Затухающая реакция.
Кинетика химических реакций
Введение
Когда происходит химическая реакция, то одни вещества - субстраты реакции - превращаются в другие - продукты реакции. Соответственно этому, с течением времени после начала процесса концентрация субстратов уменьшается, а концентрация продуктов - возрастает. Зависимость изменения концентрации участников реакции (т. е. субстратов и продуктов) от времени называют кинетикой реакции. Кривые таких зависимостей называют кинетическими кривыми, а математические уравнения, которые описывают кинетические кривые, называют уравнениями кинетики.
Итак, повторим некоторые определения:
- Субстраты - вещества, вступающие в реакцию Продукты - вещества, образующиеся в результате реакции Промежуточные вещества - продукты, сразу же вступающие в новую реакцию Скорость реакции - изменение концентрации одного из продуктов, который рассматривается в качестве главного.
Скорость химической реакции
Концентрации веществ в химии принято выражать в киломолях на кубический метр (кмоль/м3) или, что то же самое, в молях на литр (моль/л). Концентрации в таких единицах называют молярными концентрациями и обозначают большой буквой М. Полумолярный раствор (0,5 моль/л) NaCl обозначают как 0,5М NaCl.
Молярная концентрация вещества в химической кинетике обозначается формулой того же вещества, заключенной в квадратные скобки. Так [Fe2+] - это молярная концентрация ионов двухвалентного железа.
Скорость химической реакции - это изменение концентрации какого-либо из участников реакции за секунду. Таким образом в реакции:
Fe2+ + HOOH → Fe3+ + OH - + HO•
скорость реакции это:
|
От чего зависит скорость реакции
Интуитивно, каждый понимает, что число молекул, которые вступят в реакцию за единицу времени, зависит от ряда обстоятельств:
от концентрации реагирующих молекул, т. е. от концентрации первого субстрата реакции; в нашем случае это концентрация ионов Fe2+. от вероятности встретить другую молекулу, которая пропорциональна числу молекул в единице объёма, а следовательно пропорциональна молярной концентрации второго субстрата реакции; в нашем случае это величина [HOOH]. от вероятности того, что столкнувшиеся молекулы прореагируют. Обозначим её через р.Таким образом, скорость реакции в нашем случае будет равна:
| (1) |
,
где K - коэффициент пропорциональности. Произведение констант K × p в свою очередь является некоторой постоянной и называется константой скорости реакции. Обозначим её через k.
| (2) |
Порядок рeакции
Поскольку скорость реакции взаимодействия двух веществ пропорциональна произведению концентраций этих двух субстратов, такого типа реакции называются реакциями второго порядка.
Если бы для реакции требовалось одновременное участие трёх субстратов, то скорость её должна была бы зависеть от произведения концентраций всех трёх веществ, и мы бы имели реакцию третьего порядка. Этого однако практически не бывает, поскольку в подобных ситуациях сначала обычно реагируют две молекулы. а уж потом в дело вступает третья.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |