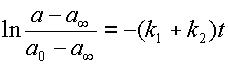Известны реакции, где имеется всего один субстрат; сюда относятся реакции распада или изомеризации веществ. В этом случае скорость реакции пропорциональна концентрации этого одного субстрата. Такие реакции называются реакциями первого порядка. Скорость реакции первого порядка A → B равна:
| (3) |
Кинетика простейших реакций
Изучение химических реакций включает в себя выяснение строения продуктов реакции и изучение скорости реакции, а также зависимости скорости от условий протекания реакции: температуры, состава и свойств растворителя и т Практически исследователь имеет возможность, используя различные методы анализа, например спектрофотометрию, измерять непрерывно или время от времени концентрацию одного или нескольких субстратов и продуктов. Зависимость концентрации от времени (кинетические кривые) сравниваются с кривыми, полученными путём расчётов, т. е. с результатами математического моделирования процесса. Рассмотрим, как будут выглядеть кинетические кривые в разных случаях.
Реакции первого порядка
Как уже говорилось, кинетика реакции первого порядка описывается дифференциальным уравнением 3, из которого можно сразу найти зависимость от времени концентрации субстрата реакции [A]. Для этого разделим переменные и проинтегрируем:
| (4) |
Откуда
| (5) |
Если все молекулы субстрата A превратились в молекулы продукта B, то найти изменение во времени концентрации продукта можно, используя уравнение материального баланса:
| (6) |
Откуда
| (7) |
Кривые зависимости субстрата и продукта реакции от времени даны на рис.1.
| Рис. 1. Кинетика реакции первого порядка Построено по уравнению A=10exp(x/20) B=10-A |
Обратимые реакции
Предположим, вещество A может превращаться в вещество B, а оно, в свою очередь, обратно переходит в вещество A. Изменение концентрации вещества A обусловлено одновременным протеканием двух реакций: распада A со скоростью k1[A] и его образования со скоростью k2[B]. Скорость изменения концентрации вещества A равна разности этих величин:
| (8) |
Надо сказать, что чем сложнее схема реакции, тем сложнее соответствующая система уравнений, и преобразования могут стать довольно громоздкими. Поэтому в дальнейшем мы наряду с распространенным обозначением концентрации будем использовать переменные в виде малых латинских букв, т. е. a вместо [A], b вместо [B] и т
Концентрацию b находим из уравнения 6 материального баланса и подставляем в уравнение 8.
| (9) |
или, используя новые, более компактные обозначения:
| (10) |
Произведём разделение переменных:
| (10) |
и интегрирование в пределах от ao до a и от 0 до t:
| (11) |
После преобразований получаем весьма громоздкое выражение для значения концентрации субстрата:
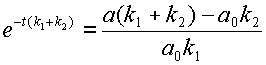 откуда
откуда ![]()
![]()
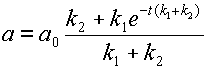 (12)
(12)
Это выражение можно несколько упростить, если ввести понятие равновесной концентрации вещества A: ![]() при
при ![]() .
.
| (13) |
Из уравнения 12 получаем,
| (14) |
Что вместе с 12 дает:
С другой стророны, из уравнения 13 находим
| (15) |
Разделив уравнение 14 на 15, получаем очень интересное выражение:
| (16) |
Откуда
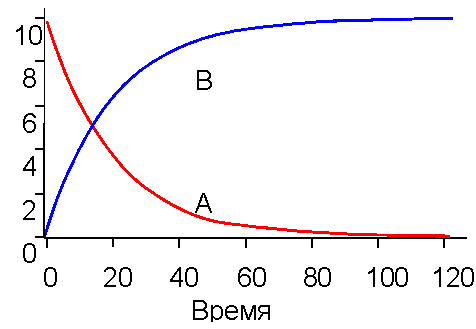
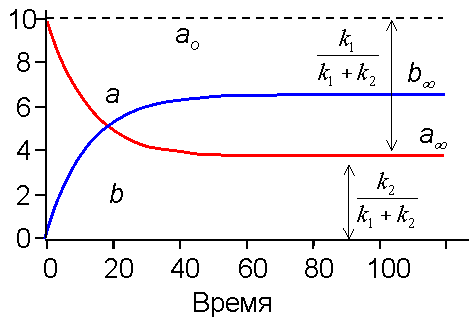
На рис. 2 приведены кривые кинетики (изменения во времени концентраций) для веществ A и B в случае обратимого процесса. Анализ этих кривых, если они получены экспериментально, сразу позволяет найти отношение констант скоростей k1/k2. Чтобы определить сами скорости, необходимо построить график в виде линейной анаморфозы (см. ниже).
| Рис. 2. Кинетика обратимой мономолекулярной реакции По отношению отрезков ординат для a при достижении равновесия (a∞ ) находим соотношение констант прямой и обратной реакции. (см. уравнение 16) |
Построение линейных анаморфоз
В химической кинетике кривые, полученные в эксперименте, стремятся путем математических операций превратить в прямые линии, поскольку анализ прямых позволяет получать параметры, включающие в себя константы скоростей реакций. Рассмотрим это на примерах обратимых и необратимых мономолекулярных реакций.
Для необратимой реакции существует линейная зависимость между логарифмом концентрации субстрата реакции и временем (см. уравнение 5):
| (17) |
Если найти опытным путем концентрации вещества A через разные промежутки времени после начала реакции, а затем построить график зависимости натурального логарифма концентрации от времени, то по тангенсу угла наклона полученной при этом прямой сразу находим константу скорости, поскольку она является угловым коэффициентом данной прямой (см. рис. 3).
| Рис. 3. Кривая расхода субстрата мономолекулярной реакции в полулогарифмическом масштабе. Объяснения даны в тексте. |
Построение линейной анаморфозы кинетической кривой для концентрации субстрата обратимой мономолекулярной реакции требует экспериментального определения равновесной концентрации субстрата a∞ , т. е. той концентрации, которая установится по источению некоторого времени и в дальнейшем не будет изменяться. Затем из экспериментальных данных рассчитывается для каждого момента времени, при котором определяли концентрации, отношение 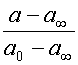 , натуральный логарифм которого откладываем по ординате графика как функцию времени (см. рис. 4). Получается прямая линия (см. уравнение 16):
, натуральный логарифм которого откладываем по ординате графика как функцию времени (см. рис. 4). Получается прямая линия (см. уравнение 16):
| (18) |
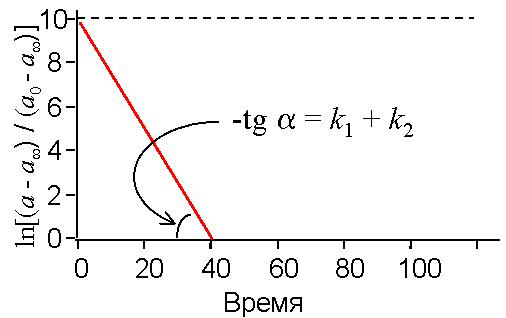
По тангенсу угла наклона этой прямой находим сумму констант скоростей прямой и обратной реакции (см. рис. 4).
| Рис. 4. Кинетика обратимой мономолекулярной реакции Данные представлены в формате, позволяющем найти сумму констант скоростей прямой и обратной реакции по тангенсу угла наклона прямой. Объяснения - в тексте. |
Отношение констант мы находим из уравнения 13

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |



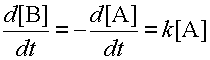
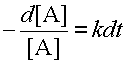 ;
; 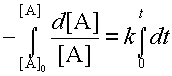 ;
; 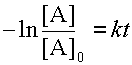
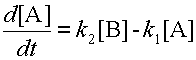
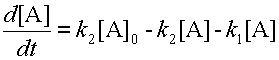
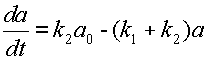
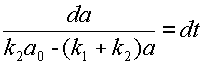
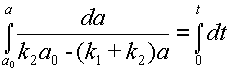
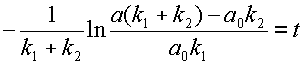
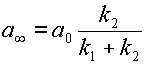
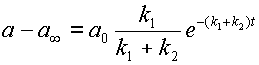
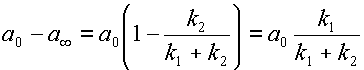
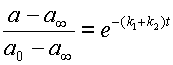
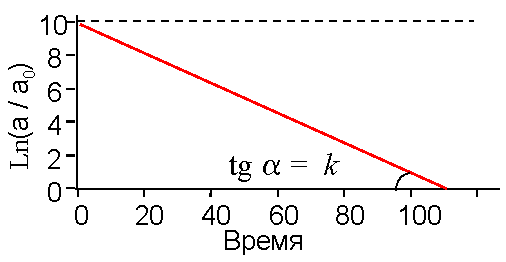
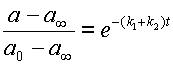 откуда
откуда