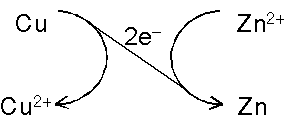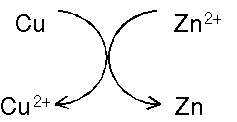Полу-реакция | Eo (B) |
Li+(aq) + e - → Li(s) | -3,05 |
Na+(aq) + e - → Na(s) | -2,37 |
Zn+(aq) + e - → Zn(s) | -0,76 |
H+(aq) + e - → H(g) | 0,00 |
Cu+(aq) + e - → Cu(s) | +,15 |
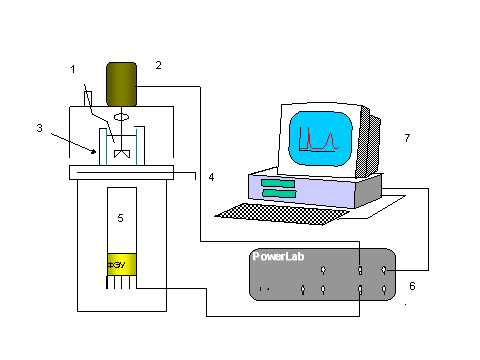
Используя эту таблицу и уравнение 7, находим электродвижущую силу гальванического элемента, состоящего из цинкового и медного электродов при концентрациях ионов цинка и меди 1М. Величина ЭДС равна - 0,76-,15=-0,91 В.
Окислительно-восстановительные потенциалы
Реакции в растворах
Реакции окисления-восстановления могут протекать также в растворах, если все четыре участника процесса растворимы в воде. В этом случае мы, разумеется, не видим никакого внешнего проявления переноса электронов, тогда как в гальваническом элементе мы можем измерить электрический ток во внешней цепи. В биохимической литературе окислительно-восстановительные реакции между участниками обычно изображаются в виде стрелок. При этом окислительно-восстановительная реакция в гальванической ячейке будет выглядеть примерно таким образом:
В гальванической ячейке
| В растворе
|
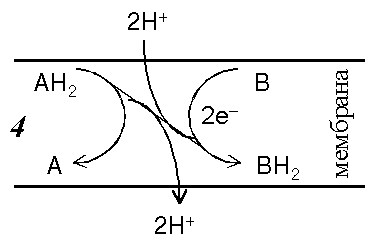
В живой клетке участниками окислительно-восстановительных реакций служат обычно молекулы, растворенные в воде или в липидной фазе биологических мембран. К таким веществам относятся ионы металлов переменной валентности, например ионы Fe2+ (восстановленная форма) и ионы Fe3+ (окисленная форма), цитохромы, в которых железо также может двух - или трехвалентном состоянии, коэнзим Q (убихинон), пиридиннуклеотиды, аскорбиновая кислота и т При этом переносчики электронов находятся в мембране. Особенность переноса электронов в определенных участках дыхательной цепи митохондрий заключается в том, что одновременно с переносом электрона происходит перенос протона через мембрану. Схематически это можно представить себе таким образом:
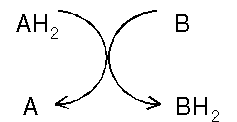
Перенос электрона в растворе
| Перенос электрона в дыхательной цепи
|
Более подробно этот вопрос рассмотрен в лекции "Хемоосмотическая теория окислительного фосфорилирования".
Свечение, сопровождающее биохимические реакции
РЕЗЮМЕ
Хемилюминесценцией (ХЛ) называется свечение, сопровождающее химические реакции. Она наблюдается в том случае, если в реакции происходит выделение большого количества энергии, например в реакции взаимодействия двух радикалов или в реакциях с участием перекисей. В последнее время все больший интерес привлекает собственное ("сверхслабое") свечение клеток и тканей животных и человека, которое обусловлено реакциями свободных радикалов: радикалов липидов и кислорода, а также окиси азота, - соединениями, играющими огромную роль в жизни организма, а при определенных условиях - и развитии ряда патологических состояний.
Введение
Энергично протекающие химические реакции сопровождаются, как правило, выделением энергии в форме тепла; существуют, однако такие реакции, которые сопровождаются излучением света. свечение, сопровождающее химические реакции, называется хемилюминесценцией (ХЛ).
Как правило, хемилюминесценция имеет низкую интенсивность и для ее измерения используют специальные приборы - хемилюминометры. Схема одного из современных хемилюминометров дана на рис. 1.
| Рис.1.Прибор для измерения хемилюминесценции (хемилюминометр) 1 - термостатируемая кювета, снабженная устройством для перемешивания и добавления растворов в ходе опыта; 2 - трубочка для введения добавок и отбора проб по ходу опыта; 3 - электромотор мешалки; 4 - приемник света - фотоэлектронный умножитель (ФЭУ); 5 - интерфейс, передающий сигналы от усилителя фототока (6) в персональный компьютер (7) и одновременно управляющий температурным режимом в кювете и скоростью перемешивания раствора (8). |
Раствор или суспензия клеток помещаются в кювету, в которой поддерживается определенная температура и осуществляется перемешивание для лучшего снабжения кислородом. В кювету по ходу опыта вводят различные добавки и отбирают пробы для химического анализа. Свет ХЛ измеряют с помощью чувствительного прибора - фотоумножителя (ФЭУ), электрический сигнал от которого усиливается, а затем обрабатывается и записывается. В настоящее время для обработки и записи сигналов используют персональные компьютеры (ПК). Между компьютером и хемилюминометром включают промежуточный прибор - интерфейс, делающий электрические сигналы от ФЭУ "понятными"для ПК..
Процессы жизнедеятельности, как теперь стало известно, практически всегда сопровождаются очень слабым излучением, которое иногда называют сверхслабым свечением или собственным излучением клеток и тканей [1]. Некоторые организмы обладают, однако способностью излучать довольно яркий свет, видимый простым глазом; это явление известно с древних времен и получило название "биолюминесценция".
В биохимических системах, т. е. в гомогенатах тканей, суспензиях клеток или клеточных органелл, смесях ферментов и субстратов, собственная хемилюминесценция в большинстве случаев отличается крайне низкой интенсивностью, и требуется особо чувствительная аппаратура, чтобы его обнаружить и измерить. Некоторые вещества, которые в отечественной литературе принято называть активаторами ХЛ (в англоязычной литературе используется термин enhancer), обладают способностью усиливать хемилюминесценцию, иногда во много тысяч раз.
Ниже приведена классификация явлений хемилюминесценции в биологических системах.
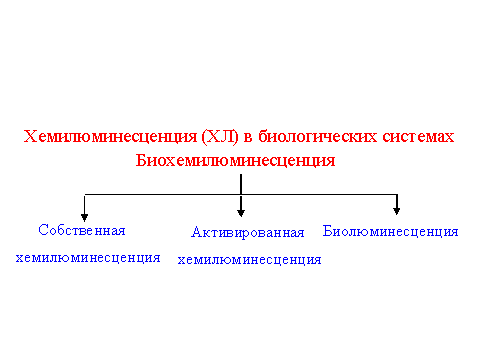
Помимо этого, слабым свечением сопровождается образование свободных радикалов при действии ряда физических факторов на объект: при облучении ионизирующей радиации наблюдается радиохемилюминесценциярадиохемилюминесценция, после облучения ультрафиолетом или видимым светом - фотохемилюминесценции, при пропускании электрического тока - электролюминесценция, при воздействии ультразвука - сонолюминесценция, при воздействии сил трения - триболюминесценция. .
Молекулярный механизм хемилюминесценции
В настоящее время известно довольно много химических реакций, сопровождающихся свечением. В большинстве случаев - это довольно сложные процессы со многими промежуточными стадиями. Но есть несколько простых случаев, в которых механизм превращения энергии химической реакции в свет вполне понятен [1,2].
Один из них - это свечение, наблюдаемое при взаимодействии органических радикалов, получаемых электрохимическим путем. В раствор люминесцирующего органического вещества (в опытах брали полициклические углеводороды) в органическом электролите (проводящем электричество) опускали пару электродов, с помощью которых через раствор пропускали электрический ток.
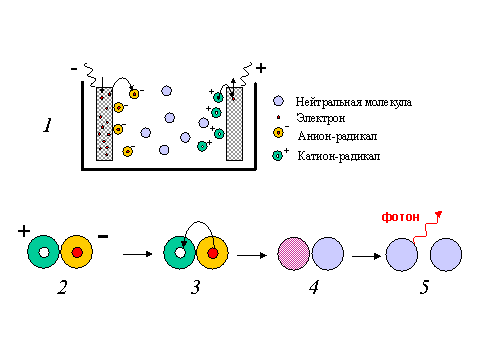
Рис. 2. Хемилюминесценция при рекомбинации катион - и анион-радикалов полициклических углеводородов.
1 - Между электродами, опущенными в раствор органического электролита, прикладывают разность потенциалов. С катода электроны захватываются молекулами и образуются анион-радикалы. На аноде электроны отрываются от молекул и образуются катион-радикалы.
2 - 5 - При взаимодействии катион-радикала и анион-радикала в результате их столкновения (2) электрон переходит с катион-радикала на анион-радикал (3). Однако при этом есть вероятность того, что он окажется не на самом нижнем электронном уровне, а на более высоком. Образуется возбужденная молекула углеводорода (красный кружок на схеме 4). При переходе электрона на более низкий уровень происходит высвечивание кванта света (5). Схема электронных уровней в радикалах и молекулах продуктов реакции дана на рис. 3.
С катода (-) на молекулы люминесцирующего вещества (обозначим их как НА) переходят электроны и образуются анион-радикалы (заряженные отрицательно). На аноде (+) электроны отнимаются от молекул и образуются катион-радикалы (заряженные положительно, см. рис. 2, вверху). Если теперь раствор перемешать, катион-радикалы будут взаимодействовать с анион-радикалами (рис. 2, внизу); при этом образуется две молекулы исходного углеводорода, одна из которых может оказаться в электронно-возбужденном состоянии и переходит в основное состояние с испусканием кванта света (фотона).
На рис. 3 показаны верхние электронные энергетические уровни в реагирующих радикалах и продуктах их взаимодействия. В молекулах на верхнем заполненном электронном уровне электроны расположены попарно (рис. 3, 1). У катион-радикала на верхнем уровне остается только один, неспаренный электрон. У анион радикала появляется неспаренный электрон на следующем (расположенном выше) энергетическом уровне (рис. 3, 2).
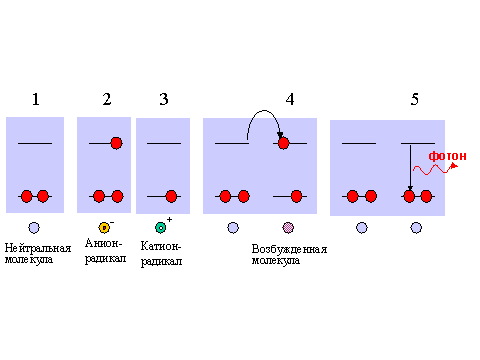
Рис. 3. Схема электронных энергетических уровней участников реакции взаимодействия катион-радикала и анион-радикала одного и того же вещества.
1 - исходная молекула; 2 - анион-радикал; 3 - катион-радикал; 4 - перенос электрона с анион-радикала на катион-радикал; 5 - перенос электрона в электронно-возбужденной молекуле продукта реакции, который сопровождается высвечиванием кванта света хемилюминесценции.
При взаимодействии радикалов (имеющих противоположный заряд и потому притягивающихся друг к другу) произойти перенос электрона может произойти таким образом, что два электрона окажутся на разных уровнях (рис. 3, 4). Последнее означает, что один из ее внешних электронов оказывается не на самом нижнем свободном электронном уровне, как у исходных молек).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |