2.5.2 Групповые реагенты
1 Групповым реагентом в аммиачно-фосфатной классификации катионов является … .
а) раствор (NH4)2CO3 в аммиачном буфере;
б) раствор H2S;
в) раствор (NH4)2HPO4 в водном растворе аммиака;
г) раствор NaOH в присутствии Н2О2.
2 Групповым реагентом в сероводородной классификации катионов является … .
а) раствор HNO3;
б) раствор (NH4)2S;
в) раствор NH4OH;
г) раствор (NH4)2HPO4.
3 Групповым реагентом в кислотно-основной классификации катионов является … .
а) раствор H2SO4;
б) раствор H2S;
в) раствор (NH4)2HPO4;
г) раствор (NH4)2S.
4 Групповым реагентом для группы катионов Ag+, Hg+, Pb+2 является водный раствор … .
а) H2SO4;
б) HCl;
в) NaOH в присутствии Н2О2;
г) NH4OH.
5 Групповым реагентом для группы катионов Zn+, Al+3, Sn+4, Cr+3 является водный раствор … .
а) NaOH в присутствии Н2О2;
б) H2SO4;
в) HCl;
г) NH4Cl.
6 Групповым реагентом для группы катионов Co+2, Ni+2, Cu+2, Cd+2, Hg2+ является водный раствор … .
а) HCl;
б) H2SO4;
в) NH4OH;
г) HNO3.
7 Групповым реагентом на катионы Ca+2, Sr+2, Ba+2 является водный раствор … .
а) HCl;
б) NaOH;
в) NH4OH;
г) H2SO4.
8 Гидроксиды металлов амфотерны и растворимы в избытке щелочи … .
а) Na+, K+, NH+4;
б) Mg+2, Mn+2, Fe+2;
в) Ca+2, Sr+2, Ba+2;
г) Zn+2, Al+3, Cr+3.
9 Гидроксиды металлов растворяются в избытке аммиака с образованием комплексных соединений … .
а) Fe+3, Bi+3, Sb+3;
б) Ca+2, Sr+2, Ba+2;
в) Co+2, Ni+2, Cd+2;
г) Na+, K+, NH+4.
10 Гидроксиды металлов нерастворимы в избытке растворов едкого натра или аммиака … .
а) Mg+2, Mn+2, Fe+2;
б) Zn+2, Al+3, Cr+3;
в) Co+2, Ni+2, Cu+2;
г) Na+, K+, NH+4.
11 Групповым реагентом на анионы SO42-, SO3-2, S2O32- является раствор … .
а) AgNO3;
б) NH4OH;
в) BaCl2;
г) NaOH.
12 Водным раствором AgNO3 осаждаются анионы … .
а) Cl–;
б) S2–;
в) NO![]() ;
;
г) Br –;
д) I –;
е) NO![]() ;
;
ж) CH3COO–.
13 Соли бария и серебра, растворимые в воде, – … .
а) нитраты;
б) карбонаты;
в) силикаты;
г) нитриты;
д) хлориды;
е) фосфаты;
ж) ацетаты.
14 Соли бария, нерастворимые в воде, – … .
а) BaSO4;
б) Ba3(PO4)2;
в) Ba(NO3)2;
г) BaCO3;
д) Ba(CH3COO)2;
е) BaCl2;
ж) BaSO3.
15 Осадки, полученные в реакциях, нерастворимы в разбавленной азотной кислоте:
а) Na2S + AgNO3 ® … ;
б) BaCl2 + AgNO3 ® … ;
в) Na2CO3 + AgNO3 ® … ;
г) K2SO3 + AgNO3 ® … .
2.5.3 Качественный анализ катионов
1 Осадок черного цвета образуется при взаимодействии катиона [Hg2]2+ с реагентом … .
а) SnCl2;
б) NaOH;
в) K2CrO4;
г) Cu (металлическая).
2 Катион серебра образует осадок красного цвета с реагентом … .
а) K2CrO4;
б) KOH;
в) HCl;
г) KBr.
3 Ярко-желтый осадок образуется при взаимодействии Pb+2 с реагентом … .
а) KI;
б) HNO3;
в) H2SO4;
г) дитидон.
4 Соответствие между определяемым катионом и реагентом:
а) Fe+2; 1) K4[Fe(CN)6];
б) Fe+3; 2) PbO2;
в) Mn+2; 3) магнезон I;
г) Mg+2. 4) K3[Fe(CN)6].
5 Соответствие между определяемым катионом и реагентом:
а) Cd+2; 1) диметилглиоксим;
б) Ni+2; 2) CNS(NH2)2;
в) Co+2; 3) KCNS;
г) Hg+2. 4) KI.
6 Ализарин С14Н6О2(ОН)2 образует в аммиачной среде с Al(OH)3 … .
1) труднорастворимое соединение ярко-красного цвета;
2) осадок ярко-синего цвета;
3) растворимое соединение голубой окраски;
4) бесцветный раствор с резким запахом аммиака.
7 Катионы металлов окрашивают пламя в соответствующий цвет:
а) калий; 1) оранжево-красный
б) кальций; 2) зелёный
в) натрий; 3) розово-фиолетовый
г) медь. 4) желтый
8 Соответствие между катионами и реактивами, используемыми для их обнаружения:
а) Ba+2; 1) (NH4)2C2O4
б) Sr+2; 2) K2Cr2O7
в) Ca+2. 3) (NH4)2SO4
9 Диметилглиоксим (реактив Чугаева) в аммиачной среде образует розово-красное соединение с катионом … .
а) магния;
б) цинка;
в) кальция;
г) никеля (II).
10 Катион Cd+2 образует желтый осадок при взаимодействии с … .
а) сероводородом;
б) хлоридом натрия;
в) трилоном Б;
г) азотной кислотой.
11 Катионы Cr+3 в щелочной среде можно обнаружить действием раствора … .
а) K2CO3;
б) NH4NO3;
в) Na2SO4;
г) H2O2.
12 Катион Zn+2 образует комплексное соединение красного цвета с … .
а) гексацланферратом (II) калия;
б) аммиаком;
в) дитизоном;
г) ЭДТА.
13 Темно-синий осадок комплексной соли, берлинская лазурь, образуется при взаимодействии гексацианоферрата (II) калия с катионом … .
а) Fe+2;
б) Mn+2;
в) Fe+3;
г) Mg+2.
14 Красный осадок образуется при взаимодействии H2S с катионом … .
а) Fe+2;
б) Mn+2;
в) Bi+3;
г) Sb+3.
15 Зеленовато-желтые кристаллы с уранилацетатом образуют катионы … .
а) натрия;
б) калия;
в) аммония.
2.5.4 Качественный анализ анионов
1 Белый творожистый осадок при взаимодействии AgNO3 образуют анионы … .
а) Br–;
б) Cl –;
в) I –;
г) S2–.
2 Сульфид-ион образует с ионами серебра осадок … цвета.
а) черного;
б) белого;
в) красного;
г) желтого.
3 В азотной кислоте при нагревании растворяется осадок … .
а) AgCl;
б) AgBr;
в) AgI;
г) Ag2S.
4 При действии перманганата калия в кислой среде на хлорид-ионы образуется:
а) ClO–;
б) Cl2;
в) ClO![]() ;
;
г) ClO![]() .
.
5 При действии Pb(NO3)2 на анионы I аналитической группы осадок белого цвета образуется с … .
а) Cl –;
б) Br –;
в) I –;
г) S –2.
6 Фосфат-ионы образуют желтый осадок при взаимодействии с … .
а) BaCl2;
б) Pb(CH3COO)2;
в) AgNO3;
г) CaCl2.
7 Соответствие между анионом и реагентом:
а) NO ![]() ; 1) сульфаниловая кислота + 2 нафтиламин;
; 1) сульфаниловая кислота + 2 нафтиламин;
б) NO ![]() ; 2) хлорид железа (III);
; 2) хлорид железа (III);
в) CH3COO–; 3) молибдат аммония;
г) PO![]() . 4) дифениламин.
. 4) дифениламин.
8 В соляной кислоте не растворяется осадок … .
а) BaSO3;
б) BaSO4;
в) BaCO3;
г) BaS2O3.
9 Желтый кристаллический осадок образуется при действии молибдата аммония (NH4)2MoO4 на … .
а) SO![]() ;
;
б) SO![]() ;
;
в) CO![]() ;
;
г) PO![]() .
.
10 Осадок образуется при действии 2н раствора HCl на … .
а) NaSO4;
б) Na2CO3;
в) Na2SiO3;
г) Na2SO3.
11 Газ образуется при действии 2н раствора HCl на … .
а) Na2CO3;
б) Na2SO4;
в) Na2SiO3;
г) Na3PO4.
12 Перманганат калия обесцвечивается в кислой среде в присутствии … .
а) Na2SO4;
б) Na2CO3;
в) Na2SiO3;
г) Na2SO3.
13 Осадок черного цвета образуется при взаимодействии Pb(NO3)2 с … .
а) Cl–;
б) Br –;
в) I –;
г) S 2–.
14 К раствору, содержащему Br – и подкисленному 2н H2SO4, добавили небольшое количество хлорной воды. Появление бурой окраски свидетельствует о выделении свободного … .
15 Хлорная вода окисляет иодид-ионы до элементного … .
2.6 Количественный анализ
2.6.1 Гравиметрия
1 Гравиметрия – метод количественного анализа, основанный на … .
а) точном измерении массы компонента пробы в виде прокаленного осадка известного состава;
б) точном измерении объема реагента, необходимого для осаждения определяемого компонента;
в) точном измерении массы реагента, необходимого для осаждения определяемого компонента;
г) точном измерении массы пробы, взятой для анализа.
2 Последовательность стадий гравиметрического анализа:
а) фильтрование полученной смеси для отделения осадка;
б) взвешивание полученного соединения;
в) прокаливание осадка для превращения в гравиметрическую форму;
г) осаждение определяемого вещества подобранным осадителем;
д) растворение навески.
3 Соответствие реагента анализируемому веществу в гравиметрии:
а) Ni+2; 1) HCl4
б) Al+3; 2) H2C2O4;
в) Ag+1; 3) 8-гидроксихинолин;
г) Ca+2. 4) диметилглиоксим.
4 Содержание бария в пробе BaCl2 · 2Н2О массой 0,4225 г, если масса прокаленного осадка BaSO4 равна 0,4044 г (А(Ba) = 137, М(BaSO4) = 233), составляет … % (с точностью до сотых долей).
5 Аналитический множитель F при определении Fe в виде Fe2O3 составляет …
(A(Fe) = 56, A(O) = 16).
а) 0,6994;
б) 0,3507;
в) 0,5000;
г) 0,1750.
6 Содержание Fe в пробе массой 0,4806 г, если масса прокаленного осадка Fe2O3 равна 0,4624 г составляет … % (A(Fe) = 56, A(O) = 16) (с точностью до сотых долей).
7 Содержание Al в образце массой 0,5014 г составляет 26,35%. Масса прокаленного осадка Al2O3 равна … г (A(Al) = 27, A(O) = 16).
8 Аналитический множитель F при определении Cr в виде Cr2O3 равен … (A(Cr) = 56, A(O) = 16).
9 При сливании равных объемов ![]() растворов хлорида железа гидроксида натрия образуется осадок, т. к. ионное произведение равно (
растворов хлорида железа гидроксида натрия образуется осадок, т. к. ионное произведение равно (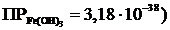 :
:
а) ![]()
б) ![]()
в) ![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
