O3S + : OH2 = O3S : OH2.
Как видно из примера, в качестве кислоты выступают молекулы BCl3 и SO3, а в качестве оснований – молекулы аммиака и воды.
Редокс-реакции сопровождаются изменением степеней окисления реагирующих веществ вследствие переноса электронов от восстановителя (отдаёт электроны) к окислителю (принимает электроны). При окислении степень окисления повышается, при восстановлении – понижается.
Например: K2Mn+6O4 + 8HCl– = 2KCl + Mn+2Cl2 + Cl![]() + 4H2O
+ 4H2O
MnO4 + 8H+ + 4ē → Mn+2 + 4H2O – восстановление
(MnO![]() – окислитель)
– окислитель)
2Cl– – 2ē → Cl![]() – окисление (Cl– – восстановитель).
– окисление (Cl– – восстановитель).
Интенсивность присоединения или отдачи электронов различными ионами (молекулами) определяется окислительно-восстановительным (редокс) потенциалом. Величину реального редокс-потенциала рассчитывают по уравнению Нернста:
Е = Е0 + 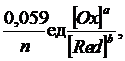
где Е – реальный (равновесный редокс-потенциал, В);
Е0 – стандартный редокс-потенциал, В;
n – число электронов, участвующих в полуреакции;
[Ox], [Red] – равновесные концентрации окисленной и восстановленной форм, моль/л;
а, b – стехиометрические коэффициенты.
Константа равновесия связана со стандартными редокс-потенциалами окислителя и восстановителя:
lgK = 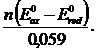
Демо-тест 3
Величина формального редокс-потенциала системы NO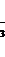 + 2H+ + 1ē → → NO2 + H2O при pH = 1 равна … В (E
+ 2H+ + 1ē → → NO2 + H2O при pH = 1 равна … В (E![]() ↛
↛![]() = 0,81 В):
= 0,81 В):
а) 1,032;
б) 0,928;
в) 0,692;
г) 0,810.
Формальным называют потенциал полуреакции окисленной и восстановленной форм, равный 1 моль/л, а концентрации посторонних ионов известны.
Формальный редокс-потенциал в данном случае рассчитывается по формуле:
Е red/ox = ![]()
(концентрация ионов водорода в квадрате, т. к. в уравнении полуреакции стехиометрический коэффициент перед [H+] равен двум).
Е red/ox = 0,81+ ![]() = 0,81 – 2·0,059 =0,81 –0,118 = 0,692 В.
= 0,81 – 2·0,059 =0,81 –0,118 = 0,692 В.
Вывод: верный ответ в).
Реакции комплексообразования – химические реакции, в которых в качестве реагентов участвуют комплексные соединения (например, Na3[CO(No3)3]) или образуются комплексные соединения (например, комплекс ализарина с катионом алюминия).
Согласно координационной теории А. Вернера (1893 г.) комплексные (координационные) соединения – это сложные молекулы, состоящие из центрального атома (комплексообразователя) и лигандного окружения и имеющие внешнюю и внутреннюю сферы. Центральный атом – чаще всего катион металла. Лигандами могут являться:
– анионы (например, NO![]() , CN–, Cl– );
, CN–, Cl– );
– молекулы (например, H2O, NH3), а также циклоообразующие (хелатирующие и макроциклические) комплексные соединения.
В комплексе Na2Pb[Сu(NO2)6] внутренняя сфера [Cu(NO2)6]4–, центральный ион – Cu+2, лиганды – NO![]() , ионы внешней сферы – Na+1, Pb+2.
, ионы внешней сферы – Na+1, Pb+2.
Демо-тест 4
Общая константа нестойкости [Сu(NO2)6]4– имеет вид:
а) Кн = 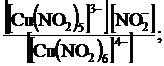
б) Кн = 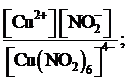
в) Кн = 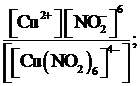
![]()
г) Кн = 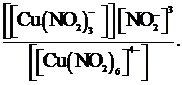
Применяя закон действующих масс, общая константа нестойкости комплексного иона [Сu(NO2)6]4– имеет вид:
Кн = 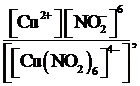
так как полная диссоциация комплексного иона идёт по уравнению
[Cu(NO2)6]4– ⇄ Cu2+ + 6NO![]() .
.
Чем больше константа нестойкости, тем легче проходит процесс диссоциации комплексного иона.
Вывод: верный ответ в).
Реакции осаждения сопровождаются образованием новой твёрдой фазы – осадка и широко используются в качественном и количественном анализе. Фаза представляет собой часть системы, отделённую от других частей поверхностностью раздела. В результате процессов осаждения и растворения между осадком и его растворенной частью наступает динамическое равновесие:
осадок ↔ раствор.
Произведением растворимости (ПР) малорастворимого электролита называется произведение концентрации (активности) ионов насыщенного раствора при постоянной температуре и давлении. ПР – величина постоянная при заданной температуре.
AmBn ⇄ mAn+ + nBm–
ПP![]() = [An+]m ·[Bm–]n,
= [An+]m ·[Bm–]n,
где [An+], [Bm–] – равновесные концентрации ионов малорастворимого вещества в растворе.
Чем меньше величина ПР, тем менее растворимо данное соединение.
Растворимостью (Р) малорастворимого соединения называют концентрацию его ионов в растворе над осадком и рассчитывают в г/л.
Осадок малорастворимого вещества образуется только в том случае, когда произведение концентрации его ионов в растворе превышает величину произведения растворимости этого соединения.
Таблица 4
Условия образования и растворения осадка
Соотношение П и ПР* | Характеристика раствора | Состояние твёрдой фазы |
П < ПР | Не насыщен | Растворяется |
П = ПР | Насыщен | Равновесие с раствором |
П > ПР | Перенасыщен | Осаждается |
- П – произведение концентраций ионов малорастворимого вещества, ПР – его произведений растворимости.
Демо-тест 5
Растворимость CaCrO4 в воде равна … г/л (ПР![]() = 7,1·10–4, М
= 7,1·10–4, М![]() = = 156 г/моль).
= = 156 г/моль).
а) 2,60·10–2;
б) 7,10·10–4;
в) 4,15·10–2;
г) 4,15.
Р![]() =
= 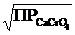 =
= 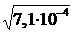 = 2,66·10–2
= 2,66·10–2 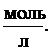
Т. к. М![]() = 156 г/моль, следовательно, Р
= 156 г/моль, следовательно, Р![]() = 2,6·10–2 ·156 = 4,15 г/л.
= 2,6·10–2 ·156 = 4,15 г/л.
Вывод: верный ответ г).
Таблица 5
Виды качественного химического анализа
Название метода | Сущность метода | Примеры |
Элементный | Какие элементы входят в состав анализируемого объекта | Определение наличия тяжёлых металлов в сточных водах |
Изотопный | Определение изотопов в смесях при исследовании искусственных элементов | Определение дейтерированной воды в обычной воде |
Молекулярный | Определение молекул химических соединений в газовых смесях | Определение в воздухе азота, СО2, озона |
Структурно-групповой | Определение функциональных групп органических соединений | Определение –СООН, –NH2, –SH и проч. групп в синтетических органических молекулах |
Фазовый | Определение наличия отдельных фаз в твёрдых объектах | Определение содержания углерода в сплавах в виде угля и карбидов железа |
Анализ химического соединения (и его составных частей: молекул, группировок атомов, ионов) возможен благодаря совокупности присущих ему свойств (физических, физико-химических и химических). Важнейшими аналитическими свойствами веществ являются:
– агрегатное состояние (характеристики: температура затвердевания, температура плавления, температура кипения, температура возгонки, плотность, показатель преломления);
– цвет (причины возникновения окраски);
– растворимость;
– химические свойства (кислотно-основные, окислительно-восстанови-тельные и т. д.).
Появление и изменение окраски веществ в ходе химической реакции является важнейшим аналитическим признаком, особенно в качественном анализе. Цвет органических молекул обусловлен наличием хромофорных групп (несущих цвет) и ауксохромных групп (усиливающих цвет).
Таблица 6
Виды хромофорных и ауксохромных групп
Название группы | Примеры |
Хромофоры | –N = N– – азогруппа >С = N– – азометиновая группа >С = NH – карбаминовая группа –NO2 – нитрогруппа –NO – нитрозогруппа |
Ауксохромы | –OH, –NH2, –SH, –OCH3, –NHCH3, –N(CH3)2, –COCH3 |
Демо-тест 6

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
