Ауксохромными группами являются … :
а) –SH;
б) –N = N–;
в) >С = N–;
г) –NHCH3;
д) –OH;
е) >С = NH.
Вывод: верные ответы а), г), д).
Методы разделения и концентрирования веществ используются для:
1) устранения мешающего влияния компонента путём физического или химического отделения его от определяемого вещества;
2) повышения отношения концентрации (или количества) микрокомпонентов к концентрации (или количеству) макрокомпонентов.
Методы разделения перечислены в таблице 7.
Таблица 7
Методы разделения
Название метода | Сущность метода |
Осаждение | В основе метода лежит различие в растворимости соединений определяемого и мешающего компонентов |
Экстракция | Основан на разделении веществ, при котором определяемое вещество извлекают из водного раствора с помощью органического растворителя, не смешивающегося с водой |
Хроматография | Основан на фазовом разделении смесей на отдельные компоненты с помощью адсорбции |
Осаждение считают полным, если в исходном растворе после выделения осадка остаётся не более 0,1 % массы определяемого компонента.
Механизмами осаждения (захвата осадком посторонних ионов, которые сами по себе в данных условиях не осаждаются) являются:
– адсорбция;
– химическое соосаждение;
– изоморфное соосаждение;
– окклюзия.
В экстракции, как методе распределения вещества между двумя несмешивающимися жидкостями, экстрагентами называются различные органические растворители (углеводороды, галогенпроизводные, высшие спирты, эфиры), экстрактом – вещества, извлечённые в фазу органического растворителя.
Константа распределения (Кд) для разбавленных растворов рассчитывается следующим образом:
Кд = ![]() или Кд =
или Кд = ![]()
где [А]о, ![]() – концентрация и растворимость вещества А в органической фазе;
– концентрация и растворимость вещества А в органической фазе;
[А]в, ![]() – концентрация и растворимость вещества А в водное фазе.
– концентрация и растворимость вещества А в водное фазе.
Коэффициент распределения (Д) зависит от pH, условий экстракции и рассчитывается следующим образом:
Д = ![]()
где ![]() ,
,![]() – общие концентрации всех форм вещества А в органической и водной фазах.
– общие концентрации всех форм вещества А в органической и водной фазах.
Коэффициент распределения (Д) связан с константой распределения (Кд) и константой диссоциации (Ка) по формуле:
Д = 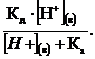
Степень извлечения R (%) показывает долю проэкстрагированного количества вещества от его общего количества:
R = 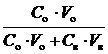 ·100 %,
·100 %,
где Со, Св – концентрации вещества в органической и водной фазах;
Vo, Vв – объёмы органической и водной фаз.
Степень извлечения зависит от коэффициента распределения и соотношения объёмов водной и органической фаз:
R = 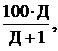
R = 100 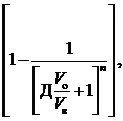
где n – количество повторных стадий экстракции.
Демо-тест 7
Степень извлечения кобальта из 20 мл его водного раствора двумя порциями по 10 мл изоамилового спирта равна … % (коэффициент распределения равен 5,2):
а) 83,9;
б) 90,1;
в) 92,3;
г) 96,4.
Степень извлечения R связана с коэффициентом распределения по формуле:
R = 100 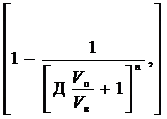 = 100
= 100 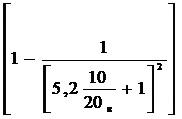 = 92,3.
= 92,3.
Вывод: верный ответ в).
Физико-химический метод разделения веществ, основанный на распределении компонентов между двумя фазами (подвижной и неподвижной), называется хроматографией.
Подвижная фаза, вводимая в слой неподвижной фазы, называется элюентом.
Подвижная фаза, выходящая из хроматографической колонки, называется элюатом.
Таблица 8
Хроматографические методы и их сущность
Название метода | Сущность метода |
Адсорбционный | Основан на различии в адсорбируемости веществ твёрдым сорбентом |
Распределительный | Основан на различии в растворимости разделяемых веществ в неподвижной фазе или на различии в растворимости веществ в подвижной и неподвижной фазах |
Колоночный | Основан на разделении компонентов в специальных колонках |
Тонкослойный | Основан на разделении компонентов смеси в тонком слое сорбента |
Ионообменный | Основан на различной способности веществ к ионному обмену |
Осадочный | Основан на образовании отличающихся по растворимости осадков разделяемых веществ с сорбентом |
График, связывающий аналитический сигнал (высота пика) с объёмом газа-носителя (V) или времени его прохождения (t) через сорбционную колонку, называется хроматограммой.
Основные характеристики колоночной хроматографии: время удержания и удерживаемый объём.
В основе ионообменной хроматографии лежит обратимый стехиометрический обмен ионов анализируемого раствора на подвижные ионы – противоионы сорбентов, называемых ионообменниками (ионитами). В качестве ионитов используют природные или синтетические смолы, не растворимые в воде высокомолекулярные кислоты и их соли, содержащие активные группы.
Схема катионного обмена:
RSO![]() H+ + M+ ⇄ RSO
H+ + M+ ⇄ RSO![]() M+ + H+
M+ + H+
(катионит)
RNH![]() OH– + А– ⇄ RТР
OH– + А– ⇄ RТР![]() А– + H–
А– + H–
(анионит)
Качественный анализ
Систематический метод анализа веществ основан на разделении ионов в растворе на группы с помощью групповых реагентов и обнаружении в пределах этих групп отдельных ионов с помощью характерных качественных реакций. Дробный метод анализа основан на непосредственном определении данного иона в исследуемом растворе с помощью качественной реакции в присутствии мешающих ионов, действие которых устраняется (маскируется) определёнными приёмами.
Маскирование – это торможение или полное подавление химической реакции в присутствии веществ, способных изменить её направление или скорость. Различают термодинамическое и кинетическое маскирование. При термодинамическом маскировании создают условия, при которых условная константа реакции понижается до такой степени, что реакция идёт незначительно. Кинетическое маскирование основано на увеличении разницы между скоростями реакции маскируемого и определяемого веществ с одним и тем же реагентом.
Групповые реагенты – это вещества, дающие схожие аналитические эффекты с несколькими ионами, принадлежащими к одной аналитической группе.
Таблица 9
Применяемые групповые реагенты в сероводородной, аммиачно-фосфатной
и кислотно-щелочной классификациях катионов
Номер группы | Групповые реагенты | ||
Сероводородная классификация | Аммиачно-фосфатная классификация | Кислотно-щелочная классификация | |
I | – | – | – |
II | Раствор (NH4)2CO3 в аммиачном буфере (pH ≈ 9,2 ) | Раствор (NH4)2HPO4 в водном аммиаке (25 %)*** | Раствор H2SO4 |
III | Раствор (NH4)2S (pH = 7–9)* | Раствор (NH4)2HPO4, фосфаты растворимы в водном аммиаке | Раствор HCl |
IV | Раствор H2S, pH = 0,5 (HCl)** | Раствор HNO3 | Раствор NaOH в присутствии H2O2 |
V | Раствор HCl | Раствор HCl | Водный раствор аммиака (NH4OH) |
VI | – | – | Водный раствор аммиака (NH4OH) |
Примечание:
* – катионы Al3+, Cr3+ осаждаются в виде гидроксидов, а катионы Zn2+, Mn2+, Fe2+, Fe3+, Co2+, Ni2+ осаждаются в виде сульфидов;
** – сульфиды катионов Cu2+, Cd2+, Hg2+, Bi2+ не растворяются в растворе сульфида натрия Na2S и в растворе полисульфида аммония (NH4)2Sn, а сульфиды катионов Sn2+, Sn4+, Sb3+, Sb5+, As3+, As5+ растворяются в растворе сульфида натрия или полисульфида аммония;
*** – фосфаты катионов Li+, Mg2+, Ca2+, Sr2+, Ba2+, Mn2+, Fe2+ растворяются в растворе уксусной кислоты CH3COOH, а фосфаты катионов Al3+, Bi3+, Cr3+, Fe3+ не растворяются в растворе уксусной кислоты.
Для разделения катионов наиболее известны сероводородная (сульфидная), аммиачно-фосфатная и кислотно-щелочная (кислотно-основная) схемы анализа.
Таблица 10
Сопоставление групп катионов в сероводородной, аммиачно-фосфатной
и кислотно-щелочной аналитических классификациях катионов
Номер группы | Катионы | ||
Сероводородная классификация | Аммиачно-фосфатная классификация | Кислотно-щелочная классификация | |
I | NH | NH | NH |
II | Ca2+, Sr2+, Ba2+ | Li+, Mg2+, Ca2+, Sr2+, Ba2+, Mn2+, Fe2+, Al3+, Bi3+, Cr3+, Fe3+ | Ca2+, Sr2+, Ba2+ |
III | Al3+, Cr3+, Zn2+, Mn2+, Fe2+, Fe3+, Co2+, Ni2+ | Cu2+, Zn2+, Cd2+, Hg2+, Co2+, Ni2+ | Ag+, Hg+, Pb2+ |
IV | Cu2+, Cd2+, Hg2+, Bi3+, Sn2+, Sn4+, Sb3+, Sb5+, As3+, As5+ | Sn2+, Sn4+, Sb3+, Sb5+, As3+, As5+ | Zn2+, Al3+, Sn2+, Sn4+, Cr3+ |
V | Ag+, Hg | Ag+, Hg | Sb3+, Sb5+, Bi3+, Mn2+, Fe2+, Fe3+ |
VI | – | – | Co2+, Ni2+, Cu2+, Cd2+, Hg2+, (Mg2+) |
Примечание: нумерация групп в различных источниках литературы может различаться.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)
